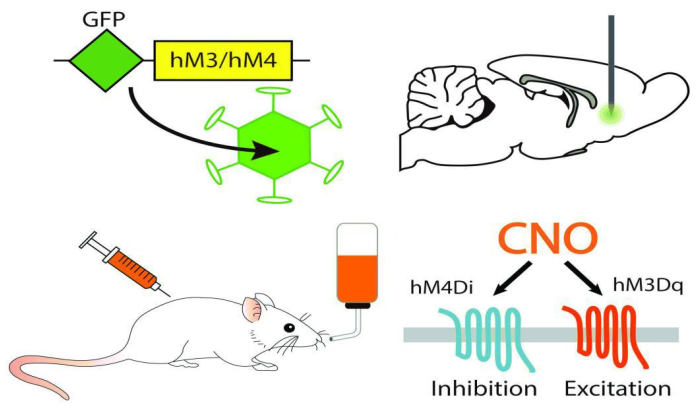
化学遗传学调控特定神经元活性——21世纪神经科学研究的利器!
化学遗传学(Chemical genetics)又称药物遗传学,是通过调查筛选化学小分子库,而对蛋白质功能以及细胞内信号转导通路进行研究的一门学科。该技术是对一些生物大分子实行改造,使其能和先前无法识别的小分子进行相互作用的过程,从而达到控制生物大分子活性的作用。
随着生物和化学交融的更加紧密,通过对生物体原有的配体与受体进行改造,得到了大量的具有外源物质激活、调节细胞通路的人工改造受体。目前改造的受体包括蛋白激酶、核酸杂交、各种代谢酶和G蛋白偶联受体,基于G蛋白偶联受体改造的化学遗传学受体有很多,从1991年构建的等位基因特异激活的基因编码受体(Allele-specific activation of genetically encoded receptors),到1998年构建的只能被合成配体激活的受体(Receptorsactivated solely by synthetic ligands, RASSLs)和基因工程改造的受体(Engineered receptors),再到2007年构建的只由特定药物激活的受体(Designer receptors exclusively activated by designer drugs, DREADDs)(如图6)。现在DREADDs已成为应用最广泛的化学遗传学技术。
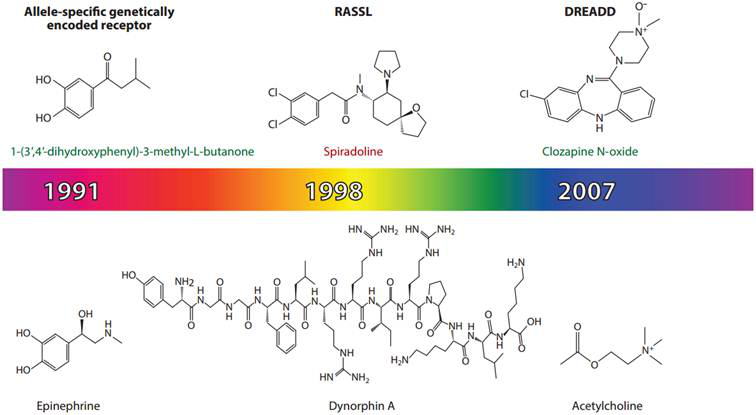
图1.化学遗传学改造天然受体得到的人工受体(Bryan L.Roth. Annu.Rev.Neurosci. 2014)
DREADDs技术是指只由特定药物叠氮平-N-氧化物(Clozapine-N-oxide,CNO)激活或抑制DREADDs受体,这些激活或抑制后的受体会选择性地作用于不同的GPCR级联反应来调节细胞信号转导,包括激活Gq、Gi、Gs、Golf和β-arrestin,其中应用最广泛的是Gq-DREADD和Gi-DREADD。
Gq-DREADD(hM3Dq)
hM3Dq是从人毒蕈碱乙酰胆碱受体M3上改造的仅对CNO(clozapine-N-oxide)有反应的人工受体(DREADD),不再受乙酰胆碱激活。在一些神经元里,CNO结合hM3D后,激活Gq蛋白偶联的磷酸酶PLCβ,引起PIP2被降解,从而使得被PIP2关闭的KCNQ外向钾离子通道被打开,以至于细胞膜去极化,形成动作电位。在KCNQ或是Gq不表达的神经元里,hM3D的功能可能会有所不同。
Gi-DREADD(hM4Di)
hM4Di是从人毒蕈碱乙酰胆碱受体M4上改造的仅对CNO(clozapine-N-oxide)有反应的人工受体(DREADD),不再受乙酰胆碱激活。在一些神经元里,CNO结合hM4D后,激活Gi蛋白偶联的内向钾离子通道GIRK,使得细胞膜超极化,抑制神经元细胞动作电位发放。 在不表达GIRK或是Gi的细胞中,hM4D的功能会有所不同。
激活或抑制神经元是通过激活或抑制DREADDs受体,而要想达到激活或抑制DREADDs受体的目的,就要选择相应的DREADDs受体。DREADDs的操作步骤如下(如图2):
①选择符合实验目的的DREADDs受体;
②将DREADDs受体基因和特异性启动子导入病毒载体并感染动物机体,使在靶细胞中表达DREADDs受体;
③在合适的时间点给予(立体定位、腹腔注射或喂水)实验动物CNO,激活或抑制DREADDs受体;
④通过行为学或电生理记录神经元活性改变带来的变化。
图2.化学遗传学的实验步骤
化学遗传学技术也被广泛用于神经科学领域,下面介绍几例运用该技术的研究案例:
案例1:
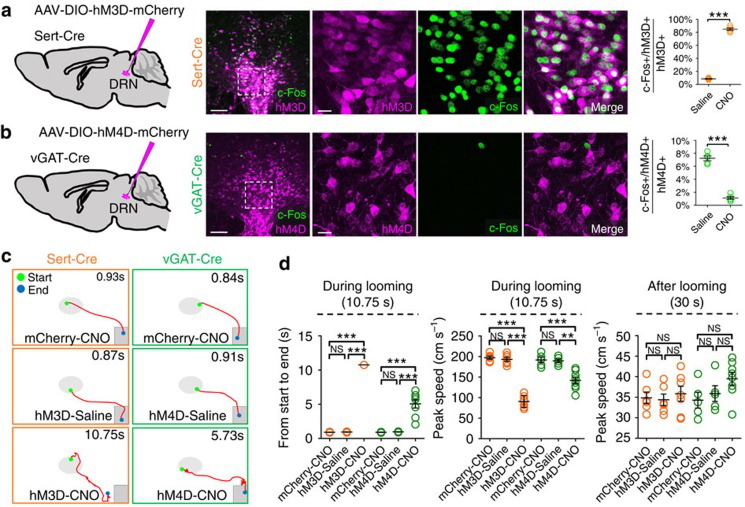
2017年3月,暨南大学任超然实验室在《Nature Communication》发表研究论文,该项工作是借助化学遗传、钙离子成像及神经示踪揭示了视网膜缝投射通路,及视网膜缝神经元对防御行为的调控(如图3)。
图3.视网膜缝神经元对防御行为的调控(Chaoran Ren, et al.,Nature Communication, 2017)
案例2:
此外,《Neuron》在2019年1月发表了国科学院上海生命科学研究院孙衍刚的工作,该工作借助了化学遗传学来研究外侧/腹外侧中脑导水管周围灰质(l/vlPAG)谷氨酸能神经元在瘙痒中的功能作用。作者通过抑制l/vlPAG谷氨酸能神经元后,观察到组胺或氯喹诱导的瘙痒抓挠行为明显减弱(如图4)。
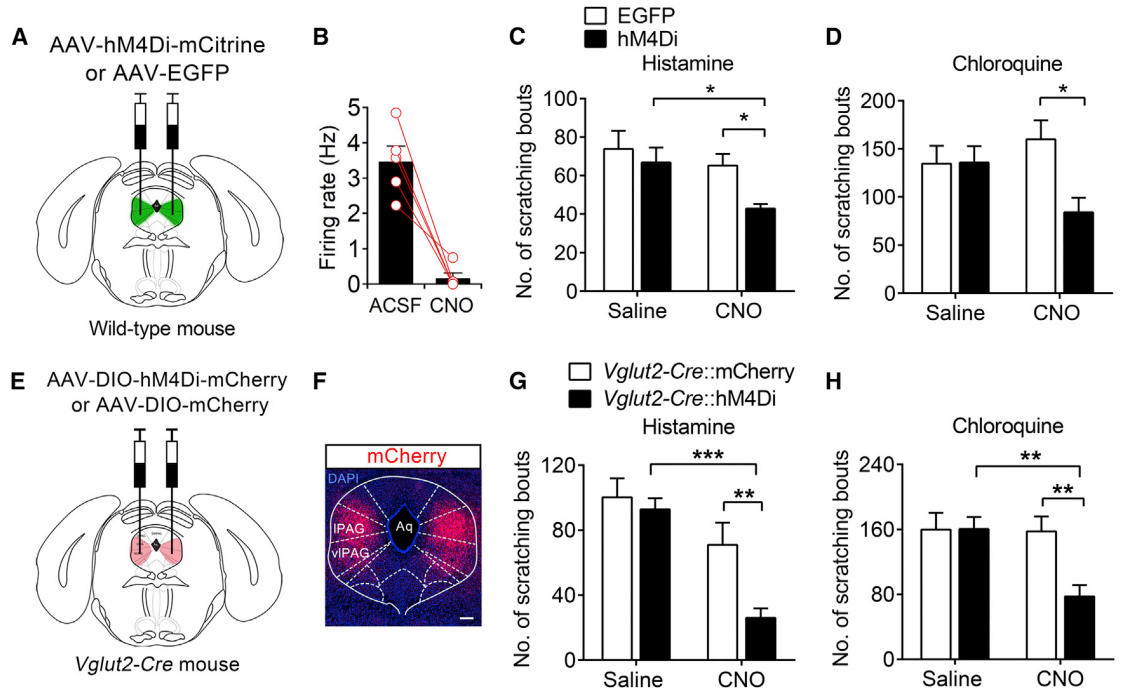
图4.l/vlPAG谷氨酸能神经元在瘙痒中的功能作用
| 功能描述 | 产品编号 | 产品名称 | 启动子 | 标签蛋白 | Cre/Flp依赖 |
| 化学遗传激活 | PT-0525 | rAAV-CaMKIIa-hM3D(Gq)-EGFP | CaMKIIa | EGFP | - |
| PT-0049 | rAAV-CaMKIIa-hM3D(Gq)-mCherry | CaMKIIa | mCherry | - | |
| PT-0152 | rAAV-hSyn-hM3D(Gq)-EGFP | hSyn | EGFP | - | |
| PT-1580 | rAAV-CaMKIIa-DIO-hM3D(Gq)-EGFP | CaMKIIa | EGFP | Cre依赖 | |
| 化学遗传抑制 | PT-0524 | rAAV-CaMKIIa-hM4D(Gi)-EGFP | CaMKIIa | EGFP | - |
| PT-0017 | rAAV-CaMKIIa-hM4D(Gi)-mCherry | CaMKIIa | mCherry | - | |
| PT-0153 | rAAV-hSyn-hM4D(Gi)-EGFP | hSyn | EGFP | - | |
| PT-1143 | rAAV-CaMKIIa-DIO-hM4D(Gi)-mCherry | CaMKIIa | mCherry | Cre依赖 |
更多产品,欢迎咨询!
1. Fenno L1, Yizhar O, Deisseroth K. The development and application of optogenetics. Annu Rev Neurosci. 2011;34:389-412.
2. Yizhar O, Fenno LE, Davidson TJ, Mogri M, Deisseroth K. Optogenetics in Neural Systems. Neuron. 2011;71(1):9-34.
3. Buchen L. Neuroscience: Illuminating the brain. Nature. 2010;465(7294):26-8.
4. Knowland D, Lilascharoen V, Pacia CP, Shin S, Wang EH, Lim BK. Distinct Ventral Pallidal
Neural Populations Mediate Separate Symptoms of Depression. Cell. 2017;170(2):284-297.
5. Zhang Z, Liu Q, Wen P, Zhang J, Rao X, Zhou Z, Zhang H, He X, Li J, Zhou Z, Xu X, Zhang X, Luo R, Lv G, Li H, Cao P, Wang L, Xu F. Activation of the dopaminergic pathway from VTA
to the medial olfactory tubercle generatesodor-preference and reward. Elife. 2017;6. pii: e25423.
6. Sternson SM, Roth BL. Chemogenetic tools to interrogate brain functions. Annu Rev Neurosci.
2014;37:387-407.
7. Huang L, Yuan T, Tan M, Xi Y, Hu Y, Tao Q, Zhao Z, Zheng J, Han Y, Xu F, Luo M, Sollars PJ, Pu M, Pickard GE, So KF, Ren C. A retinoraphe projection regulates serotonergic activity and looming-evoked defensive behaviour. Nat Commun. 2017;8:14908.
8. Ren S, Wang Y, Yue F, Cheng X, Dang R, Qiao Q, Sun X, Li X, Jiang Q, Yao J, Qin H, Wang G, Liao X, Gao D, Xia J, Zhang J, Hu B, Yan J, Wang Y, Xu M, Han Y, Tang X, Chen X, He C, Hu Z. The paraventricular thalamus is a critical thalamic area for wakefulness. Science.2018;
362(6413):429-434.
9. Gao ZR, Chen WZ, Liu MZ, Chen XJ, Wan L, Zhang XY, Yuan L, Lin JK, Wang M, Zhou L, Xu XH, Sun YG. Tac1-Expressing Neurons in the Periaqueductal Gray Facilitate the Itch-Scratching Cycle viaDescending Regulation. Neuron. 2019;101(1):45-59.e9.
信息订阅
我们将及时向您推送最新产品资讯

市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK