水疱性口炎病毒(Vesicular stomatitis virus,VSV)属于弹状病毒科(Rhabdoviridae)水疱病 毒属(Vesiculovirus) ,是有囊膜的单股负链RNA病毒。野生型VSV 具有顺向跨突触传播的特性,能感 染多种动物和昆虫,可以用于灵长类及啮齿类动物神经解剖学的研究。基于这类病毒对人及动物的低危 害性,已经被广泛用于疫苗和基因载体的开发。VSV作为嗜神经工具病毒,感染神经元后,在极短时间 内高丰度地表达目的蛋白。感染细胞后,其第一批子代病毒最快只需1.5 h 即可被释放出来。vanden Pol等通过构建囊膜糖蛋白缺失且携带GFP 报告基因的dG-VSV,在病毒感染细胞1 h之后即可检测到报告 基因的表达。Beier 等测试了VSV 对啮齿类大脑的感染特性,发现其具有顺行跨突触能力,同时也具有神经元感染的高度特异性,可被其他病毒的囊膜糖蛋白包装而获得不同方向的跨突触能力。他们发现VSV 利用其本身的囊膜糖蛋白(VSV-G)包装可顺向跨突触感染神经环路;同时,用RV的囊膜糖蛋白RV-G 替 换VSV的囊膜糖蛋白VSV-G之后,病毒可获得逆向跨突触感染神经环路的特性。2013 年,Beier等又 对VSV进行了一系列的改造工作,利用类似RV跨单突触系统的设计方法,实现了基于VSV 对特定神经 网络进行跨单级和跨多级的顺向和逆向标记。
VSV的囊膜糖蛋白(glycoprotein,G)是其顺向跨突触所必需的蛋白, G蛋白缺失的VSV(VSV- ΔG)会丧失跨突触能力,而其基因组的复制及转录不受影响(可继续高丰度表达外源基因),通过在被 VSV-ΔG感染的神经元中外源补偿VSV的G蛋白,VSV-ΔG可重获顺行跨突触能力从而感染下一级神经 元,而在下一级神经元中由于缺少G蛋白的补充,VSV-ΔG不能继续跨突触传播,从而可利用VSV-ΔG实 现可控的跨单级神经突触标记神经网络。禽类肉瘤病毒(Aviansarcoma-leukosisvirus,ASLV)的外膜蛋 白(EnvA)可通过识别其同源的病毒受体TVA 介导病毒特异性地感染细胞,而TVA 只存在于禽类细胞中, 在哺乳动物神经元中无表达。利用EnvA 膜外区与跨膜区及RV的G蛋白胞内区融合得到的重组囊膜蛋白 包装缺陷型的VSV-ΔG(VSV-EnvA-ΔG),其感染神经元需要TVA的表达,而其跨突触需要G蛋白的补偿。 结合特异的表达Cre重组酶的转基因动物品系及Cre-LoxP系统,通过立体定位注射AAV,可实现只在 特定区域特异类型神经元中表达TVA及G蛋白(VSV-G或RV-G),从而利用VSV-EnvA-ΔG实现对特异类 型神经元的顺向或逆向跨单级突触标记。此外,在利用AAV介导特异类型神经元表达TVA及VSV-G蛋白 的同时,使该神经元中表达一种荧光蛋白,如,GFP;而使VSV-EnvA-ΔG表达另一种荧光蛋白,如,RFP, 则起始感染的特异类型神经元可同时被标记为绿色和红色(黄色),而其直接输出的下一级神经元会被 标记为红色,从而可对特定类型神经元本身与其下游游神经元进行区分。在此基础上,使VSV带上CHR2 及Gcamp等基因,可实现对特异类型神经元的直接输出网络进行功能操纵及活动监测。
首先将AAV-EF1α-DIO-GFP-TVA 与AAV-EF1α-DIO-VSVG按照特定比例混合,然后向在特异神经元中表达Cre的转基因小鼠目标脑区立体定位注射AAV混合病毒。待AAV病毒充分表达两周以上, 即可在同一区域立体定位注射VSV-EnvA-ΔG-dsRed,VSV注射后12-14 h,可对动物心脏灌注,利用4%PFA固定后取出脑组织制备样本观察标记结果。
1、我们提供的AAV目前均为2/9型或5型,病毒滴度均约为1E+12v.g/mL,推荐的病毒混合比例为AAV-EF1α-DIO-GFP-TVA与AAV-EF1α-DIO-VSVG(或AAV-EF1α-DIO-RVG)按照体积比1:2混合。
2、推荐的注射体积为混合后的总体积100-300 nL,注射速度为20-50nL/min。若目标核团较小或Cre在该区域的外周围也有较多表达,为控制起始感染区域的特异性,可适当降低注射AAV病毒的体积及速度;反之,如需标记大范围或Cre只在局部区域高特异性表达,可增加AAV注射的体积与速度。
3、为保证VSV-EnvA-ΔG-dsRed注射时已有高丰度表达的TVA介导其感染神经元及G蛋白补偿其跨突触能力,AAV注射后需表达两周以上六周以内再注射VSV-EnvA-ΔG-dsRed,六周以外未进行相关实验评估, 但可尽量缩短AAV感染时间以缩短实验周期及避免AAV过表达外源TVA 及G 蛋白导致的细胞毒性及神 经网络改变;VSV注射后,一般以12 h为标准时间牺牲动物,而此时间也可控制在2-3天,对跨突触标记结果无太大影响(所有实验样本都需保证采用一致的时间窗口)。
对特定神经网络进行跨单级和跨多级的顺向和逆向标记;
特定区域特异类型神经元的全脑单级或多级输入或输出网络标记;
两个不同区域特异类型神经元被协同调控的单级输入或输出网络模式;
两个区域之间特异类型神经元的直接连接的检测及验证等。
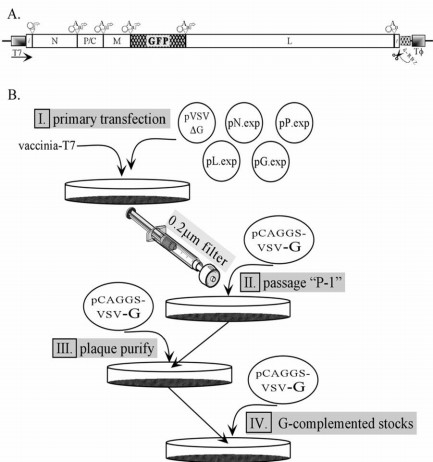
图1:VSV拯救和扩增示意图
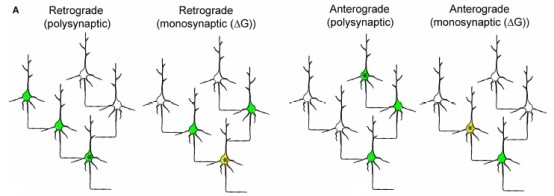
图2:VSV病毒的跨突触追踪策略
(A)编码绿色荧光蛋白等报告基因的rVSV对特定神经网络进行跨单级或跨多级的逆 向或顺向标记。初始感染的细胞用星号表示。基因组包含G 蛋白的VSV可以进行跨多突触传播。传播的方向取决于糖蛋 白的特性。感染的神经细胞用绿色标出。在一些情况下, 将TVA(带红色标签,mCherry)、G同时导入同一个起始神经 元中,再用EnvA包装的携带绿色荧光蛋白GFP基因的EnvA-VSV-GFP可以特定感染这类起始神经元,在起始神经元中组 装成成熟的病毒粒子,感染上一级(逆行)或下一级(顺行)神经元,在上一级或下一级神经元中,只能进行RNA复制 并表达外源蛋白,但不能产生成熟的病毒粒子继续跨突触感染,实现重组的VSV病毒按特定的方向传输。
信息订阅
我们将及时向您推送最新产品资讯

市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK