腺相关病毒载体在肝脏中的研究及应用(一)
一、原理
腺相关病毒(Adeno-associated Virus,AAV)属于细小病毒科(parvoviridae),病毒颗粒无包膜,结构为直径约20nm的正二十面体,是迄今发现的一类结构最简单且无法自主复制的线性单链DNA病毒,对分裂细胞和非分裂细胞均具有感染力。通过人工进化的方法对AAV衣壳蛋白Cap基因进行定向突变改造,可以筛选到具有高转导效率和不同感染特性的AAV载体,极大增加了AAV的应用潜力。
研究中采用的重组腺相关病毒(Recombination adeno-associated virus,rAAV)载体是在非致病的野生型AAV的基础上改造的基因表达载体,具有种类多样、免疫原性低、安全性高、宿主范围广、扩散能力强、体内表达外源基因时间长等特点,已被广泛的应用在动物水平的基因表达、基因操作和基因治疗。
利用AAV载体可实现肝脏细胞广泛表达,还可以结合特异性启动子实现细胞类型的特异性表达,如AAV8型对肝脏有较好的趋向性,特异性启动子TBG可驱动外源基因在肝细胞中特异表达。
rAAV所包含的DNA一般是用外源基因表达元件替换AAV的编码基因,仅保留了病毒复制和包装所需的ITR序列。通过反式补偿Rep基因、Cap基因和辅助病毒功能因子包装产生携带外源DNA的rAAV。rAAV的载体容量是4.7kb,插入外源目的片段大小不超过2.8kb。
表1.AAV靶向不同的器官及组织推荐使用对应血清型,注射方法及剂量
备注:
1. 血清型:同一位置选择不同注射方式,所适用的血清型会存在差异;
2. 注射量:不同文献,病毒供应商不同,滴度不同,剂量会有差异;
3. 以上数据大多查阅文献所得,仅供参考。
二、注射方法
常用的方法有尾静脉注射、腹腔注射及肝门静脉注射。
注意事项:
1)由于心脏血流快,或者由于病毒进入血液系统以后,肝脏的首过效应,使尾静脉注射的病毒不容易富集在心脏(反而在肝脏的富集程度更高),因此相比其他器官,尾静脉注射需要更高的病毒量。
三、应用案例
1)
6-8周龄成年C57BL/6小鼠尾静脉注射1×1011GC的AAV8-TBG-GFP,注射7天后对肝组织切片行GFP免疫荧光染色,结果显示GFP在肝细胞中高效表达。
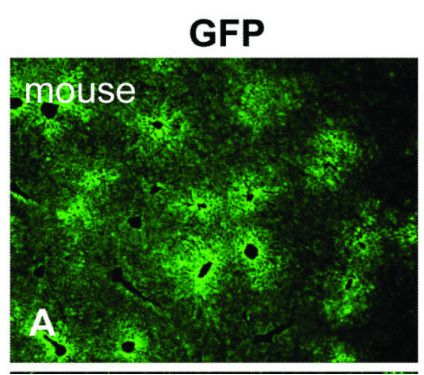
新生C57BL/6小鼠出生后24小时内颞静脉注射2.5×1010GC的AAV8-TBG-EGFP,7天后对肝组织切片行GFP免疫荧光染色,结果显示GFP在肝细胞中高效表达。
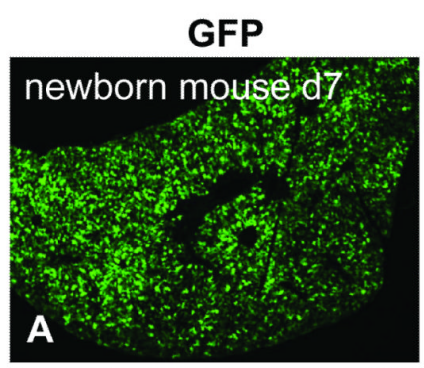
参考文献:
Bell P, Wang L, Gao G, et al. Mol Genet Metab. 2011.
2)基因功能研究
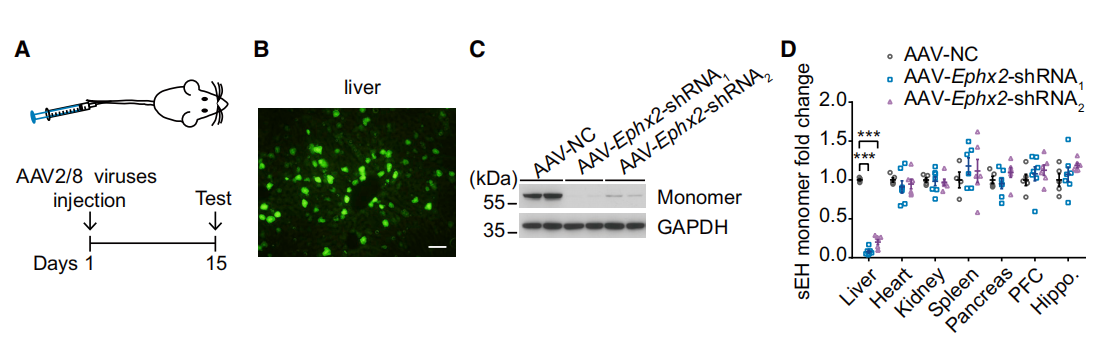
参考文献:
Qin XH, Wu Z, Dong JH, et al.Cell Rep. 2019.
3)
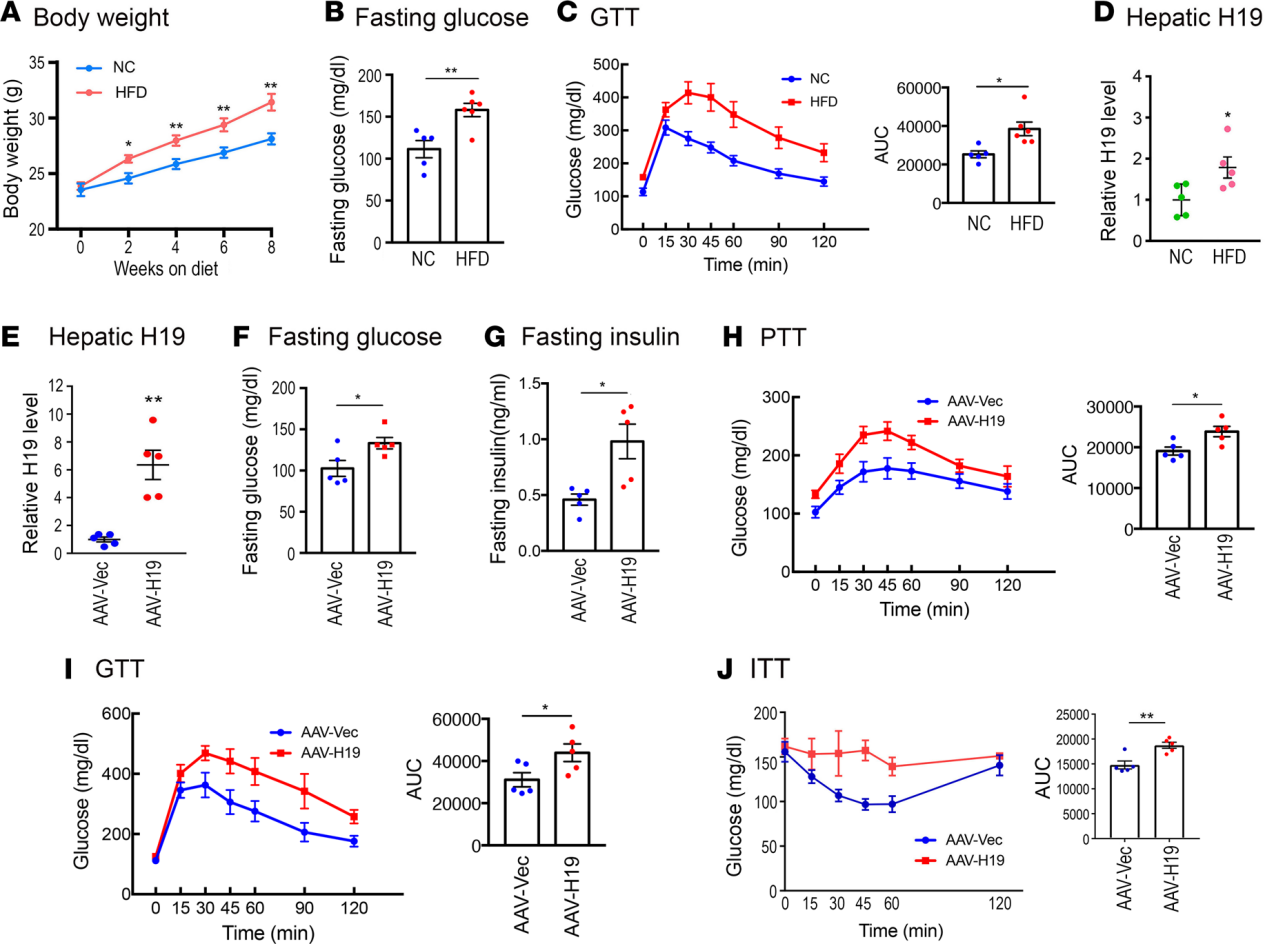
糖尿病小鼠肝脏H19表达慢性增加
相比于正常饲料喂养(NC)小鼠,高脂饲料喂养(HFD)小鼠体重增加更多,空腹血糖升高,并变得葡萄糖不耐受[葡萄糖耐量试验(GTT)],这些小鼠肝脏中H19表达也增加。这些结果表明肝脏H19表达增加与葡萄糖稳态受损之间存在正相关关系。
肝脏特异性H19过表达促进HGP、高血糖和胰岛素抵抗
为了确定肝脏H19表达增加是否与糖代谢受损相关,小鼠尾静脉注射1×1010GC的AAV8-TBG-H19(AAV-H19)实现小鼠全长H19在肝脏特异性表达,H19功能增强小鼠的空腹血糖和胰岛素水平均升高。丙酮酸耐受性试验(PTT)显示丙酮酸注射后血糖水平更高。H19过表达的小鼠也具有葡萄糖不耐受和胰岛素抵抗(胰岛素糖耐量试验ITT)。总的来说,这些结果表明肝脏中H19水平升高增加HGP(肝脏葡萄糖生成)并损害葡萄糖稳态。
参考文献:
Zhang N, Geng T, Wang Z,et al. JCI Insight. 2018.
4)rAAV在肝脏疾病如肝纤维化治疗中的应用
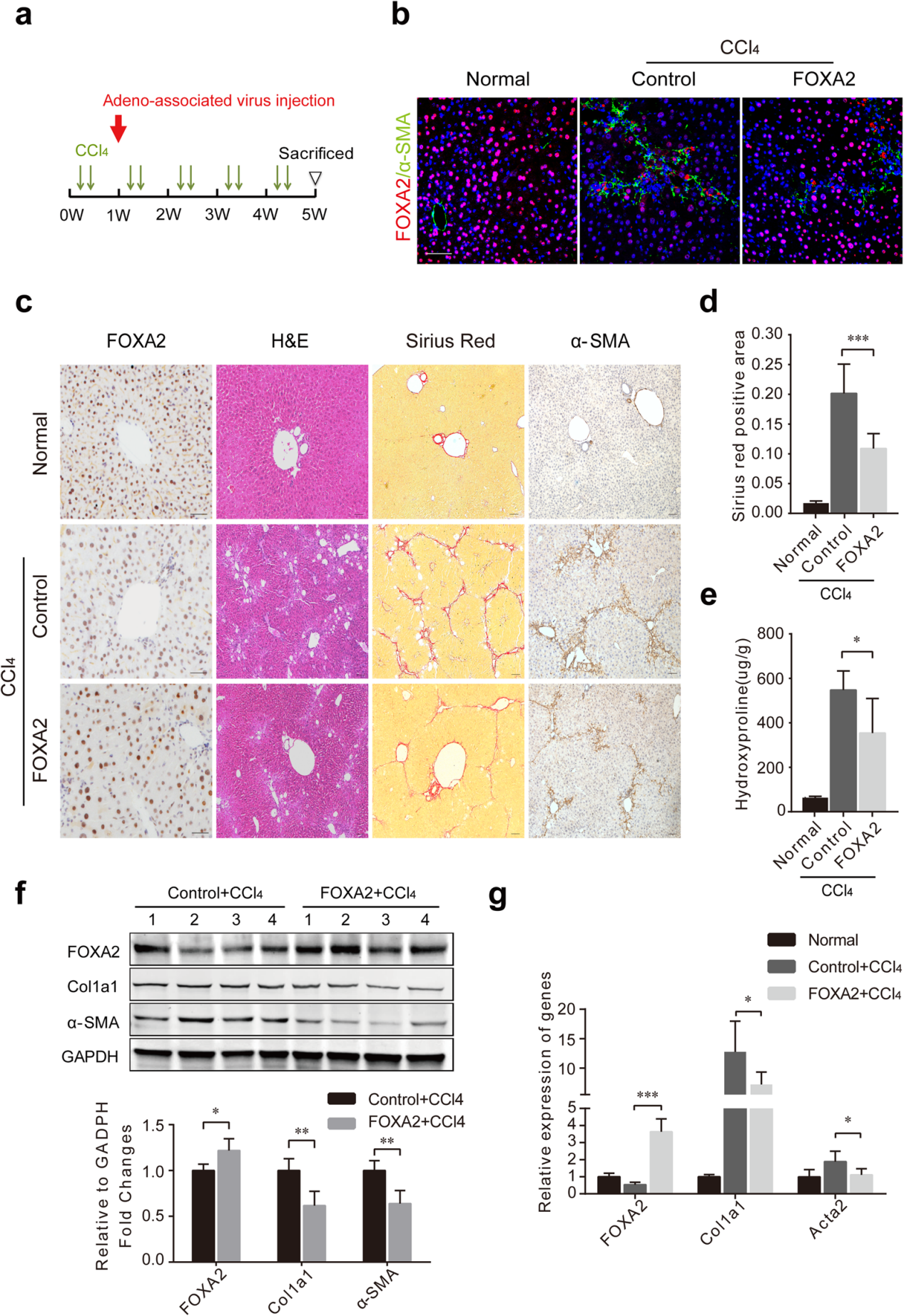
参考文献:
Wang W, Yao LJ, Shen W, et al., Sci Rep. 2017.
信息订阅
我们将及时向您推送最新产品资讯

市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK