2026-04-14 阅读量:198
慢性疼痛累及全球超20%人群,是造成残疾与疾病负担的主要诱因,现有一线治疗效果有限且存在严重不良反应:非甾体抗炎药疗效有限,伴随胃肠道、肾脏及心血管风险;阿片类药物虽可强效镇痛,但易引发耐受、依赖与成瘾,催生全球性阿片危机。中枢神经系统异常适应性神经可塑性(包括中枢敏化与结构重塑)是慢性疼痛持续存在的核心机制,痛觉敏化可从脊髓背角延伸至丘脑、中央杏仁核(CeA)、前扣带回皮层等高级中枢,长时程增强(LTP)与基因表达持续改变维持该敏化状态。脊髓LTP是损伤诱导痛觉过敏与疼痛记忆的细胞基础,阻断脊髓LTP可逆转痛觉过敏,但全身干预缺乏特异性且安全性差。靶向编码疼痛记忆的脊髓上环路更为精准持久,其中CeA作为厌恶学习与伤害性信号整合的关键节点,是调控持续性疼痛的理想靶点,但目前仍缺乏安全、特异的调控手段。
神经调控为靶向异常脑环路提供了无创策略,非节律性光刺激已在临床与动物模型中展现镇痛效应,但其作用通路与机制尚不明确。腺苷信号(尤其是A1、A2A受体)在疼痛调控与LTP诱导阈值调控中发挥关键作用,可全身给药却存在心血管抑制、镇静等不良反应。据此本研究提出假设:40 Hz(伽马γ频段)闪光可作为慢性疼痛无创治疗新手段,通过视网膜-脑环路靶向诱导腺苷释放以调控疼痛通路。
2026年3月4日,温州医科大学附属眼视光医院/瓯江实验室张懿/陈江帆/瞿佳教授团队在Cell Research(IF=25.9,JCR Q1/中科院1区Top)发表题为“40 Hz light flickering alleviates chronic pain via adenosine signaling in the retina-amygdala pathway”研究成果。本研究发现,闪光的镇痛效应具有频率与强度依赖性,其中40 Hz光刺激的镇痛效果最为显著,可有效缓解小鼠炎性疼痛与神经病理性疼痛,并证实视网膜-CeA通路是介导其镇痛作用的关键通路。通过环路特异性操控进一步证实,激活视网膜-CeA通路是40 Hz光刺激发挥镇痛效应的充分且必要条件。机制上,40 Hz闪光可显著升高CeA胞外腺苷水平:局部药理学阻断平衡型核苷转运体(ENT)可抑制腺苷升高并消除镇痛效应,而局部输注腺苷则可模拟光刺激的镇痛作用,且上述效应均依赖A2A受体信号抑制伤害性感受反应。此外,40 Hz光刺激或局部腺苷输注可逆转CeA内的痛觉过敏,该过程与记忆再巩固高度相似,提示CeA是擦除疼痛记忆的关键位点。
综上,本研究证实40 Hz闪光作为无创神经调控手段,可通过特异性视网膜-CeA通路诱导内源性腺苷释放,从多维度调控中枢敏化、缓解慢性疼痛并干预疼痛记忆,为慢性疼痛的靶向治疗提供了全新的无创干预策略与理论依据。
1.40 Hz闪光在慢性疼痛模型中发挥镇痛作用
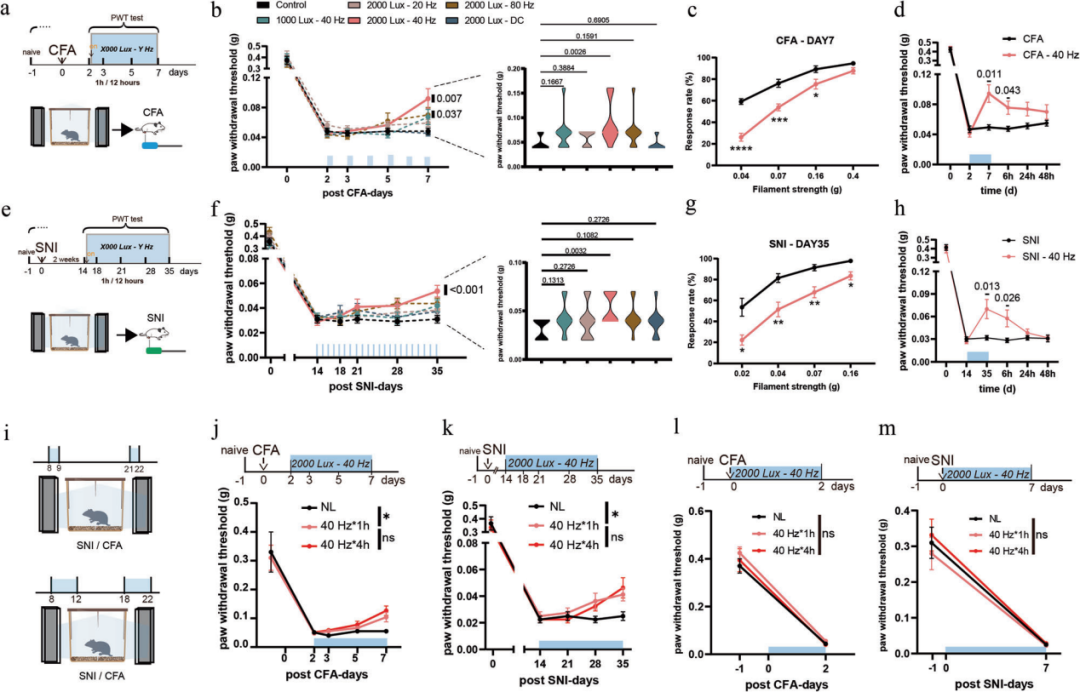
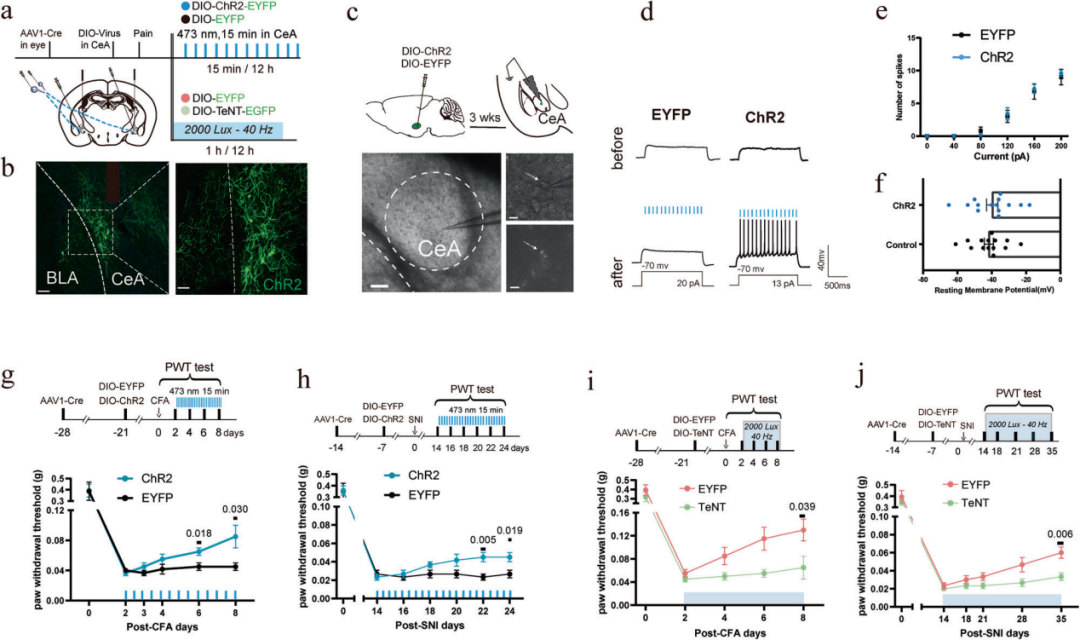
本研究在两种慢性疼痛模型中探究闪光刺激的抗伤害效应:完全弗氏佐剂(CFA)诱导的炎性疼痛模型,以及保留性神经损伤(SNI)诱导的神经病理性疼痛模型。单侧足底注射CFA可诱发持续性炎症与机械性痛觉过敏;SNI模型可模拟人类神经病理性疼痛,稳定诱导出长期持续的触诱发痛与痛觉过敏。
本研究首先评估20 Hz、40 Hz、80 Hz闪光及恒定光(DC)的镇痛效果,所有刺激均采用LED光源,强度为2000勒克斯(lux),干预方案为每日2次、每次1小时,早晚间隔12小时,每日总刺激时长2小时。结果显示,在CFA模型中,2000 lux-40 Hz闪光连续刺激6天后,可显著减轻机械性痛觉过敏,效果优于造模后基线(第2天)及未处理对照组。依据缩足频率,该光刺激可显著降低小鼠对0.07~0.16 g非伤害性机械刺激的机械性痛觉超敏,且镇痛效应在刺激结束后可持续6小时以上。20 Hz闪光及DC光均未产生显著镇痛作用;80 Hz闪光虽可使CFA小鼠缩足阈值(PWT)较自身基线显著升高,但与未处理对照组相比无统计学差异,在SNI模型中也仅呈现轻微、无统计学意义的改善。将光强降至1000 lux的40 Hz闪光,在两种模型中均仅产生微弱、不显著的镇痛效果。
在SNI小鼠中,采用相同的每日2小时干预方案,需连续刺激21天方可达到显著镇痛效果,镇痛效应同样在刺激停止后维持6小时以上,随后明显减弱。2000 lux-40 Hz闪光可显著缓解SNI小鼠的机械性痛觉过敏:SNI造模第35天,小鼠PWT较基线水平(SNI造模第14天)显著升高;组间比较显示,光刺激组PWT显著高于未处理对照组。综合以上结果,2000 lux-40 Hz闪光可产生最强、最稳定的镇痛效应。
为明确延长每日刺激时长能否增强镇痛效果,本研究将刺激时长增加至早晚各4小时(每日8小时),但在两种模型中,其镇痛效果与每日2小时方案相近。
图1.40 Hz闪光可缓解慢性疼痛模型中的机械性痛觉过敏
2.CeA中响应40 Hz闪光的镇痛神经元群
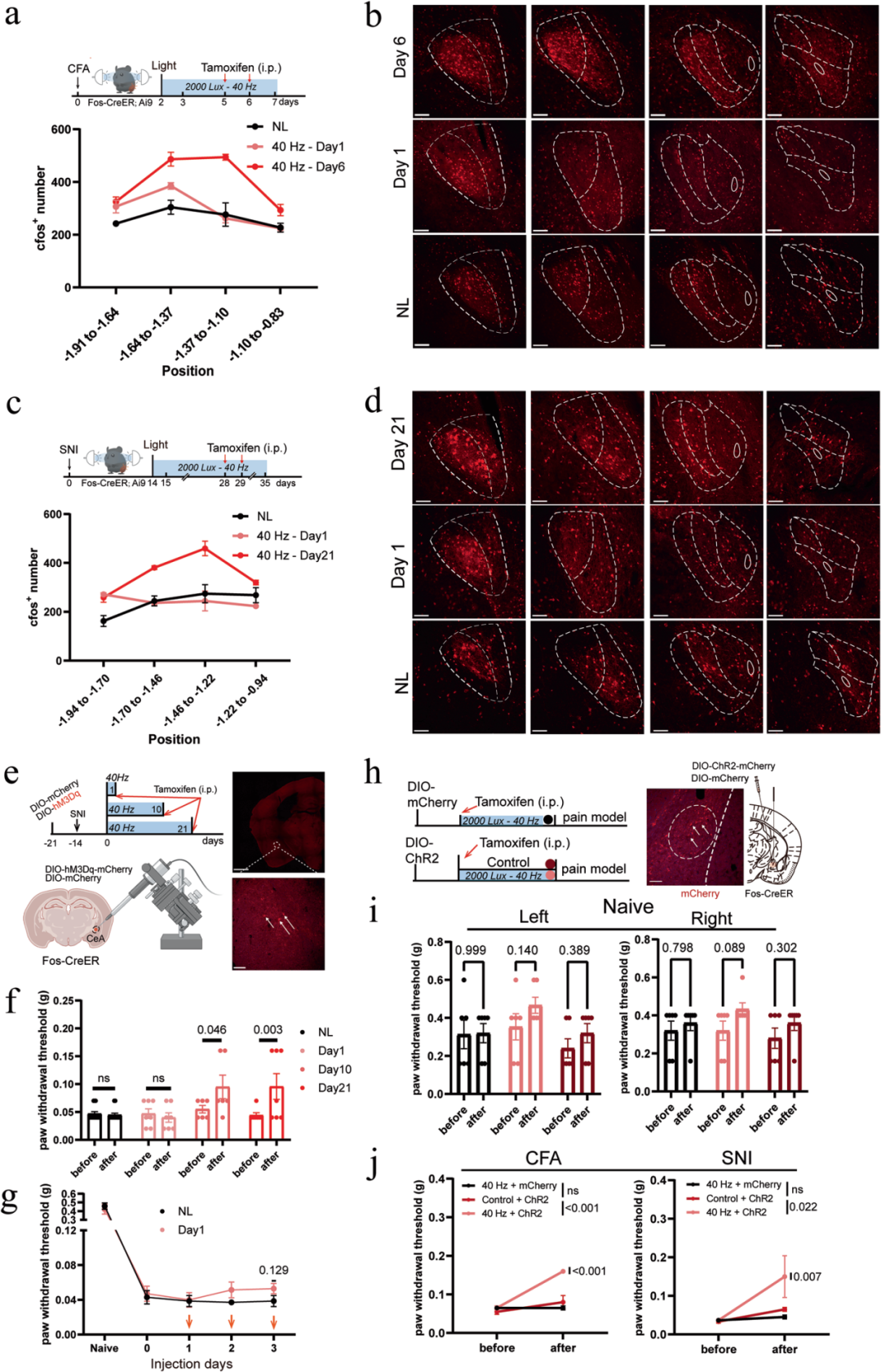
为鉴定被40 Hz闪光激活的神经元,本研究借助即刻早期基因Fos的刺激-转录偶联机制,采用Fos-CreERT2/TRAP2;Ai9小鼠,实现对特定时间窗内激活神经元的遗传标记。小鼠首先构建CFA炎性疼痛或SNI神经病理性疼痛模型,在40 Hz光刺激结束后立即给予他莫昔芬(tamoxifen)以标记被激活的神经元群,1周后处死小鼠并进行成像分析。定量结果显示,经40 Hz光连续刺激6天(CFA模型)或21天(SNI模型)后,CeA中被TRAP标记的神经元数量较单纯疼痛对照组显著增多,提示CeA脑区出现显著神经元激活。与之相反,两种模型中仅给予1天40 Hz光刺激,均未显著增加CeA内TRAP标记神经元数量,其数量与未处理对照组无显著差异。
为明确该TRAP标记神经元集群的功能作用,本研究在SNI小鼠中对其进行化学遗传学激活。向TRAP2小鼠CeA脑区注射AAV-Syn-DIO-hM3Dq或对照病毒AAV-Syn-DIO-mCherry,1周后对小鼠进行SNI造模;自SNI术后第14天起,连续给予21天40 Hz光刺激,随后注射他莫昔芬。2周后,在无40 Hz光刺激的条件下,使用去氯氯氮平(DCZ,1 mg/kg)单次化学遗传学激活CeA中TRAP标记的神经元,可显著减轻SNI小鼠的机械性痛觉过敏。上述结果表明,即便部分TRAP标记细胞可能对疼痛产生响应,40 Hz光激活的CeA神经元仍以镇痛功能为主导。
接下来研究人员探究该神经元集群在21天刺激周期内是否保持稳定或随时间发生改变。为检测其时间动态变化,在刺激早期(刺激第1天或第10天)对CeA神经元进行TRAP标记,随后开展化学遗传学激活实验。结果显示,单次DCZ注射激活刺激第10天标记的CeA神经元,可在SNI小鼠中产生显著镇痛效应;而激活刺激第1天标记的神经元则无镇痛作用。连续3天反复激活第1天标记的神经元,仅呈现出延迟性镇痛趋势,但该效应未达到统计学差异。上述结果提示,需经多次光刺激才能有效捕获CeA中响应40 Hz光的镇痛神经元集群。
最后,本研究探究naïve小鼠中被TRAP标记的40 Hz响应性CeA神经元是否足以产生镇痛效应。向TRAP2小鼠CeA脑区注射AAV-Syn-DIO-mCherry或AAV-Syn-DIO-ChR2,3周后将小鼠分为3组:①mCherry注射组+2周40 Hz闪光(对照组);②ChR2注射组+标准环境光(对照组);③ChR2注射组+2周40 Hz闪光(实验组),并在光刺激结束后立即给予他莫昔芬。在正常生理状态下,光遗传学激活TRAP标记的CeA神经元仅使小鼠PWT出现轻微、无统计学意义的升高;而经SNI或CFA诱导慢性疼痛后,通过40 Hz光介导光遗传学激活该神经元集群,可显著降低机械性痛觉超敏。
综上,40 Hz闪光可激活CeA中一类独特的镇痛神经元集群。该集群在反复光刺激过程中逐步形成,并足以在多种疼痛模型中产生强效镇痛作用,为40 Hz闪光用于慢性疼痛缓解的治疗潜力提供了核心实验依据。
图2.40 Hz闪光可激活CeA中与镇痛相关的神经元
3.视网膜-CeA环路是40 Hz闪光诱导镇痛的必需通路
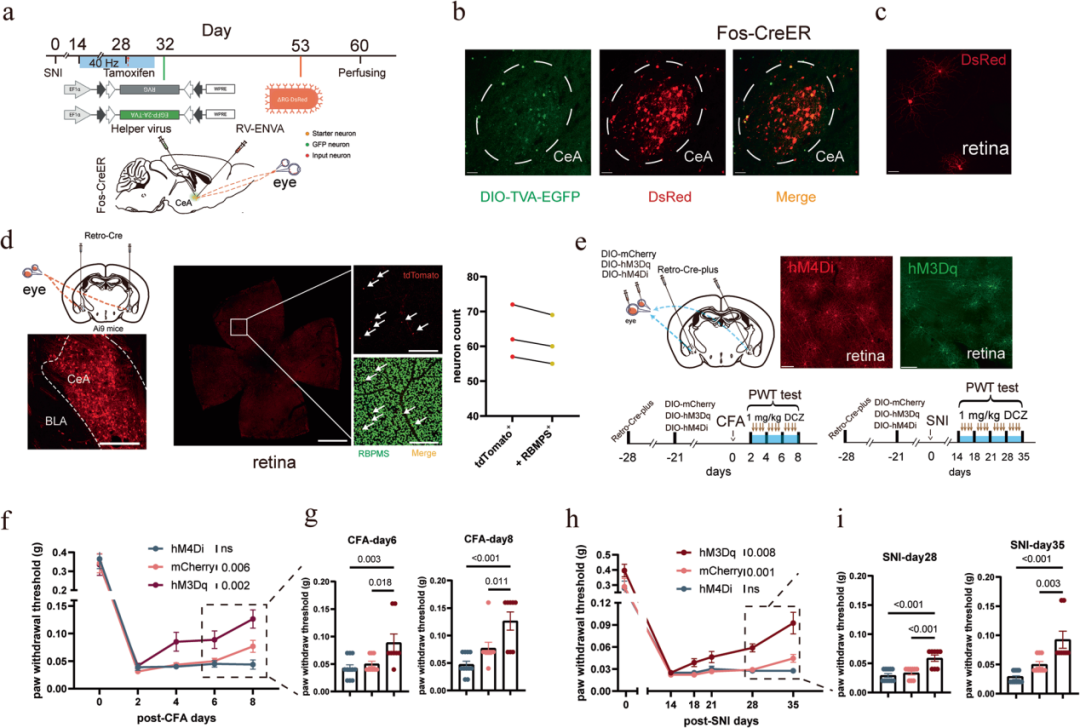
为阐明40 Hz闪光诱导抗伤害效应的神经环路机制,本研究采用狂犬病毒(RV)单突触示踪技术,定位被40 Hz光激活的CeA神经元的突触前输入。在光刺激的SNI小鼠中,先向TRAP标记的CeA神经元注射表达RV糖蛋白及辅助蛋白的AAV;21天后,将EnvA假型SAD-ΔG-DsRed RV注入CeA,选择性感染表达辅助蛋白的TRAP阳性CeA神经元。这些RV-DsRed⁺/TVA-EGFP⁺双标细胞为起始细胞,可产生具有感染性的ΔG-RV-DsRed,并逆行传递至单突触连接的上游神经元。令人意外且惊喜的是,每个视网膜中约有十几个视网膜神经节细胞(RGCs)被标记。
为独立验证视网膜→CeA直接投射的存在,本研究向Ai9小鼠CeA注射AAV2/Retro Plus-hSyn-Cre进行逆行示踪,结果显示大量RGCs被标记,单侧视网膜约有60个荧光标记细胞。免疫组化证实,超过95%的标记细胞为RBPMS阳性RGCs,明确证实存在视网膜至CeA的直接神经通路。
为明确该环路的功能意义,采用化学遗传学手段操控投射至CeA的RGCs:向双侧CeA注射AAV2/Retro Plus-hSyn-Cre,再向玻璃体腔注射Cre依赖性AAV(hM3Dq激活型、hM4Di抑制型或mCherry对照),并通过EGFP/mCherry荧光确认其在视网膜中的表达。仅通过腹腔注射DCZ(1 mg/kg,每日2次),对投射至CeA的RGCs进行长达7天的慢性化学遗传学激活,与对照组相比,CFA小鼠的PWT有升高趋势,但该效应未达到统计学显著性。然而,当与40 Hz闪光联合使用时,与单独40 Hz闪光刺激相比,慢性化学遗传学激活可在CFA和SNI两种模型中显著增强镇痛效果。更重要的是,在两种疼痛模型中,慢性化学遗传学激活联合40 Hz闪光刺激,可显著缩短光诱导镇痛效应的起效时间。相反,对投射至CeA的RGCs进行慢性化学遗传学抑制(DCZ,1 mg/kg,每日2次,光刺激前给药),可完全消除40 Hz光刺激的镇痛作用。
图3.视网膜-CeA通路介导40 Hz闪光诱发的镇痛效应
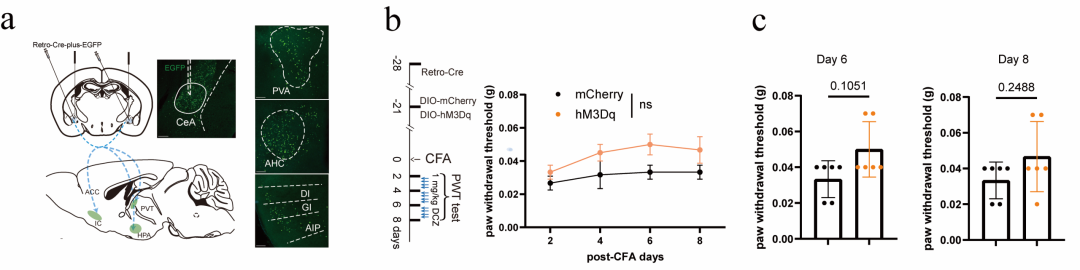
图4.对投射至CeA的RGCs进行化学遗传学激活,仅使CFA模型小鼠的PWT出现小幅升高
为进一步验证该通路,本研究采用顺行示踪策略直接激活接收视网膜输入的CeA神经元:向双侧玻璃体腔注射可顺行扩散的AAV1-Cre,1周后向CeA注射AAV-hSyn-DIO-ChR2或对照病毒AAV-hSyn-DIO-EYFP。急性脑片电生理记录显示,蓝光刺激可在表达ChR2的接收视网膜输入的CeA神经元上稳定诱发动作电位串,且ChR2/EYFP表达不改变所记录CeA神经元的基础电生理特性。病毒注射4周后构建CFA/SNI疼痛模型,给予每日2次、每次15分钟的光遗传学刺激:连续刺激5天(CFA模型)或9天(SNI模型)即可显著缓解机械性痛觉过敏,证实该通路足以介导镇痛效应。
随后,通过在接收视网膜输入的CeA神经元中表达破伤风神经毒素(TeNT)阻断其突触输出,可完全消除40 Hz闪光的镇痛作用,证明该环路完整的突触传递是介导抗伤害效应的必需条件。
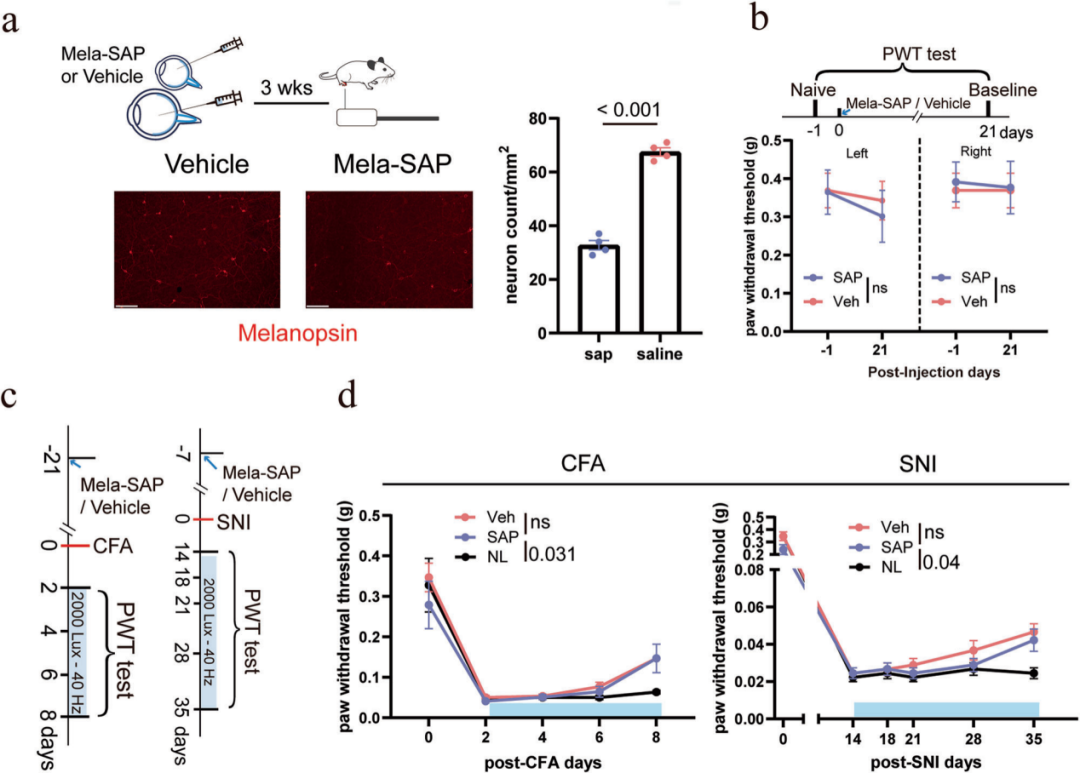
最后探究自感光视网膜神经节细胞(ipRGCs)的作用(该细胞已知介导非成像视觉反应):向双侧玻璃体腔注射黑视蛋白偶联皂草素(melanopsin-SAP)特异性损毁ipRGCs,损毁效率约70%。处理后小鼠基线PWT无明显改变;且即便损毁ipRGCs,40 Hz闪光在CFA及SNI模型中的镇痛效应仍保持完整,提示ipRGCs并非40 Hz闪光诱导镇痛所必需。
综上,本研究发现一条全新的视网膜-CeA视觉通路,该通路是40 Hz闪光诱导镇痛的充分且必需条件,其作用不依赖ipRGCs,而是通过常规RGCs介导镇痛效应。
图5.接收视网膜输入的CeA神经元介导40 Hz闪光诱发的镇痛作用
图6.表达黑视蛋白的RGCs(ipRGCs)并非40 Hz闪光诱发镇痛所必需
4. CeA内腺苷信号介导40 Hz闪光诱导的镇痛效应
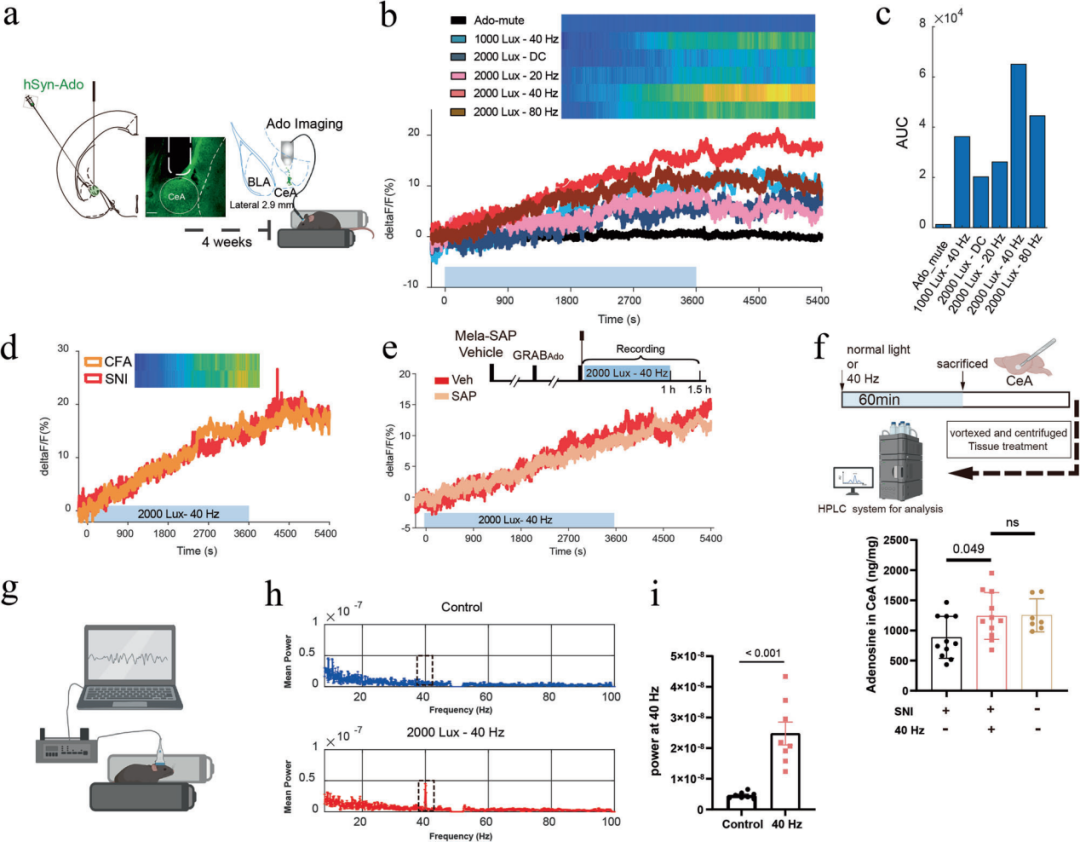
既往研究提示,腺苷参与40 Hz闪光诱导的脑功能改变。为探究腺苷是否参与本研究中观察到的镇痛效应,本研究采用高灵敏度、高特异性腺苷探针(GRABAdo),监测光刺激期间CeA内胞外腺苷的动态变化。向CeA注射表达GRABAdo或其非结合突变体(GRABAdo-mut)的腺相关病毒(AAV),通过光纤光度法检测可反映胞外腺苷水平的荧光信号。给予2000 lux-40 Hz闪光刺激后,CeA内胞外腺苷浓度出现显著且持续的升高,荧光强度(ΔF/F)最高可达基线水平的20%,并在刺激结束后维持至少30分钟。本研究进一步探究不同频率和强度的光对CeA内腺苷生成的影响:1000 lux-40 Hz、2000 lux-80 Hz闪光可中度升高CeA胞外腺苷水平,而20 Hz闪光与2000 lux DC光仅引起轻微变化,提示腺苷释放依赖于光的频率和强度。在CFA炎性疼痛和SNI神经病理性疼痛模型中,2000 lux-40 Hz闪光均可显著升高CeA胞外腺苷水平,且升高幅度与naïve小鼠中观察到的水平相当;重要的是,melanopsin-SAP处理不影响CeA胞外腺苷的升高效应。
为验证上述结果,本研究采用高效液相色谱(HPLC)检测40 Hz闪光诱导的CeA内源性腺苷水平升高。SNI小鼠CeA内总腺苷水平较正常小鼠显著降低,而1小时40 Hz光刺激可使SNI小鼠CeA总腺苷水平明显升高,恢复至与正常小鼠相当的水平。此外,局部场电位(LFP)电生理记录显示,2000 lux-40 Hz闪光可诱导CeA γ波段振荡同步化,实现节律性视觉输入与局部神经活动的直接偶联。
图7.40 Hz闪光以光频率和强度依赖性方式升高CeA的细胞外腺苷水平,且该效应与LFP γ波功率相关
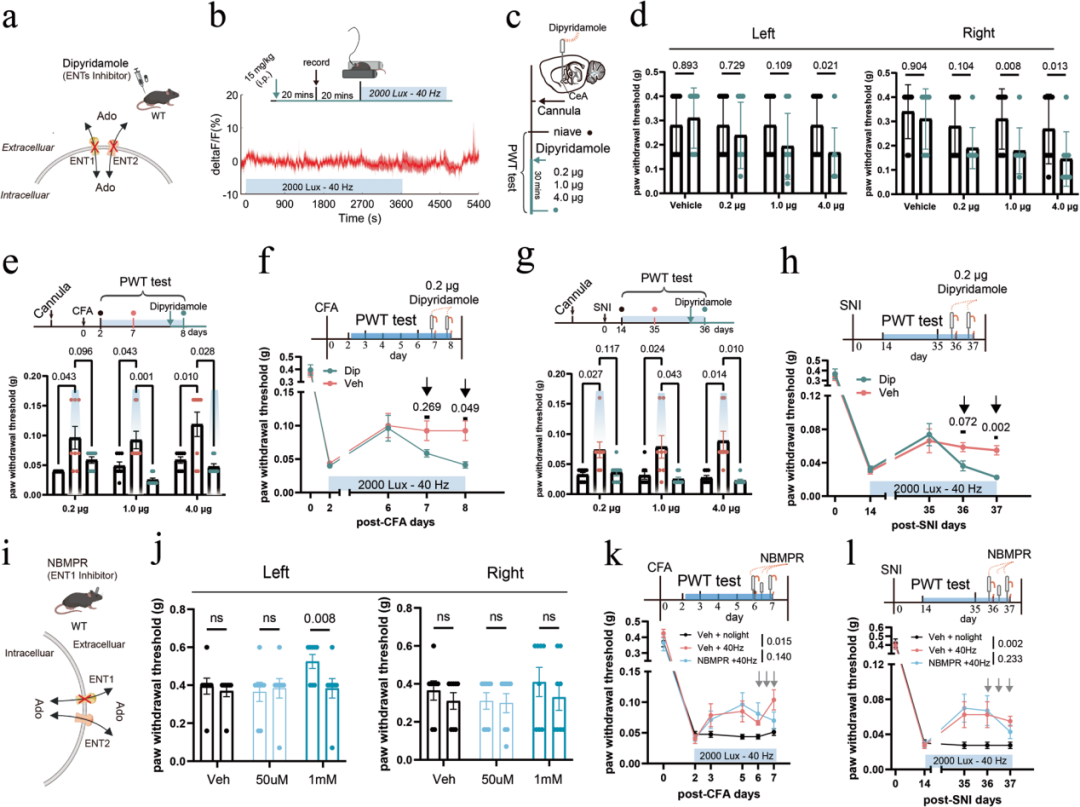
胞外腺苷主要来自ATP代谢产生的胞内腺苷,经平衡核苷转运体(ENT)介导的跨膜外排作用释放到胞外。本研究进一步探究依赖ENT1/2的跨膜转运在40 Hz光诱导CeA腺苷升高中的作用:光刺激前40分钟腹腔注射ENT1/2抑制剂双嘧达莫(15 mg/kg),可完全阻断40 Hz光刺激诱导的CeA胞外腺苷升高。本研究还检测了向右侧CeA局部给予双嘧达莫对小鼠疼痛行为的影响。结果显示,不同剂量的双嘧达莫均对正常小鼠的PWT产生负面影响;其中高剂量(1.0 μg、4.0 μg)双嘧达莫可有效消除40 Hz闪光在CFA和SNI模型中的镇痛效应,即使是低剂量(0.2 μg)双嘧达莫,连续给药超过2天也可显著拮抗40 Hz闪光的镇痛作用。除抑制ENT1/2外,双嘧达莫还具有多种药理靶点。因此,本研究采用ENT1的金标准拮抗剂——高特异性抑制剂NBMPR,探究ENT1的作用。既往研究表明,向CeA微注射0.5 μL 50 μM NBMPR可减轻焦虑样行为,提示ENT1在CeA中具有功能作用。本研究向正常小鼠右侧CeA给予两种剂量的NBMPR(2 μL 50 μM或2 μL 1 mM)进行评估:其中高剂量(2 μL 1 mM)会改变基线行为,而低剂量(2 μL 50 μM)不影响正常小鼠的机械敏感性,因此被选用于后续实验。
在CFA和SNI模型中,每次40 Hz光刺激前15分钟向CeA微注射NBMPR,连续3次给药后,40 Hz闪光的镇痛效应呈现部分减弱趋势,但在两种模型中均未达到统计学差异。考虑到40 Hz闪光可显著增加胞内腺苷生成,在此条件下ENTs预计主要以向外转运模式发挥作用。本研究结果得到作者既往在初级视觉皮层(V1)利用ENT敲除小鼠的研究支持:ENT2敲除几乎完全阻断40 Hz光诱导的胞外腺苷升高,而ENT1敲除仅部分减弱该反应。ENT2的优先参与可能与其更高的转运能力以及在神经元和星形胶质细胞中约4倍的高表达有关,这使其能够在闪光刺激期间更高效地升高胞外腺苷水平。综上,这些结果提示ENT1和ENT2均可能参与40 Hz光诱导的CeA胞外腺苷升高,其中ENT2可能发挥更显著的作用。
图8.双嘧达莫可拮抗40 Hz闪光诱导的镇痛效应
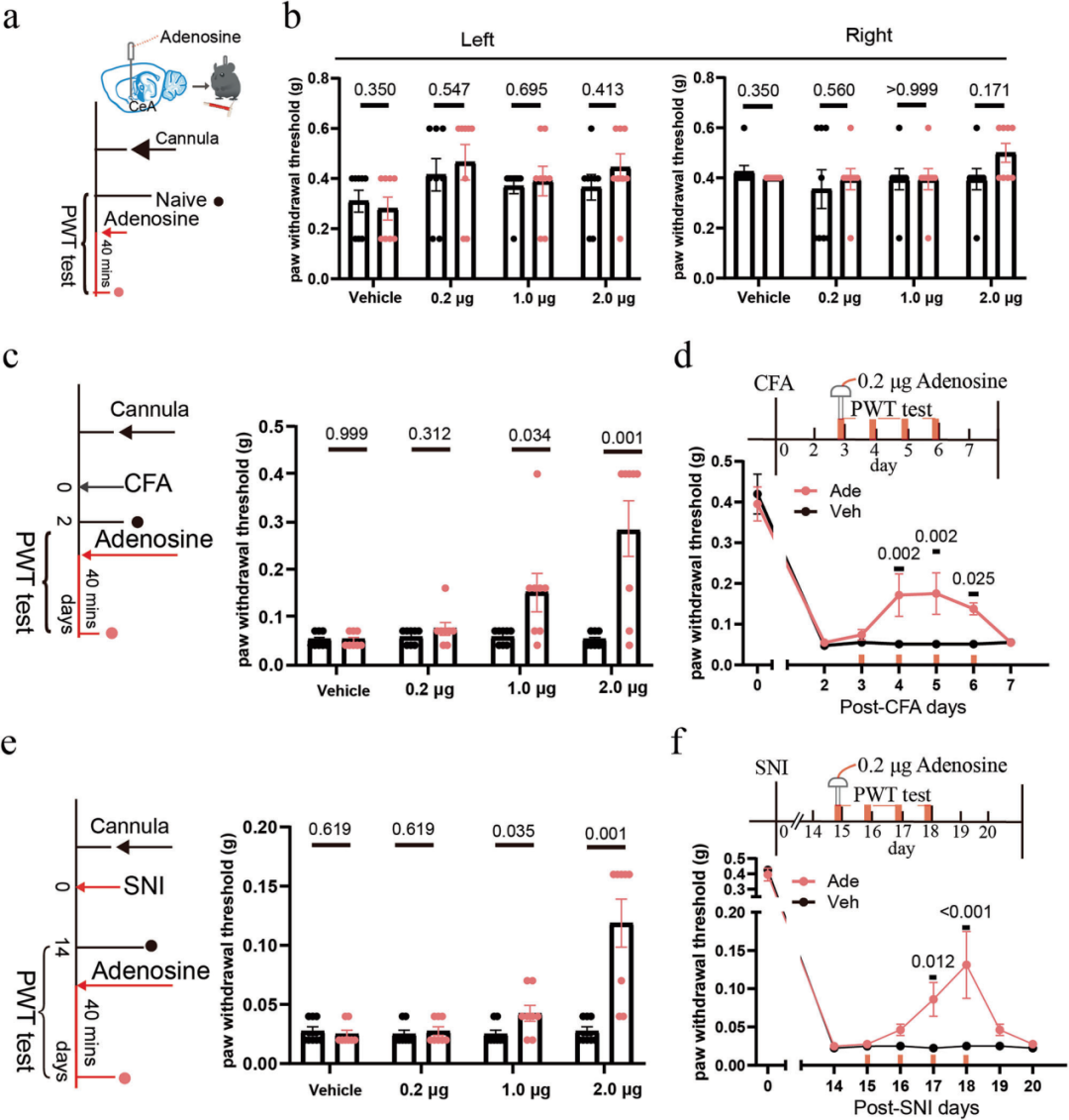
为探究直接给予腺苷是否可模拟40 Hz光诱导的镇痛效应,本研究向右侧CeA输注不同剂量的腺苷(0.2 μg、1.0 μg和2.0 μg)。在正常小鼠中,所有剂量的腺苷均未显著影响PWT;随后,本研究通过套管向CFA和SNI小鼠右侧CeA给予相同剂量的腺苷,结果显示,高剂量腺苷(1.0 μg、2.0 μg)可快速缓解两种模型中的机械性痛觉过敏;低剂量腺苷(0.2 μg)无法立即降低机械性痛觉超敏,但连续给药超过2天后,0.2 μg腺苷也可显著升高CFA和SNI小鼠的PWT。HPLC检测显示,正常小鼠与SNI小鼠的CeA总腺苷含量差值为0.13 μg,40 Hz光刺激可使SNI小鼠CeA腺苷水平升高0.11 μg,该剂量与本研究体内药理学实验中使用的低剂量腺苷(0.2 μg)接近。与上述检测结果一致,药理学实验表明,升高CeA胞外腺苷足以产生抗伤害效应,且每日反复给药可使该效应累积增强。
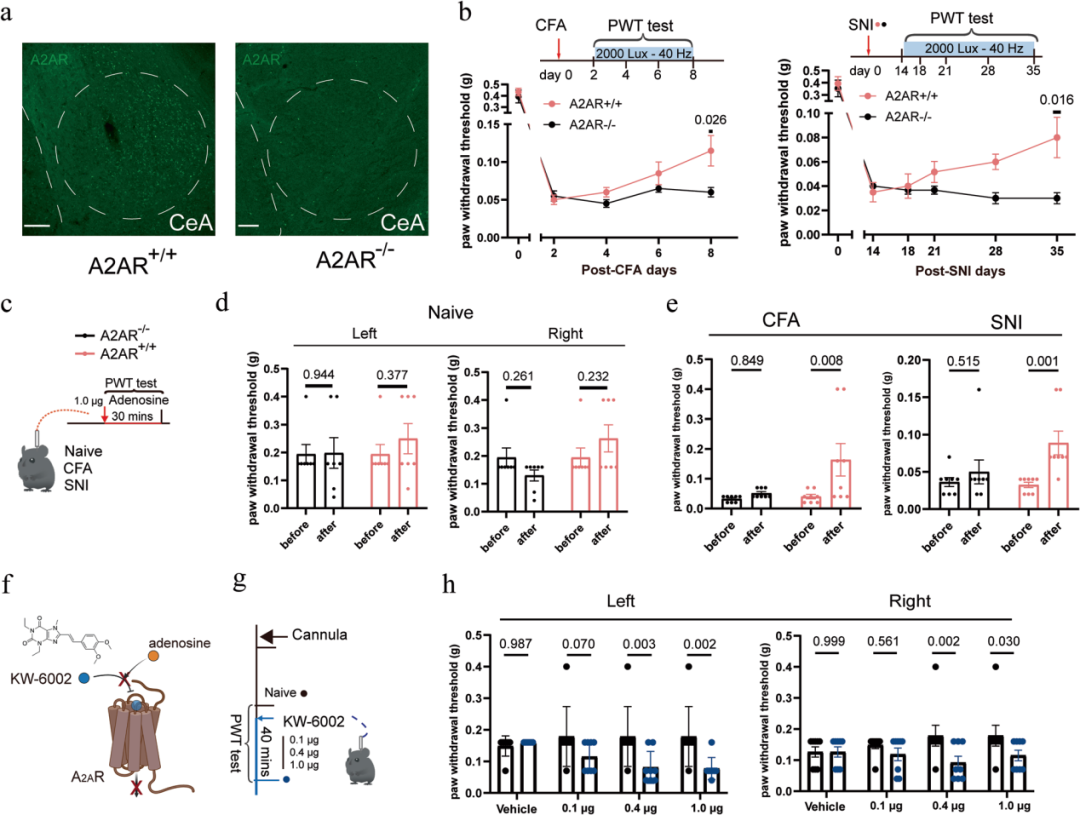
免疫染色结果显示,野生型(WT)小鼠CeA中表达腺苷A2A受体(A2AR),而A2AR敲除(A2AR-/-)小鼠CeA中无A2AR表达。这促使研究人员探究A2AR在40 Hz闪光诱导镇痛中的作用。与同窝对照小鼠不同,A2AR-/-小鼠在两种疼痛模型中均无法响应40 Hz闪光产生镇痛效应,证实该受体亚型是镇痛效应所必需的。为进一步明确CeA是腺苷作用的位点,本研究向A2AR-/-小鼠及其同窝WT对照小鼠的CeA局部输注腺苷,结果显示,腺苷在突变小鼠中无法发挥镇痛效应,证实该镇痛效应由CeA局部的A2AR特异性介导。此外,向右侧CeA直接注射A2AR特异性拮抗剂KW6002(剂量为0.4 μg或1.0 μg),可显著降低正常小鼠的PWT,提示该脑区的A2AR对机械敏感性调控至关重要。
综上,这些结果提示,40 Hz闪光通过促进CeA胞外腺苷蓄积,并激活CeA神经元中的A2AR,从而发挥镇痛效应。
图9.向CeA内注射腺苷可缓解疼痛模型中的机械性痛觉超敏
图10.A2AR介导40 Hz闪光及腺苷的镇痛作用
5.CeA脑啡肽能神经元是40 Hz闪光诱导镇痛所必需的
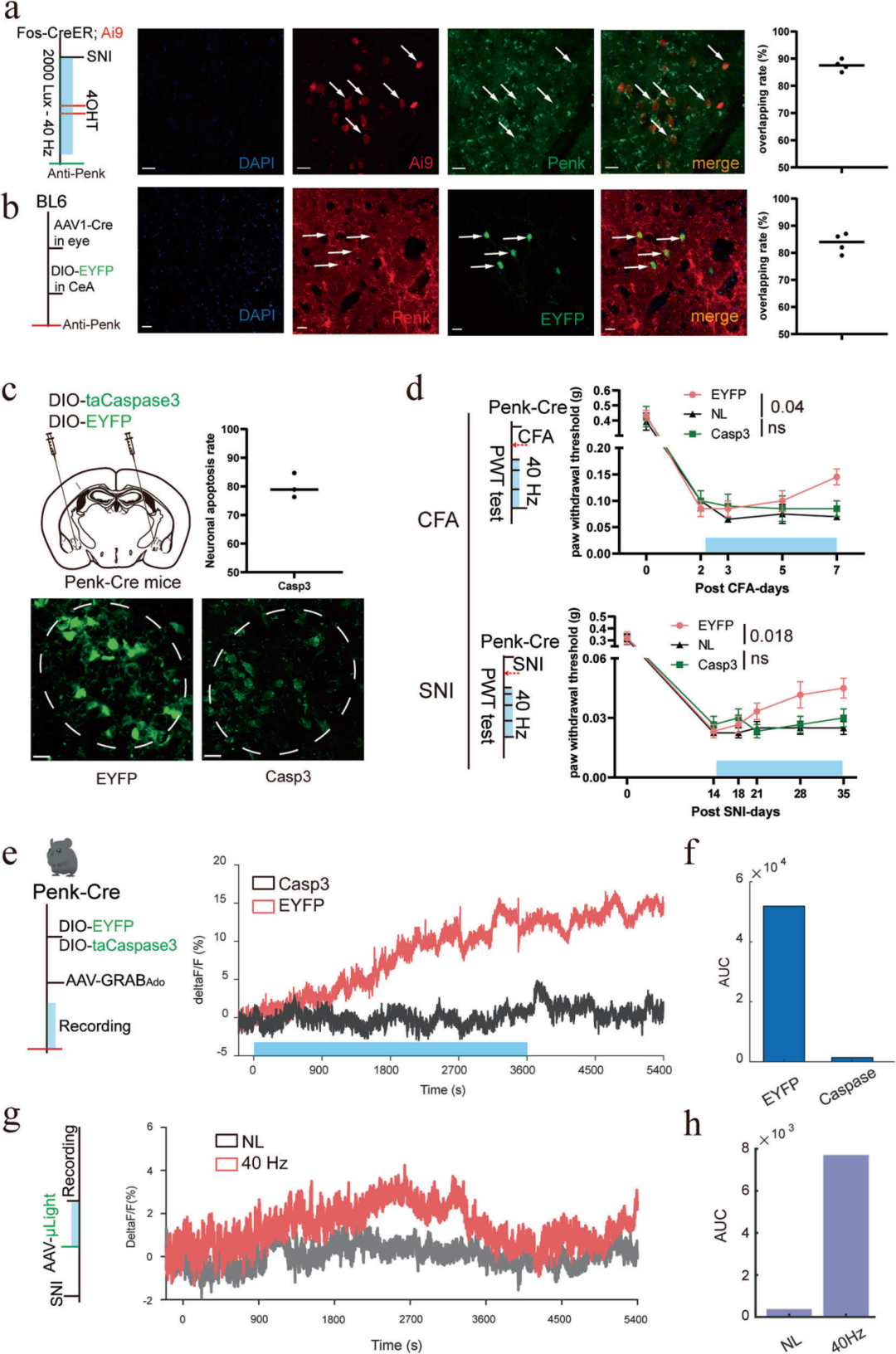
鉴于CeA在40 Hz闪光诱导镇痛中的核心作用,本研究进一步鉴定被光刺激激活的特异性神经元亚型。CeA是神经化学组成多样的脑区,存在多个参与感觉与情感加工的神经元亚群。为明确接收RGCs直接输入的CeA细胞类型,本研究向视网膜注射顺行转运病毒AAV1-Cre,向CeA注射Cre依赖性报告病毒AAV2/9-hSyn-DIO-mCherry。免疫组化结果显示,约80%的mCherry标记CeA神经元呈前脑啡肽原(Penk)免疫阳性,表明该视网膜-CeA通路的突触后神经元主要为脑啡肽能神经元。这类神经元可释放脑啡肽(内源性阿片肽),后者结合阿片受体发挥镇痛作用。利用Fos-CreERT2/TRAP2;Ai9小鼠进一步证实,经40 Hz光刺激被TRAP标记的CeA神经元中,超过80%共表达Penk,属于脑啡肽能神经元。
为探究该类神经元的功能,本研究在Penk-Cre小鼠CeA脑区注射Cre依赖性促凋亡病毒AAV-taCaspase3,以特异性损毁Penk⁺神经元;组织学分析证实损毁效率超过80%。重要的是,损毁该类神经元后,40 Hz光刺激在CFA和SNI模型中均无法产生镇痛效应,且无法诱导CeA胞外腺苷水平升高,提示该类神经元不仅是镇痛行为所必需,同时也是腺苷释放的必要前提。因此,CeA内表达Penk的神经元是连接40 Hz光刺激、视网膜输入、腺苷信号与慢性疼痛状态下行为学结局的关键细胞底物。
本研究进一步使用基因编码阿片肽探针δlight检测内源性脑啡肽释放,结果显示,40 Hz闪光可显著升高CeA内脑啡肽水平。同时检测了CeA内腺苷A1受体(A1R)的表达。A1R是经典的Gi/o偶联抑制型受体,参与疼痛抑制,被认为是极具潜力的非阿片类镇痛靶点;但免疫染色结果显示,A1R在基底外侧杏仁核(BLA)中高表达,而在CeA中仅呈弱表达。与之相对,本实验中发挥关键作用的A2AR为Gs偶联兴奋型受体,与通路功能更为契合。鉴于40 Hz闪光可激活下游Penk⁺CeA神经元并产生镇痛效应,上述结果提示,该抗伤害效应更可能由兴奋型A2AR而非抑制型A1R介导。
图11.CeA中的前脑啡肽原阳性(Penk+)神经元介导40 Hz闪光诱导的镇痛效应及细胞外腺苷水平升高
6.40 Hz闪光通过CeA擦除疼痛记忆
中枢敏化是慢性疼痛的核心细胞机制。脊髓背角的中枢敏化与海马的神经可塑性类似,可增强突触传递效率,使神经系统对伤害性刺激产生持续性的异常适应性改变。然而,疼痛状态下CeA中是否存在类似记忆形成的过程仍不明确。为此,本研究探究在痛觉敏化再次激活后,靶向干预CeA能否使机械性痛觉过敏变得不稳定且可逆转。
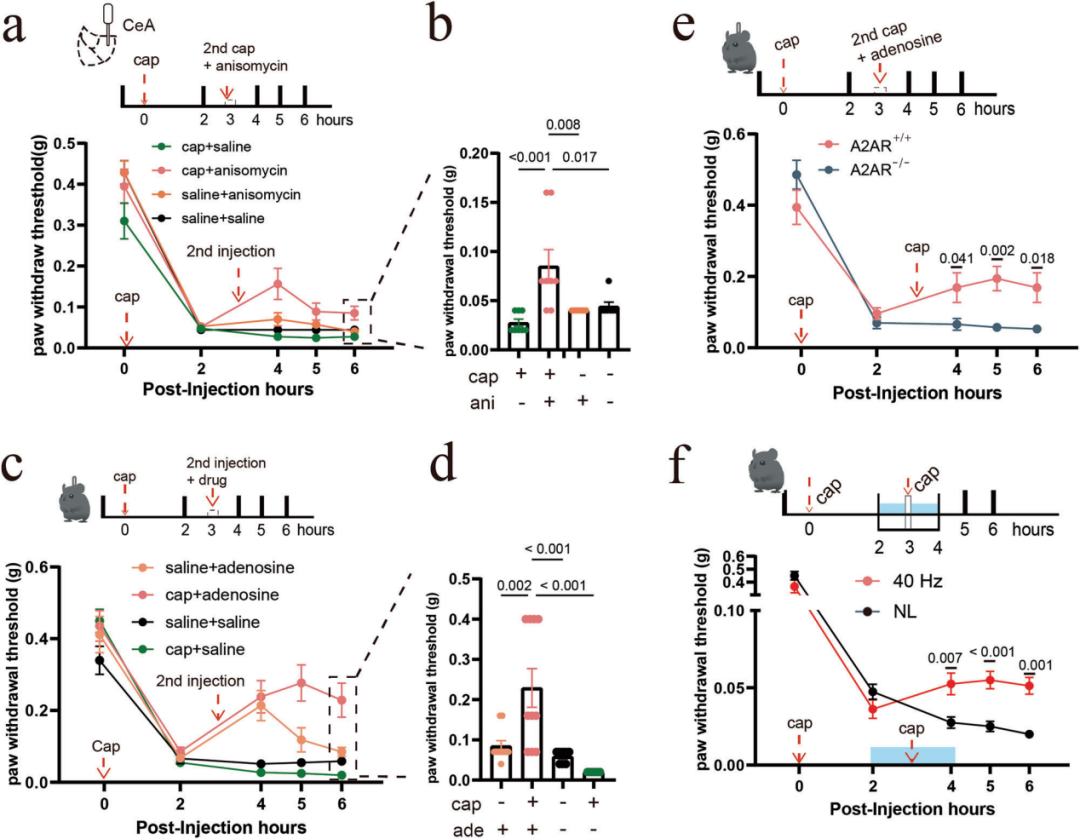
本研究采用成熟的疼痛记忆研究范式,通过向小鼠足底注射辣椒素诱导机械性痛觉过敏,该疼痛状态可持续超过6小时。首次辣椒素注射3小时后,给予第二次相同剂量的辣椒素注射以重新激活敏化的疼痛通路,同时向右侧CeA注射蛋白合成抑制剂茴香霉素或溶媒对照(生理盐水)。第二次辣椒素注射联合右侧CeA给予生理盐水,对机械性痛觉超敏几乎无影响;而联合茴香霉素注射则可显著且持久地减轻机械性痛觉过敏。上述结果提示,CeA内存在疼痛记忆再巩固样过程,抑制蛋白合成可破坏该过程。
随后,本研究探究40 Hz闪光或腺苷信号能否像茴香霉素一样,干扰CeA中的疼痛记忆。如图12c所示,在辣椒素诱导的机械性痛觉过敏模型中,第二次注射溶媒对照联合右侧CeA输注1.0 μg腺苷,可短暂逆转痛觉过敏,但效应迅速消退;与之不同,第二次辣椒素注射联合右侧CeA输注1.0 μg腺苷,则可显著且持久地逆转机械性痛觉过敏,该效应在A2AR-/-小鼠中消失。同样,第二次辣椒素注射联合2小时40 Hz闪光刺激,可产生强效且持久的镇痛作用。以上结果表明,在疼痛通路重新激活后,通过CeA内的腺苷/A2AR信号,可使已稳固形成的痛觉过敏失稳并被擦除。
图12.CeA中腺苷水平升高可破坏疼痛相关记忆痕迹的稳定性
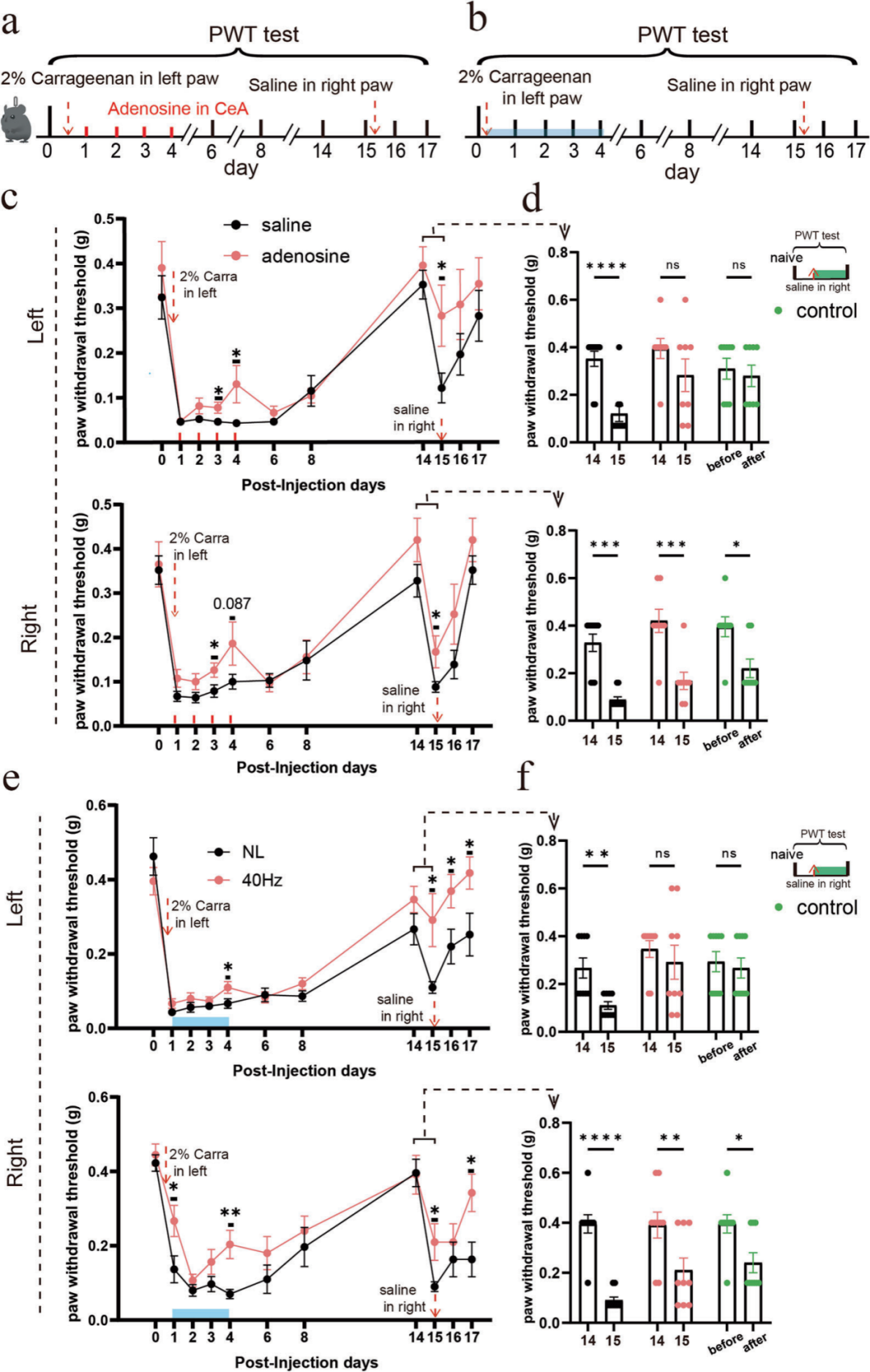
为进一步探究腺苷和40 Hz闪光对疼痛记忆提取的影响,本研究采用角叉菜胶诱导炎症后,通过交叉注射溶媒诱发远隔性痛觉过敏的模型。在该模型中,单侧注射角叉菜胶可诱发注射侧(左后足)痛觉过敏,持续约1周,至第14天逐渐缓解;同时对侧未注射的右后足会出现继发性痛觉过敏。治疗组在角叉菜胶注射后,连续4天每日向右侧CeA输注1.0 μg腺苷,对照组则输注生理盐水。腺苷给药4天后,双侧后足的机械性痛觉过敏均得到显著缓解。待第14天PWT恢复至基线水平后,于第15天向对侧原未注射侧(右后足)交叉注射生理盐水。两组在溶媒注射侧后足均再次出现机械性痛觉过敏。重要的是,在原角叉菜胶注射侧(左后足),仅对照组重新出现痛觉过敏,腺苷处理组未出现该现象。作为对照,正常小鼠仅在右后足接受一次生理盐水注射,仅会在4小时内诱发同侧痛觉过敏,对侧无明显变化,提示单纯生理盐水注射不会诱发未注射侧的机械性痛觉过敏。上述结果表明,在角叉菜胶致炎早期向右侧CeA输注腺苷,可有效抑制疼痛记忆的提取。
本研究使用相同的角叉菜胶疼痛模型探究40 Hz闪光的作用。角叉菜胶注射后,治疗组连续4天每日接受2小时40 Hz闪光刺激,对照组置于正常光照环境中。至第4天,光刺激即可显著缓解双侧后足的机械性痛觉过敏。第14天PWT恢复正常后,于第15天交叉注射生理盐水,两组在注射侧均出现痛觉过敏;而在原炎症侧(左后足),仅对照组痛觉过敏复发,40 Hz光处理组未出现痛觉超敏复发。值得注意的是,治疗组原炎症侧后足的PWT在交叉注射后出现短暂下降,随后回升并持续升高。上述结果提示,40 Hz闪光不仅可缓解持续性疼痛,还可主动破坏或逆转病理性疼痛记忆痕迹。
图13.40 Hz闪光可抑制疼痛记忆的提取
总结
慢性疼痛作为高发、致残性疾病,现有药物疗效有限且副作用显著,神经调控则有望重塑异常中枢环路。本研究证实,40 Hz闪光是一种无创、强效的慢性疼痛干预手段,可显著缓解慢性炎性疼痛与神经病理性疼痛,其镇痛效应严格依赖光刺激的频率与强度,核心通路为直接的视网膜-CeA通路;该干预可特异性促进CeA局部腺苷释放,从而规避全身给予腺苷所带来的心血管等不良反应。
该镇痛机制以CeA为核心:40 Hz闪光通过视网膜-CeA通路激活CeA内脑啡肽能(Penk⁺)神经元,促进内源性腺苷释放,进而激活CeA内A2AR介导的信号通路。更关键的是,本研究证实慢性疼痛由CeA内的类记忆机制主动维持,而40 Hz闪光可破坏CeA中病理性疼痛记忆的巩固与提取,从机制层面革新了对慢性疼痛持续存在的传统认知。
综上,本研究不仅阐明了40 Hz闪光镇痛的分子与神经环路机制,更确立了其无创、环路特异性、神经化学靶向的治疗价值,为慢性疼痛治疗带来范式转变,实现了视觉刺激调控、内源性腺苷信号激活与疼痛记忆重塑的有机整合。
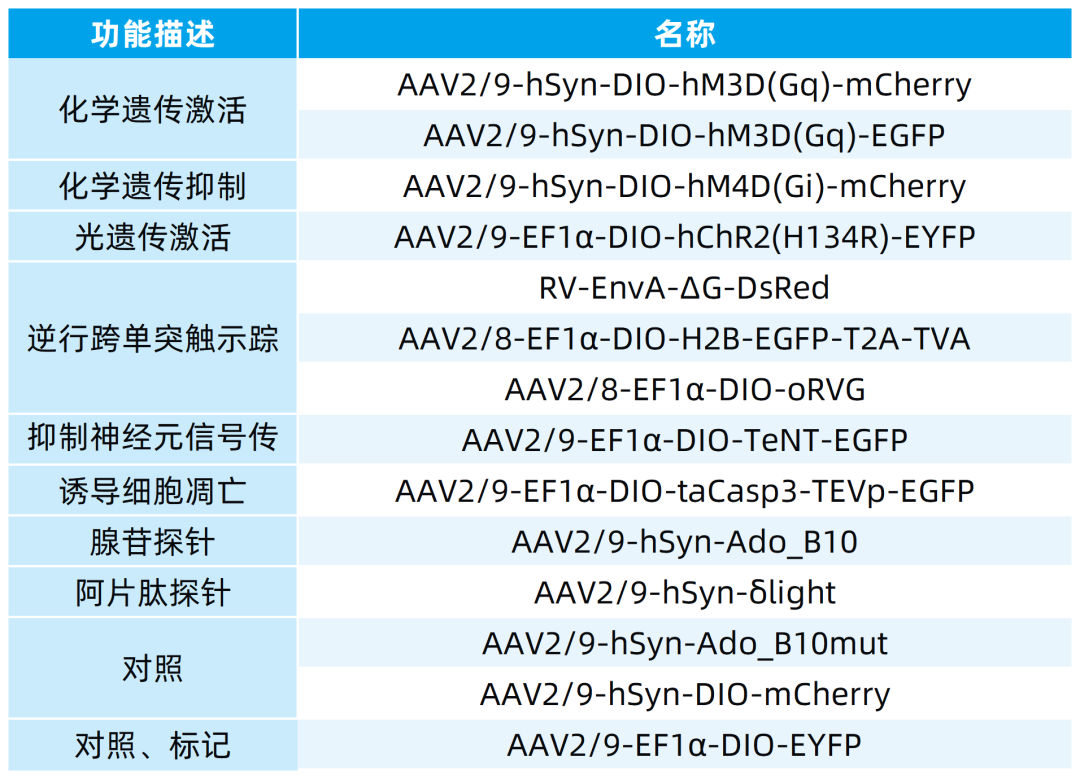
本文使用的来自枢密科技的病毒产品,列表如下:
扫码添加客服
更多产品及详情欢迎咨询!


市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK