2026-04-23 阅读量:17
慢性疼痛累及全球近20%人群,患者常并发焦虑、抑郁等情绪障碍。疼痛与负性情绪相互加剧、形成恶性循环,最终使合并情绪共病的慢性疼痛成为临床难治性问题,现有药物难以实现理想缓解效果。应激是调控痛觉与疼痛进展的关键因素,其效应依赖作用时长与模式:急性高强度应激可发挥镇痛作用,慢性持续应激则诱发痛觉过敏。既往研究证实,下丘脑-垂体-肾上腺(HPA)轴是应激调控疼痛的核心通路,但HPA轴介导急、慢性应激差异化调控痛觉及疼痛进程的具体神经机制,尚不明确。
2025年8月8日,江苏省人民医院/南京医科大学第一附属医院杨春教授团队联合徐州医科大学江苏省麻醉学重点实验室曹君利教授,在Molecular Psychiatry(IF=10.1)发表题为“Acute and chronic stress differentially regulate pain via distinct ensembles in the paraventricular nucleus of hypothalamus”的研究论文。该研究利用雄性小鼠束缚应激模型与完全弗氏佐剂(CFA)炎症痛模型证实:急性束缚应激(ARS)在正常生理状态与病理疼痛状态下均能产生镇痛效应;慢性束缚应激(CRS)则会加重正常生理状态下的痛觉过敏,并在疼痛状态下延长疼痛持续时间,同时诱发焦虑抑郁样行为。下丘脑室旁核(PVN)内存在两类可被急、慢性应激差异化激活的神经元集群。研究通过活性神经元靶向重组(TRAP)技术与化学遗传学手段证实,上述神经元集群分别介导急、慢性应激对疼痛的调控作用,并进一步通过双载体策略明确,两类神经元分别经PVN-蓝斑(PVN-LC)与PVN-外侧隔核(PVN-LS)投射通路发挥功能。
综上,本研究揭示了急、慢性应激对疼痛发生发展的差异化调控效应,阐明了PVN特异性神经元集群及其下游神经环路的核心作用,完善了应激-疼痛相互作用的神经机制体系。该成果为阐释疼痛慢性化机制提供了新视角,也为临床慢性疼痛合并情绪共病的精准干预提供了潜在的靶点与理论支撑。
1.急、慢性应激对疼痛及相关行为的差异化作用
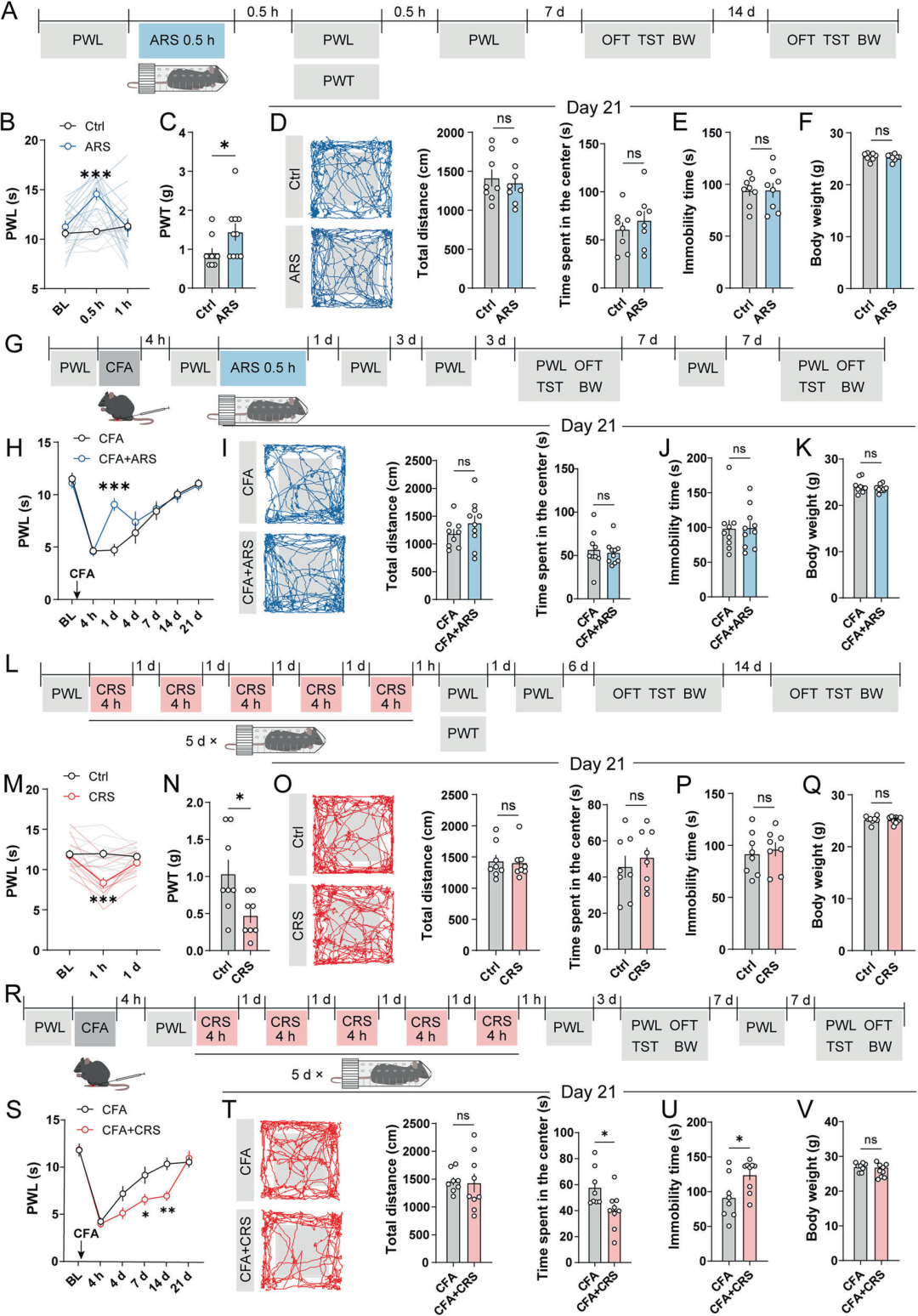
为探究应激对疼痛的调控作用,本研究构建小鼠ARS与CRS模型:ARS为单次30 min束缚干预,CRS为连续5 d、每日4 h束缚干预。ARS可快速升高naïve小鼠痛阈,且不影响旷场实验(OFT)、悬尾实验(TST)行为表现。为探究急性应激对疼痛进展的影响,本研究采用CFA诱导的小鼠炎症痛模型,并参照已有研究将CFA注射后4 h~3 d定义为炎症痛的进展阶段。在CFA注射4 h后施加ARS,可升高CFA小鼠缩爪潜伏期(PWL),产生应激诱导镇痛(SIA)并持续1 d。此外,ARS对后续炎症痛阶段的痛阈无明显影响,也未改变CFA小鼠的情绪相关行为。
与ARS不同,CRS可诱导naïve小鼠对伤害性热刺激、机械刺激产生痛觉过敏,表现为CRS造模1 h后小鼠痛阈降低。CRS造模后1 w、3 w,小鼠情绪行为均未受影响;在CFA注射4 h后施加为期5 d的CRS(首次束缚于CFA注射4 h后进行),可加剧CFA小鼠第7、14 d的痛敏程度,至第21 d痛阈才与对照组趋于一致;而单纯CFA小鼠PWL显著降低并于14 d内恢复至基线水平,提示CRS可延长炎症痛病程。此外,CFA注射后3 w,小鼠在旷场中央停留时间缩短、悬尾不动时间延长,提示小鼠出现焦虑抑郁样行为。上述结果明确提示:ARS与CRS在痛觉感知及疼痛发生发展过程中发挥着截然不同的关键调控作用。随后,本研究采用强迫游泳模型验证应激对疼痛的作用:急性强迫游泳应激(AFS)时长为2 min,慢性强迫游泳应激(CFS)为连续2 d,每日15 min。与对照组相比,AFS可升高小鼠PWL,而CFS则使其降低,该结果进一步佐证了SIA与应激诱导痛觉过敏(SIH)的存在。此外,应激处理后1 w,经OFT与TST评估的小鼠情绪行为均无统计学差异。
为探究预暴露应激对疼痛慢性化的影响,研究在CFA注射前分别实施ARS与CRS,二者分别诱导小鼠产生SIA与SIH。CFA注射后,小鼠PWL下降并在14 d内恢复至正常水平;且在CFA注射后第1、3 w,疼痛模型造模前施加的ARS或CRS均未改变小鼠的情绪行为。该结果表明,应激预暴露对痛觉感知及疼痛相关反应的发生发展几乎无影响。慢性疼痛建立后再施加应激也可能成为混杂因素。为排除该干扰,本研究在CFA注射后第3-7 d对炎症痛小鼠实施每日4 h的CRS处理。结果显示,末次CRS处理30 min后(第7 d),CFA小鼠PWL降低;但在第14、21 d,其PWL与单纯CFA模型小鼠无差异,OFT、TST检测的情绪行为也相近。上述结果提示,慢性疼痛建立后再施加慢性应激,不影响疼痛持续时长,也不诱发相关焦虑抑郁样行为。
图1.急、慢性应激对疼痛及相关情绪行为的差异性影响
2.下丘脑室旁核神经元集群的激活
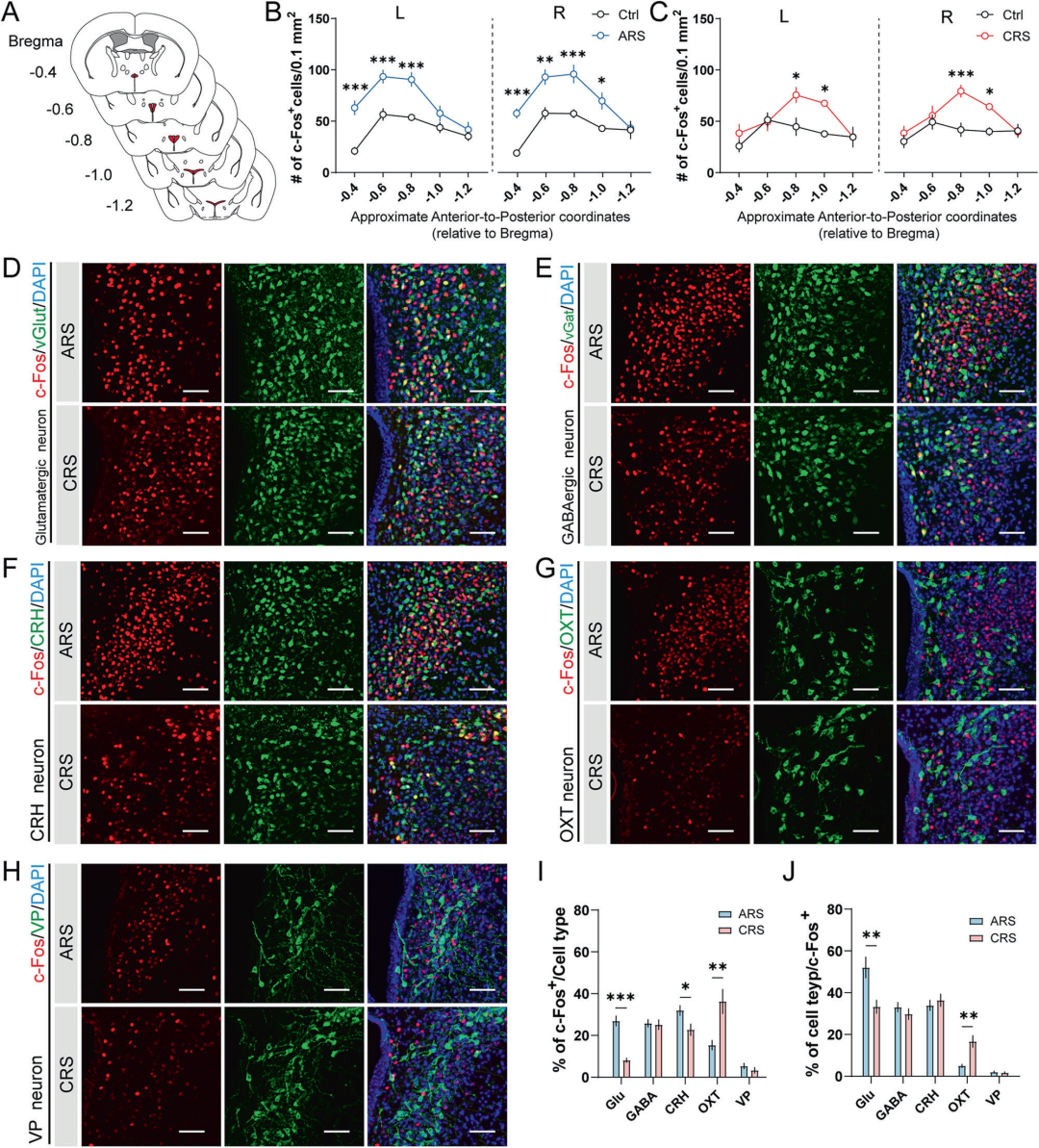
为筛选介导应激调控疼痛的关键脑区,本研究选取25个参与应激应答与自主神经调控的核心脑区,通过c-Fos免疫荧光染色,分别检测急性、慢性应激后的神经元活化特征。结果显示,ARS与CRS可诱发完全不同的脑区活化模式:ARS会降低边缘前皮质、边缘下皮质、前扣带回皮层、伏隔核、外侧隔核(LS)、外侧下丘脑、下丘脑背内侧核及海马亚区的神经元活性,同时显著激活下丘脑室旁核(PVN)、弓状核、臂旁核(PBN)与蓝斑(LC);CRS则抑制前扣带回皮层、基底外侧杏仁核及海马神经元,仅特异性激活LS与PVN。综上,PVN可同时响应急性与慢性应激,是应激调控的关键中枢核团。
PVN为下丘脑-垂体-肾上腺(HPA)轴核心结构,富含多种功能神经元,参与应激反应、能量稳态、免疫调节等多项生理过程。为明确两种应激是否激活PVN同一类神经元,本研究沿头尾轴定位并量化活化细胞:ARS主要激活PVN前中部神经元,CRS则集中活化PVN中后部神经元。为进一步探究急、慢性应激在PVN内激活的神经元类型,本研究采用免疫荧光染色联合腺相关病毒(AAV)介导的荧光蛋白神经标记技术进行分析,共靶向标记5类关键神经元:谷氨酸能神经元、GABA能神经元、CRH神经元(促肾上腺皮质激素释放激素神经元)、催产素(OXT)神经元及加压素(VP)神经元。结果显示,ARS与CRS在PVN内激活的神经元类型存在显著差异:ARS以大量激活谷氨酸能神经元和CRH神经元为主,而CRS则优先活化OXT神经元,提示急、慢性应激可在PVN内触发截然不同的神经应答。
本研究采用TRAP靶向标记技术,在同一小鼠体内特异性区分不同应激所激活的PVN神经元:将AAV-DIO-Gi-mCherry载体注射至FosCreERT2小鼠的PVN脑区,随后腹腔注射他莫昔芬并给予首次应激刺激,以此实现对初次应激活化PVN神经元的特异性标记。同时,通过c-Fos免疫荧光染色标记被第二次应激激活的神经元,其中共标记神经元代表被两次应激共同激活的PVN神经元。结果显示,当两次应激类型一致(均为ARS或均为CRS)时,PVN内共标记神经元在总mCherry阳性细胞中的占比显著更高,提示ARS与CRS可能分别募集PVN内两组相互独立的神经元集群。
图2.ARS与CRS对PVN神经元集群的激活
3.TRAP-ARS神经元
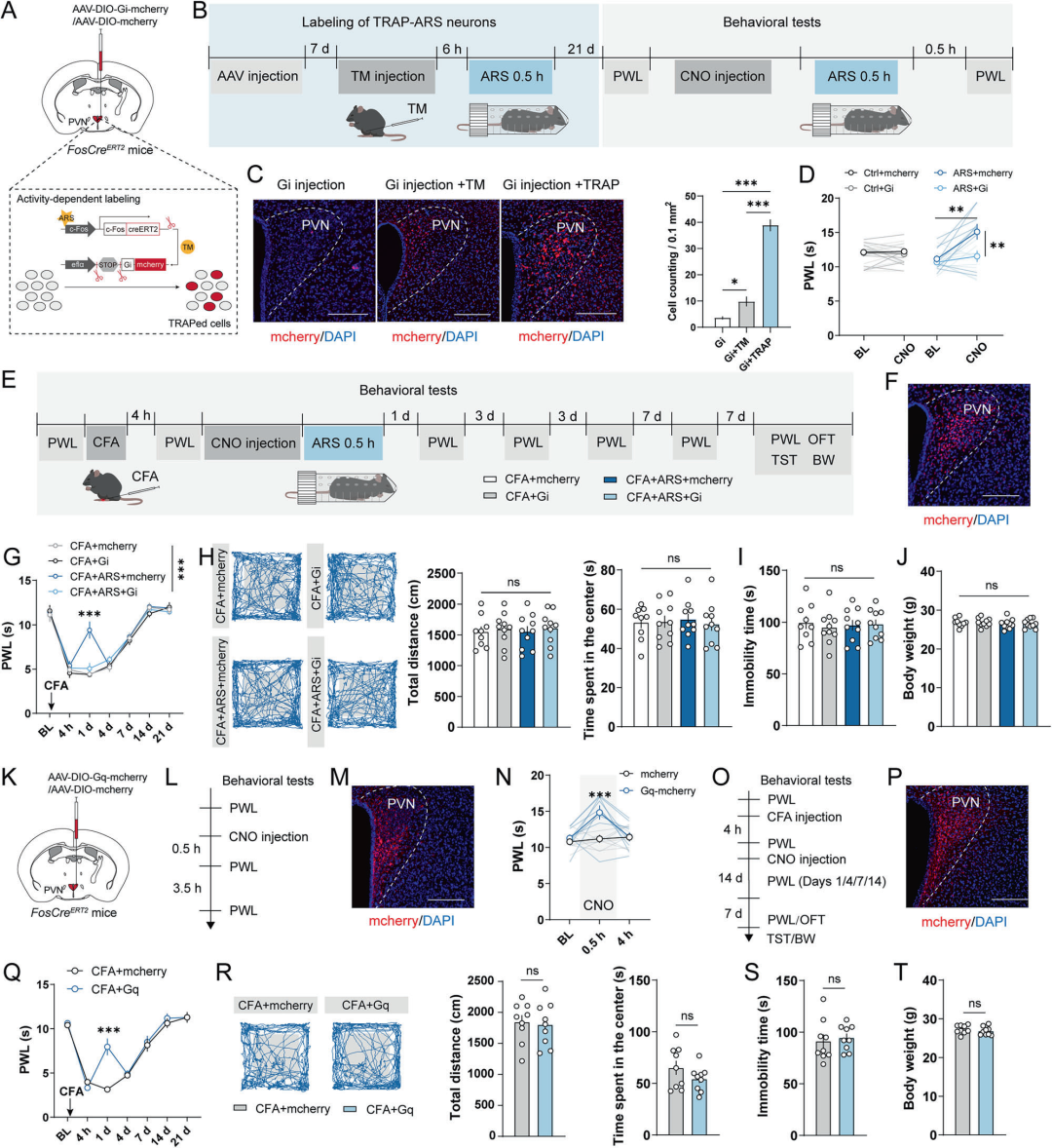
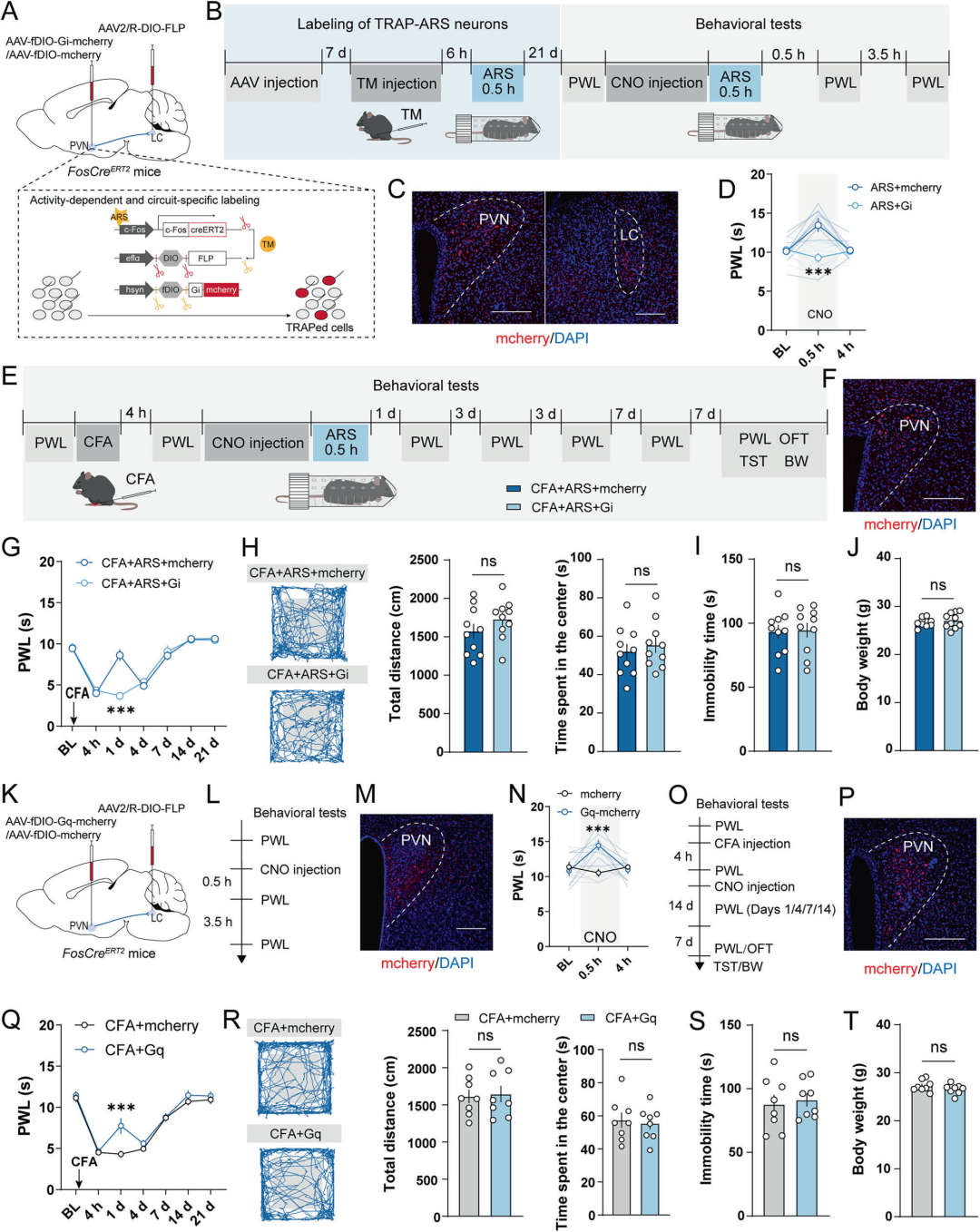
为探究急、慢性应激活化的PVN神经元集群(分别定义为TRAP-ARS神经元与TRAP-CRS神经元)的调控功能,本研究结合TRAP靶向标记技术与化学遗传学方法,通过表达Gq/Gi受体调控神经元活性。ARS处理前腹腔注射CNO,结果显示,naïve小鼠中抑制TRAP-ARS神经元可完全阻断急性应激的镇痛效应(对照组急性应激可升高痛阈);CFA注射后4 h给予CNO,CFA诱导炎症痛小鼠中抑制TRAP-ARS神经元可逆转急性应激介导的短期(1 d)镇痛,且不影响小鼠情绪行为。另一方面,naïve小鼠中激活TRAP-ARS神经元可升高痛阈,诱发即时镇痛;CFA诱导炎症痛小鼠中激活该神经元可在造模初期(第1 d)缓解疼痛,但镇痛效应随炎症进展逐渐衰减,且不影响炎症后期小鼠行为学表现。综上,PVN内TRAP-ARS神经元可调控生理及炎症病理状态下的痛觉感知,是急性应激发挥镇痛作用的核心介导神经元集群。
图3.PVN中TRAP-ARS神经元对疼痛及相关情绪行为的影响
4.TRAP-CRS神经元
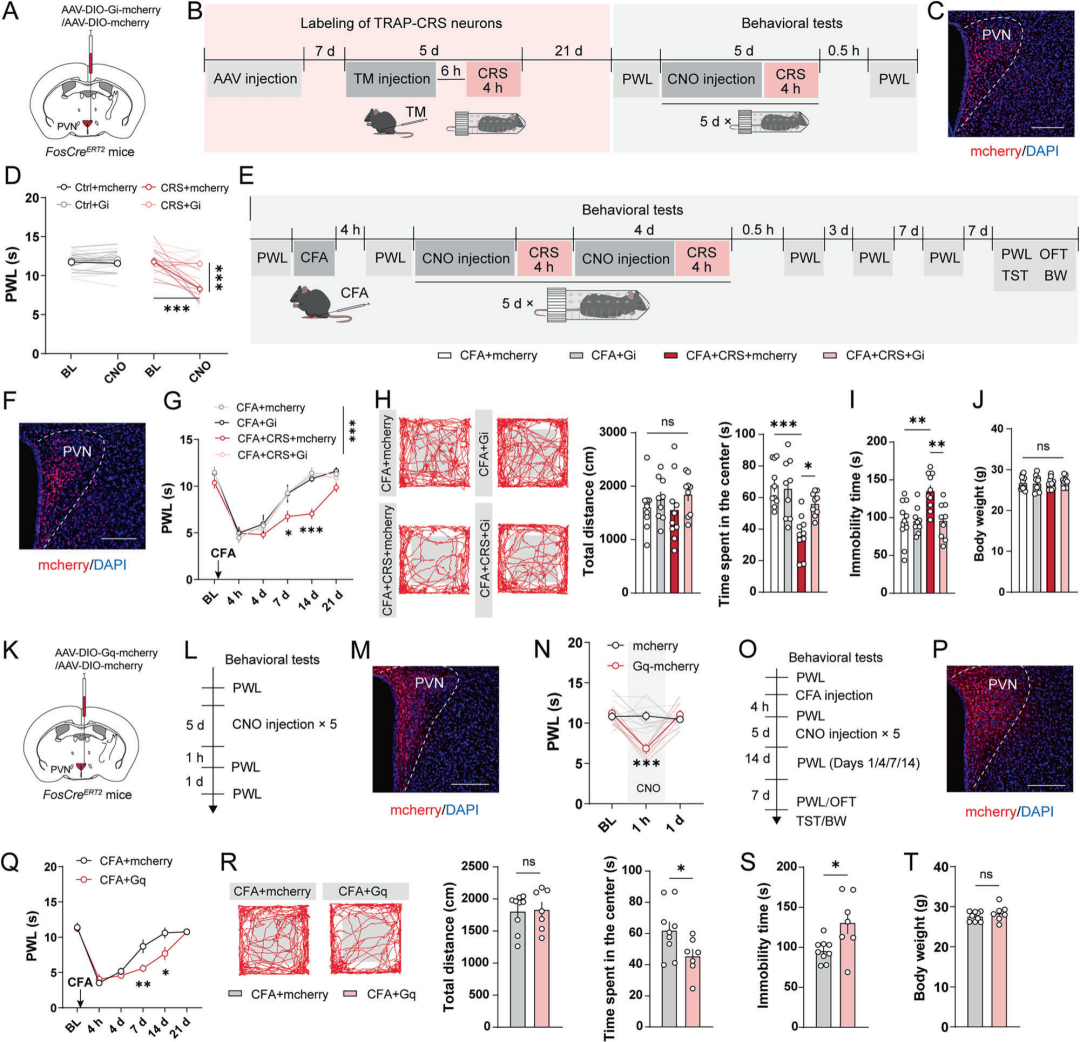
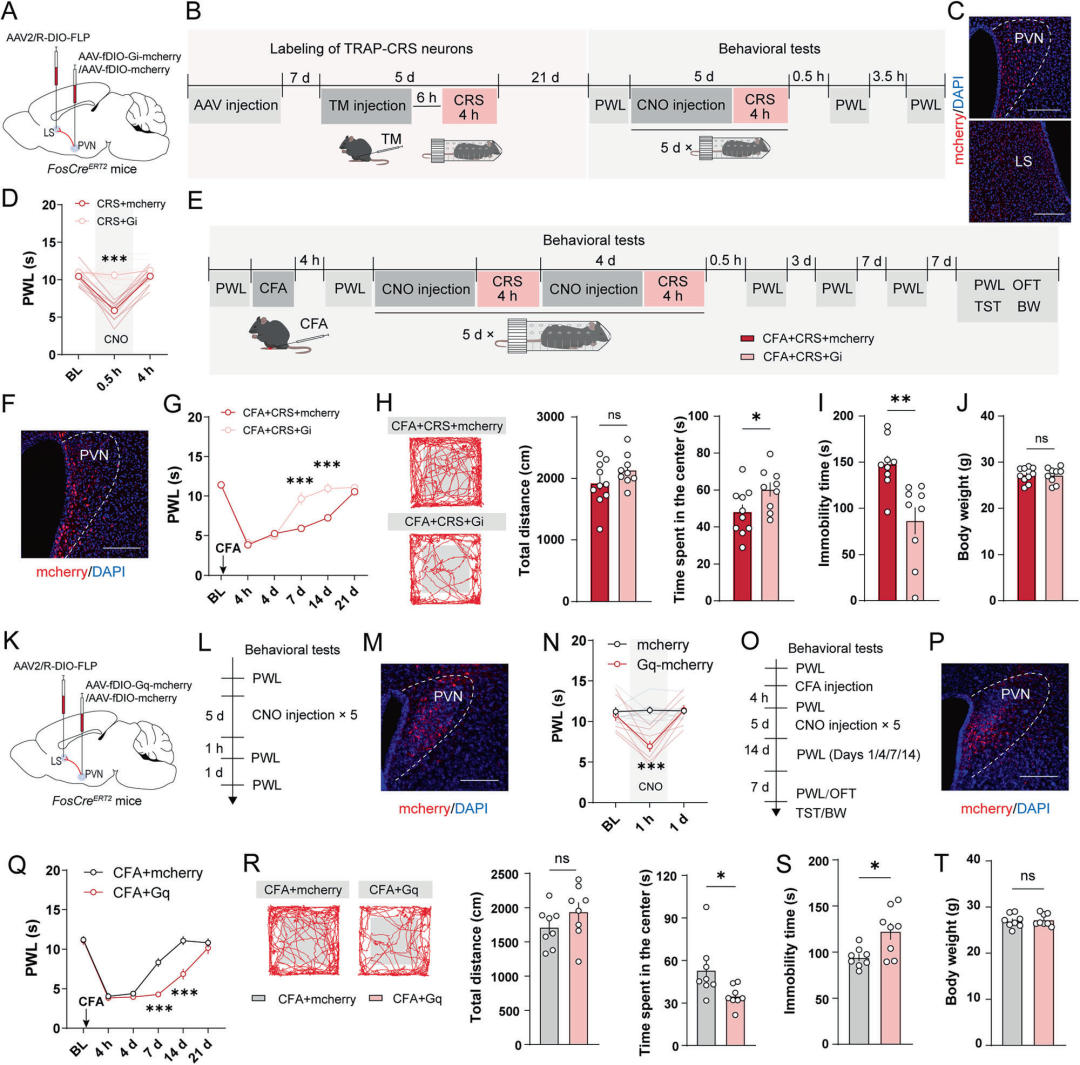
为明确TRAP-CRS神经元在慢性应激调控痛觉感知与疼痛进展中的作用,本研究结合化学遗传学方法,靶向调控PVN内该群神经元。每次CRS处理前腹腔注射CNO,结果显示,naïve小鼠中,化学遗传抑制TRAP-CRS神经元,可显著逆转慢性应激诱导的痛阈降低;CFA诱导炎症痛小鼠中,靶向抑制TRAP-CRS神经元后,慢性应激引发的痛觉过敏与情绪障碍均被有效阻断。此外,naïve小鼠中,激活TRAP-CRS神经元可诱发痛觉过敏;炎症痛小鼠经连续激活该神经元后,造模第7 d、第14 d痛敏反应显著加重,并于第21 d出现焦虑抑郁样行为。综上,PVN内TRAP-CRS神经元是介导慢性应激加剧痛觉过敏、延长炎症痛病程并诱发情绪共病的关键功能神经元集群。
图4.PVN中TRAP-CRS神经元对疼痛及相关情绪行为的影响
5.TRAP-ARS/CRS神经元的神经投射
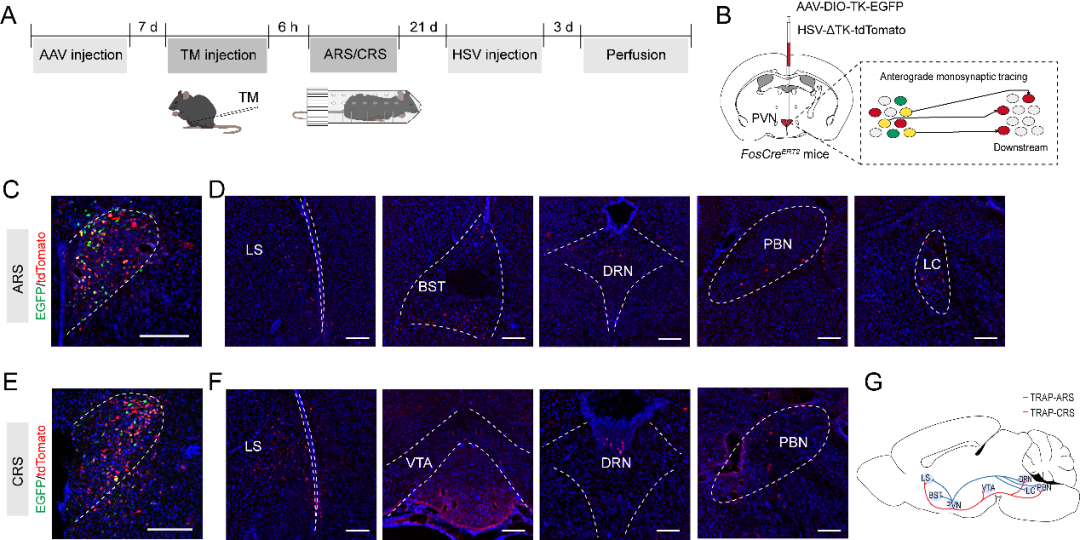
已有研究证实,PVN及其相关神经环路深度参与疼痛感受及疼痛相关负性情绪的调控。本研究深入探究PVN内TRAP-ARS和TRAP-CRS神经元发挥作用的环路机制。首先,本研究采用缺陷型单纯疱疹病毒(HSV)介导的顺向单突触示踪技术,分别可视化标记PVN内TRAP-ARS与TRAP-CRS神经元支配的下游脑区。TRAP-ARS神经元可与多个核心脑区形成突触联系,包括LS、终纹床核(BNST)、中缝背核(DRN)、PBN和LC。与之相似,TRAP-CRS神经元靶向支配的下游细胞主要集中于LS、腹侧被盖区(VTA)、DRN和PBN。
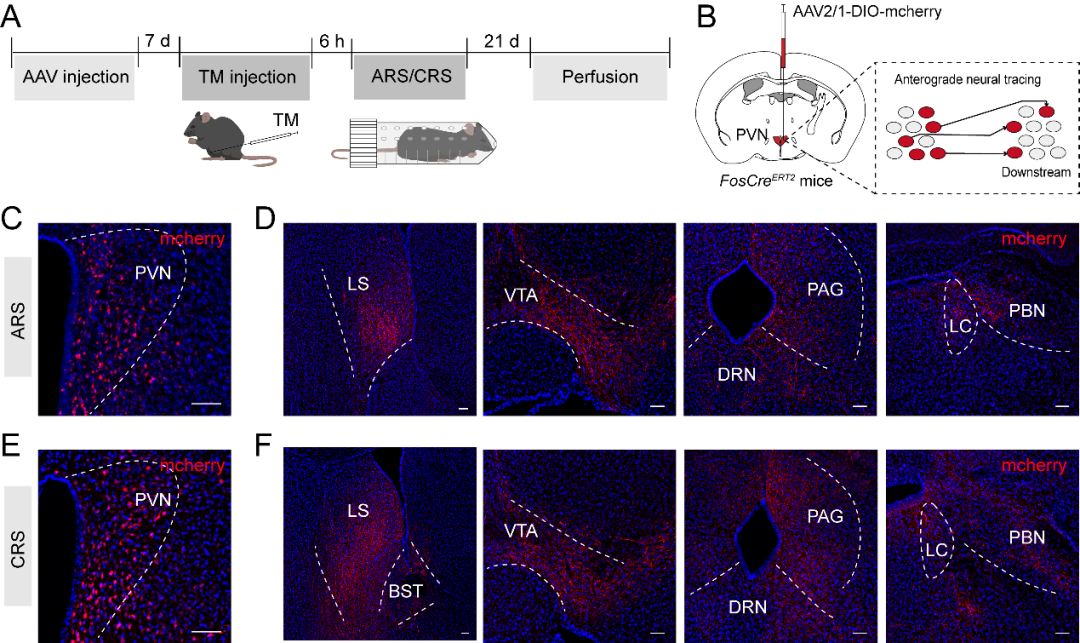
值得注意的是,由于HSV具有固有的神经毒性,该方法获得的示踪结果可能存在一定偏差。为规避该问题,本研究另外采用高滴度1型血清型AAV载体对下游脑区进行鉴定。出乎意料的是,基于AAV的示踪结果与HSV介导的示踪结果高度一致。
图5.HSV介导的PVN内TRAP-ARS与TRAP-CRS神经元顺向单突触示踪
图6.AAV介导的PVN内TRAP-ARS与TRAP-CRS神经元顺向单突触示踪
6.PVN-LC神经投射
LC可被ARS显著激活,作为脑内去甲肾上腺素(NE)的主要来源核团参与痛觉调控。应激状态下PVN与LC存在反馈环路,因此本研究推测PVN-LC投射通路介导PVN内TRAP-ARS神经元的镇痛效应。
本研究采用Cre/Flp双病毒载体策略,在FosCreERT2小鼠LC注射AAV2/R-DIO-FLP(逆行),并将AAV-fDIO-Gi/Gq-mCherry载体注射至PVN,从而特异性标记并化学遗传调控投射至LC的TRAP-ARS神经元。抑制该类神经元可逆转naïve小鼠中ARS诱导的痛阈升高;在CFA诱导炎症痛小鼠中,同样可阻断急性应激的短期镇痛作用,且不影响疼痛进程与情绪行为。与之相反,抑制PVN-LC投射环路TRAP-ARS神经元,对单纯CRS及CFA+CRS小鼠的痛阈均无显著影响,亦不影响CFA+CRS小鼠情绪行为。综上,在naïve小鼠及炎症痛小鼠模型中,化学遗传抑制PVN-LC通路TRAP-ARS神经元可特异性拮抗ARS的镇痛效应。进一步地,化学遗传激活PVN-LC通路TRAP-ARS神经元,可快速提升naïve小鼠及CFA造模后第1 d小鼠的痛阈,从而模拟ARS的镇痛效果。
图7.ARS的作用由PVN-LC投射介导
7.PVN-LS神经投射
CRS可显著激活LS。LS是调控情绪行为、认知与痛觉的关键核团,接受PVN的神经投射,已有研究表明PVN-LS通路参与内脏痛敏的调控。本研究结合双病毒载体策略与化学遗传技术,特异性调控PVN-LS投射内的TRAP-CRS神经元,解析该环路介导应激调控痛觉的作用。化学遗传抑制该类神经元,可逆转慢性应激所致的naïve小鼠痛阈下降;在CFA诱导炎症痛模型中,能有效缓解慢性应激诱发的持续性痛觉过敏,显著提升造模后第7、14 d的痛阈,且可改善小鼠焦虑抑郁样行为。此外,持续化学遗传激活PVN-LS通路TRAP-CRS神经元,可诱发naïve小鼠痛觉过敏,加剧炎症痛小鼠造模后第7、14 d疼痛程度,并诱导产生焦虑抑郁样情绪障碍。
图8.CRS的作用由PVN-LS投射介导
总结
本研究证实,急性与慢性应激对痛觉感知及疼痛进程具有截然不同的调控作用。ARS可诱发短暂的SIA,而CRS则会加剧痛觉过敏、延长炎症痛病程,并诱导疼痛相关的焦虑抑郁样情绪障碍。PVN内存在两类特异性激活的神经元集群,即TRAP-ARS神经元与TRAP-CRS神经元,二者分别特异性响应急性与慢性应激,构成应激双向调控痛觉的核心细胞学基础。
神经环路层面,PVN-LC投射通路特异性介导急性应激的镇痛作用,PVN-LS通路则专一调控慢性应激诱导的痛敏、延长炎症痛病程及疼痛-情绪共病;两条通路的神经元几乎无重叠、功能相互独立。本研究系统阐明了急慢性应激差异化调控痛觉的神经环路机制,为解析疼痛慢性化的病理机制、研发疼痛合并情绪共病的临床干预策略提供了全新实验依据。
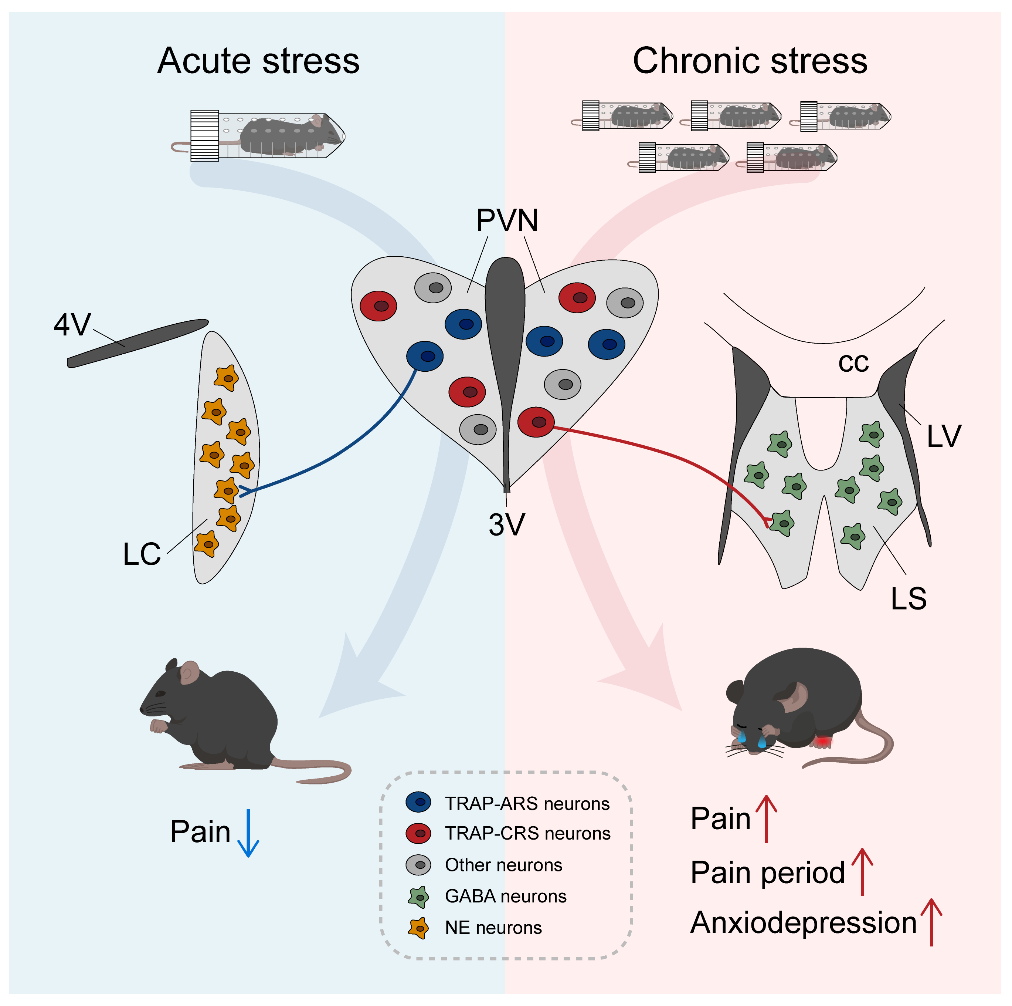
图9.急、慢性应激差异性调控痛觉感知与疼痛进程的机制模式图
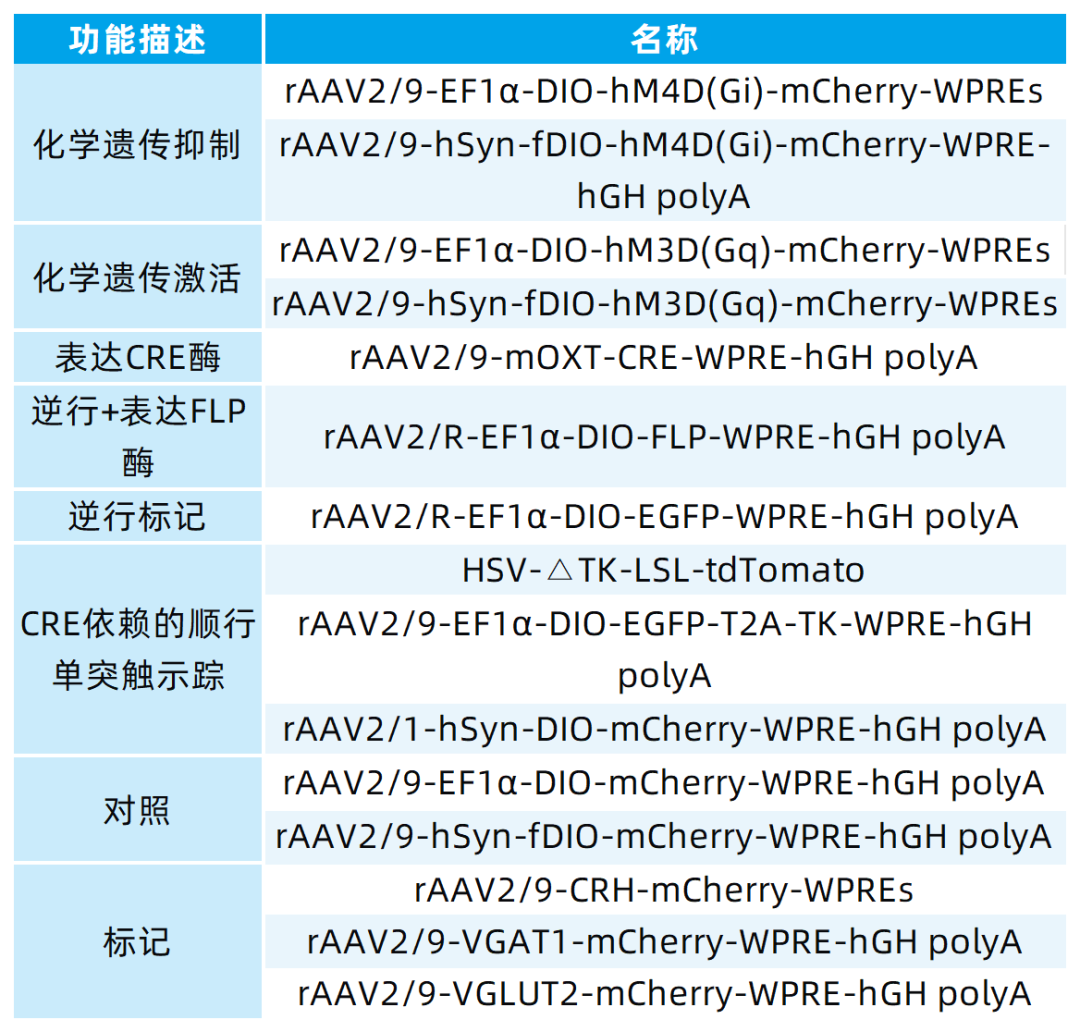
本文使用的病毒产品均来自枢密科技,列表如下:
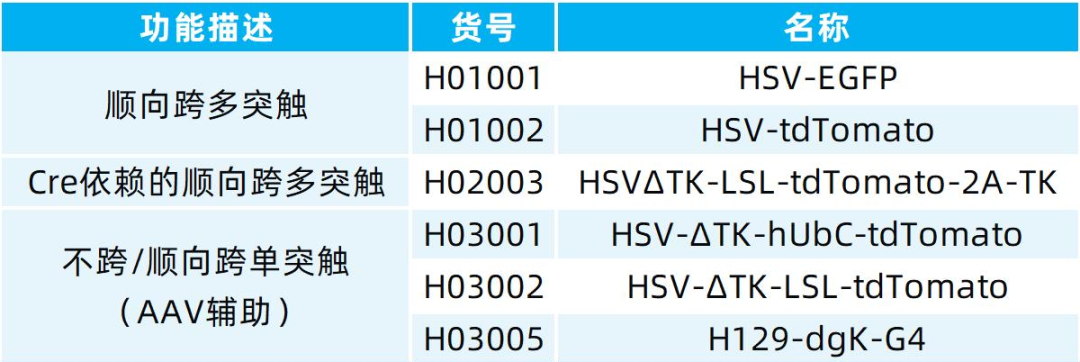
我司可提供顺向跨单突触、顺向跨多突触HSV神经示踪病毒,部分产品列表如下:
扫码添加客服
更多产品及详情欢迎咨询!


市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK