2026-04-07 阅读量:129
基于将环化重排绿色荧光蛋白(cpGFP)嵌入G蛋白偶联受体(GPCR)而构建的基因编码荧光探针(以下简称GPCR型探针),能够以高时空分辨率在体光学检测神经调质。此类探针是对现有在体神经调质监测技术(微透析、快速扫描循环伏安法、CniFERs、iTango)的重要补充。将红色荧光探针加入该工具库进一步拓展了其应用场景,如可与蓝光激发的光遗传工具联用,或实现神经递质的多通道并行成像。
神经调质去甲肾上腺素(NE)在脑内发挥重要功能,包括调控觉醒、警觉性及应激反应等。尽管在体直接检测NE的工具需求持续攀升,当前可用工具仍较为有限,其核心原因之一在于相关工具的开发需投入大量人力开展筛选工作。事实上,通常需要在哺乳动物细胞中筛选成百上千个GPCR型探针变体,才能获得具备适用于在体研究特性的候选蛋白。现有NE探针(GRABNE)可实现NE的在体光学检测,但其仅基于α2A受体(α2-肾上腺素能受体α2-AR的亚型之一)骨架构建。因此,对现有工具库进行多样化拓展具有重要意义。
瑞士苏黎世大学药理学与毒理学研究所Tommaso Patriarchi教授团队在Nature Methods期刊(IF=48)发表题为“Sensitive multicolor indicators for monitoring norepinephrine in vivo”的研究成果。本研究采用此前未被使用的受体亚型开发了NE探针。研究人员以α1A(α1-AR的亚型之一)为骨架,构建了高灵敏的绿色与红色荧光NE探针nLightG与nLightR。在多种实验体系中对其进行了系统评估,结果表明,相较于GRABNE1m探针,二者具有独特的药理学特征,且灵敏度、配体选择性与动力学特性均更优。利用此类探针,可通过多种技术手段(宽场成像、多位点光纤光度法、双光子显微成像)在离体与在体水平精准检测NE释放。如利用nLightG进行在体多位点光纤光度记录,可同时监测光遗传诱导下小鼠蓝斑(LC)与海马的NE释放;对nLightG的双光子成像结果显示,海马背侧CA1区存在与运动及奖赏相关的NE瞬变信号。综上所述,本研究构建的高灵敏NE探针(nLightG与nLightR)是对现有探针库的重要补充。该系列探针为更全面地解析NE生理功能提供了即用型研究工具,也为深入研究NE系统提供了可靠手段。

1.多色NE探针的开发
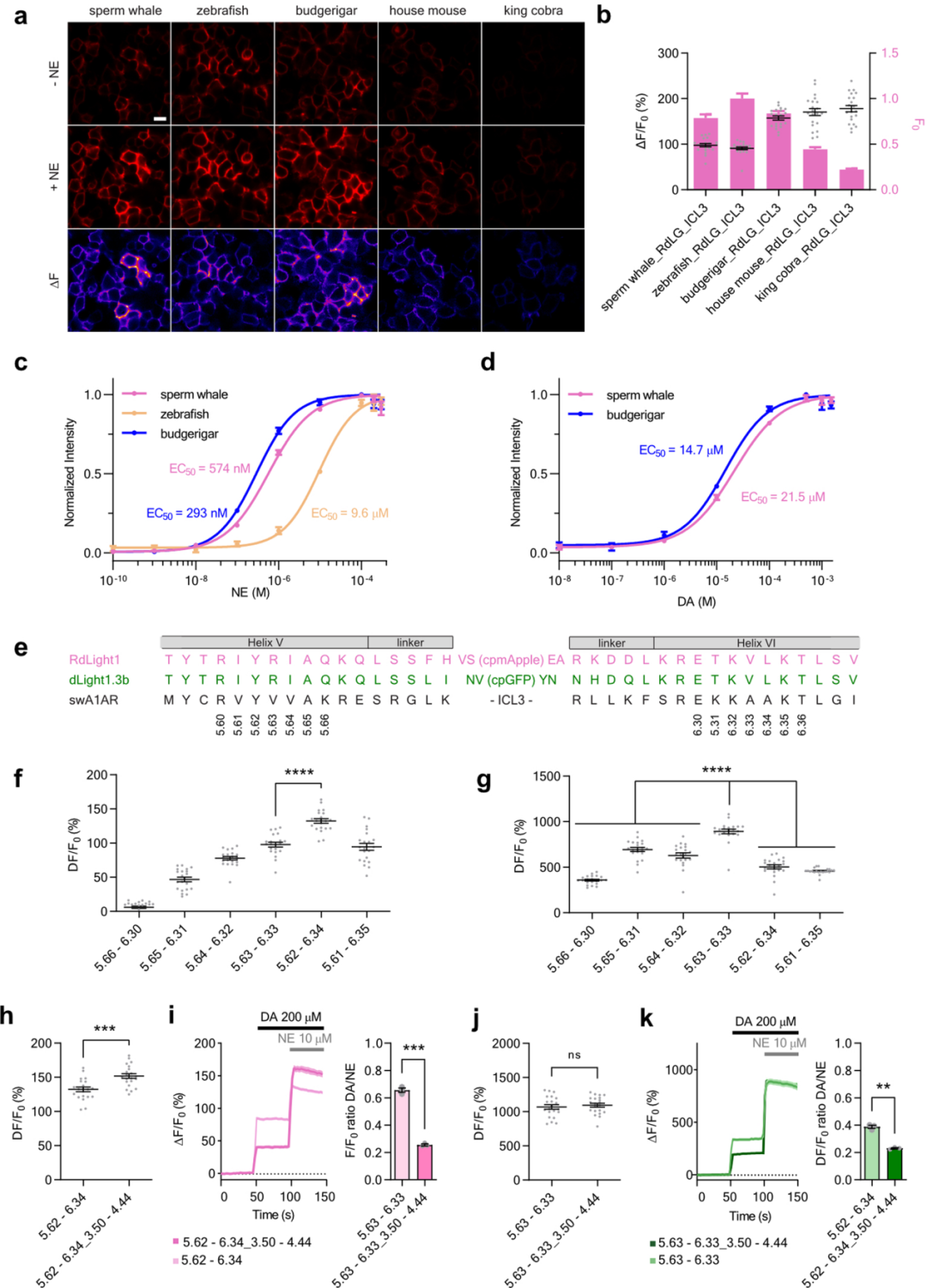
GPCR家族成员间序列差异极大,但其整体结构与激活机制均高度保守,7次跨膜螺旋的核心空间构象亦高度保守。据此,研究人员采用结构嫁接策略拓展NE探针家族:将已优化的绿色、红色DA探针dLight1.3b与RdLight1中,包含环化重排荧光蛋白及跨膜螺旋V、VI部分片段的结构域,直接嫁接至目标α1-AR。现有NE探针均为绿色,因此首先尝试构建红色NE探针,基于小鼠、虎皮鹦鹉、眼镜王蛇、斑马鱼、抹香鲸5个物种的α1-AR制备原型探针,并依据Ballesteros-Weinstein(BW)编号完成序列比对与荧光蛋白模块插入。结构比对显示,抹香鲸α1-AR(swAlpha-1 AR)与人多巴胺D1受体在插入位点结构高度保守。
5种原型探针均能在瞬时转染的HEK293T细胞膜上表达,加入10 μM NE后荧光响应(ΔF/F0)达100%~180%。其中抹香鲸、虎皮鹦鹉、斑马鱼来源的探针本底亮度最高;进一步筛选显示,抹香鲸来源探针对NE兼具高灵敏度与选择性(NE的EC50=574 nM,DA的EC50=21.5 μM),被选为后续优化对象。
随后采用dLight1.3b的荧光蛋白模块构建绿色NE探针,其ΔF/F0响应约1000%。通过并行系统优化BW嫁接位点,绿色探针初代原型动态范围最大,红色探针则获得更优嫁接位点。
前期研究发现,胞内第二环(ICL2)突变可提升GPCR型探针的荧光响应。鉴于ICL2紧邻跨膜螺旋V、VI,作者将dLight1.3b/RdLight1中包含螺旋III、IV片段及完整ICL2的结构域嫁接至NE探针原型:该改造提升了红色探针的荧光响应,且显著增强红绿两种探针对NE的选择性(优于DA)。
图1.nLightG和nLightR的开发
2.nLightG与nLightR的体外表征
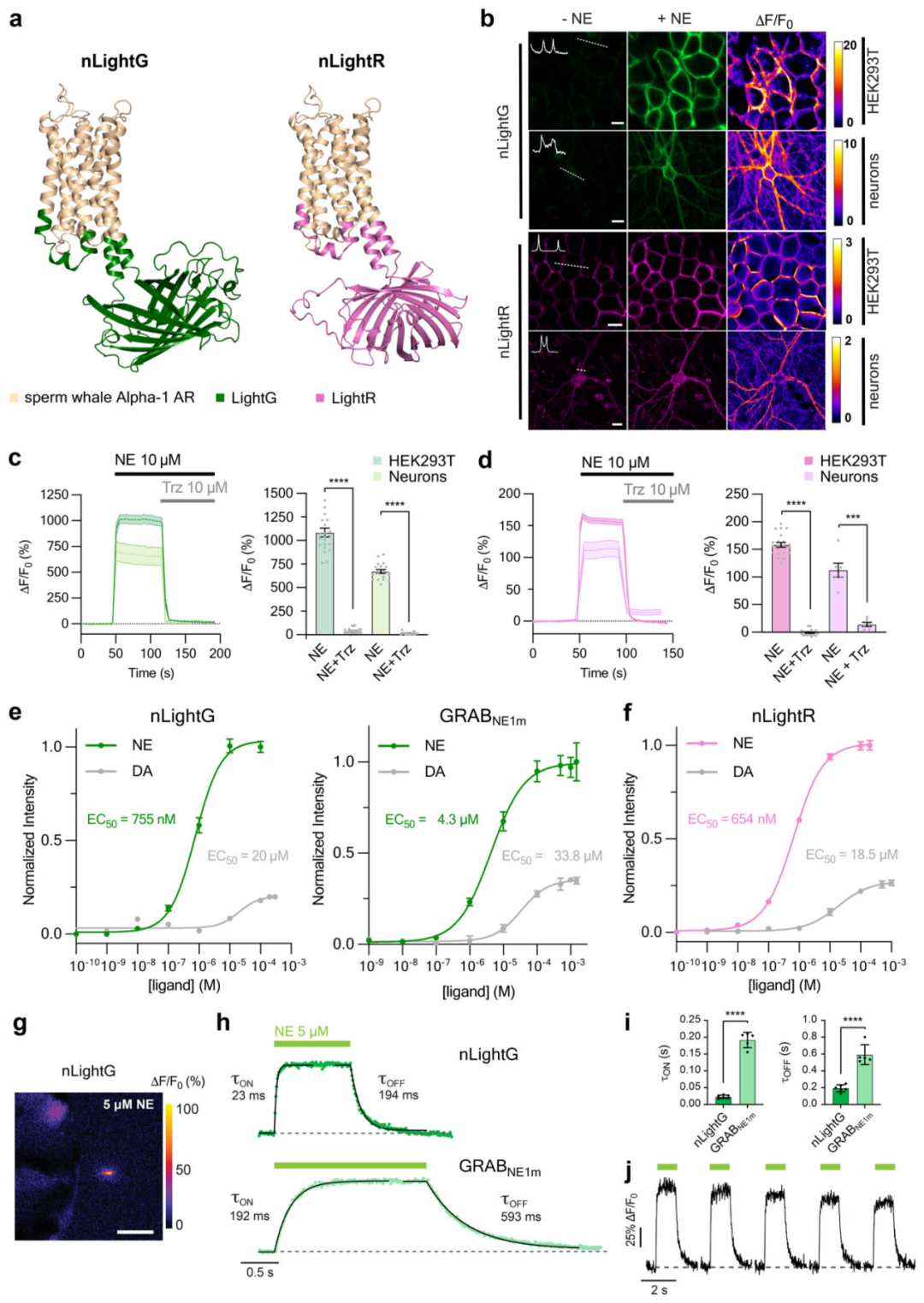
研究人员对绿色与红色NE荧光探针nLightG、nLightR进行了体外特性表征。两种探针均能良好定位于细胞膜,在HEK293T细胞与大鼠皮层神经元中经10 μM NE刺激均表现出显著的荧光响应:nLightG在HEK293T细胞中ΔF/F0为1083±47%,神经元中为671±21%;nLightR对应为158±4%与113±13%。加入α1-AR拮抗剂曲唑酮(Trz)可完全逆转两种探针的激活信号;而GRABNE1m不受Trz影响,仅能被α2-AR拮抗剂育亨宾(Yoh)灭活,体现两类探针截然不同的药理特征。HEK293T细胞中nLightG本底亮度与GRABNE1m相近。此外,光谱检测显示,nLightG与nLightR的单光子激发峰分别为498 nm、566 nm,发射峰为516 nm、594 nm;nLightG还可实现双光子激发,最佳激发波长为920 nm。
GPCR型荧光探针核心特性是其天然具备的分子特异性,在10 μM浓度下对8种神经递质进行特异性测试,结果显示仅NE、肾上腺素及低浓度DA可诱发显著荧光响应,说明探针工程改造后仍保留了swAlpha-1 AR的配体特异性。nLightG对NE的EC50在HEK293T细胞为755±85 nM,神经元中为937±133 nM;nLightR则分别为654±47 nM与408±55 nM。二者在HEK293T细胞中对DA的EC50约为NE的30倍,且DA仅能诱发不足NE 26%的最大响应,表现为部分激动效应。相比之下,GRABNE1m对DA的EC50仅为NE的8倍,最大响应可达NE的35%,表明nLightG与nLightR对NE相较于DA具有更高选择性。在培养神经元中,nLightG与nLightR由DA诱发的响应进一步降至NE的10%以下。
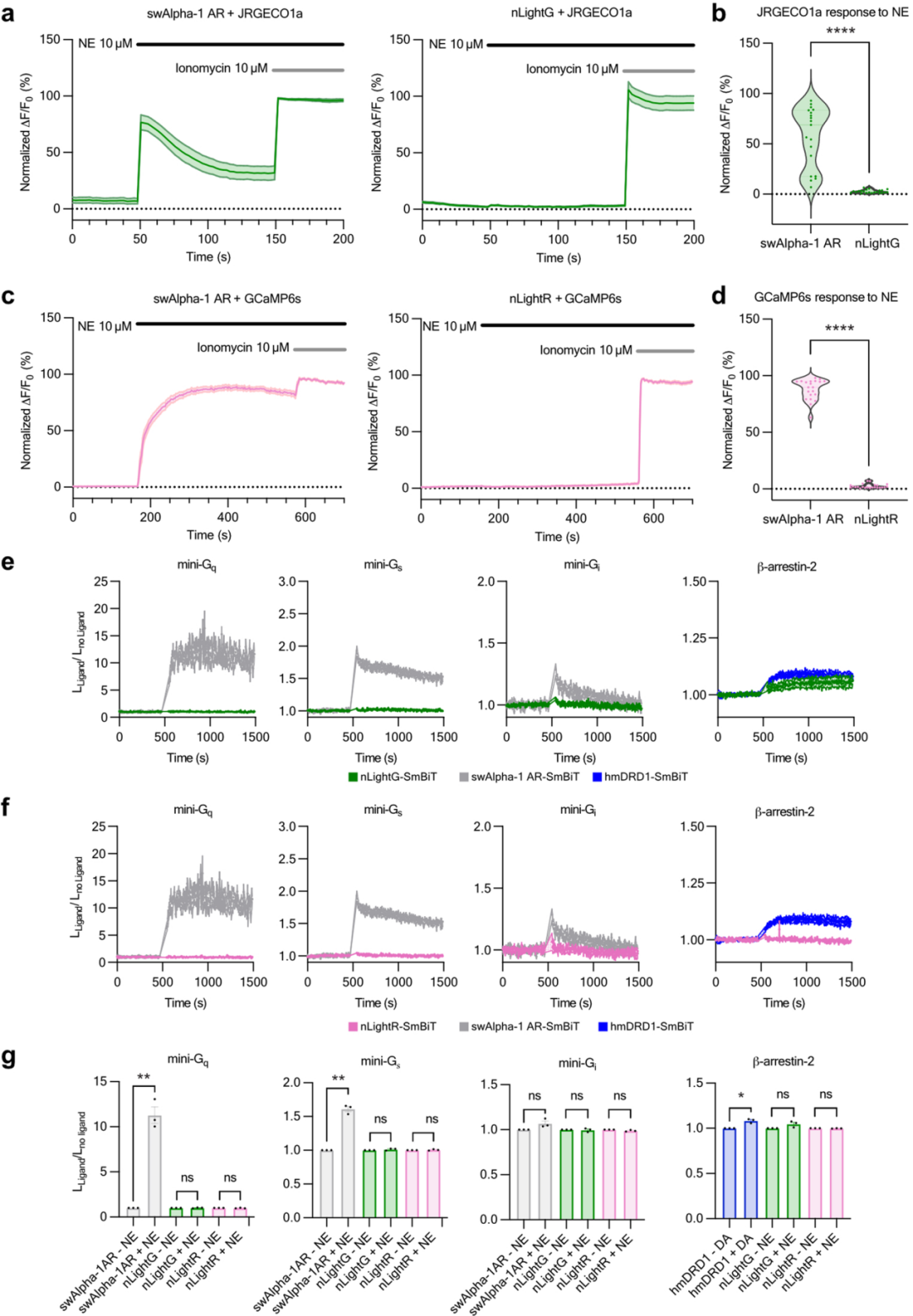
膜片钳荧光测定结果显示,nLightG具有快速的激活与失活动力学(τon=23±5 ms,τoff=194±42 ms),显著快于GRABNE1m(τon慢8倍,τoff慢3倍),可真实、连续地反映胞外NE浓度的多次快速双向变化。胞内信号实验表明,野生型swAlpha-1 AR激活后可显著升高胞内Ca²⁺浓度,提示其偶联Gαq通路;而nLightG、nLightR被NE激活后未引起显著Ca²⁺上升。NanoBiT实验进一步证实,野生型受体可偶联mini-Gq/Gs,而两种探针均不与mini-Gq/Gs/Gi结合,也不招募β-arrestin-2。
综上,nLightG与nLightR是高选择性、高灵敏度的NE荧光探针,且几乎不干扰内源性G蛋白及阻滞蛋白信号通路。
图2.nLightG与nLightR的体外特性
图3.nLightG与nLightR的胞内信号表征
3.nLightG与nLightR的离体及在体性能验证
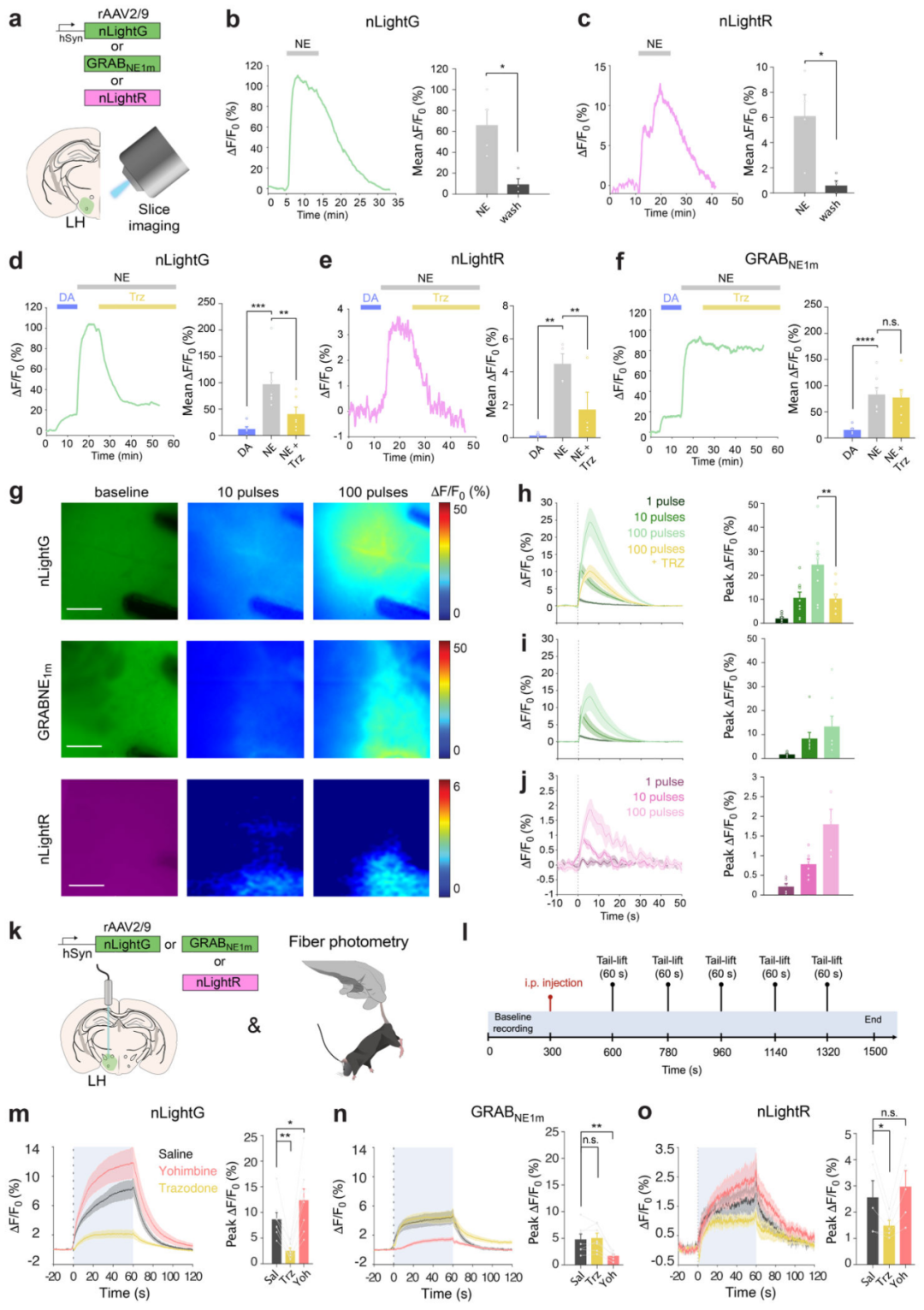
研究者在脑片水平对nLightG、nLightR进行表征,并与GRABNE1m对比。将受人突触素启动子驱动的nLightG、nLightR或GRABNE1m重组腺相关病毒(rAAV2/9.hSynapsin1.nLightG/nLightR/GRABNE1m)注射至小鼠外侧下丘脑(LH),表达至少4周后制备急性脑片并进行落射荧光成像。脑片灌流50 μM NE可诱发两种探针产生可逆的荧光响应。特异性实验显示,50 μM DA仅能诱发nLightG、nLightR产生约12%与3%的NE响应幅度,而GRABNE1m的DA响应可达NE的19%。α1-AR拮抗剂Trz可显著逆转nLightG、nLightR的NE响应,对GRABNE1m无作用,证实两类探针在脑组织中仍保持不同药理特性。
电刺激诱发内源性NE释放实验显示,nLightG与GRABNE1m均可检测单脉冲刺激信号,且响应随脉冲数增加而增强;nLightR仅能检测10次及以上脉冲信号,仍可监测内源性NE释放。
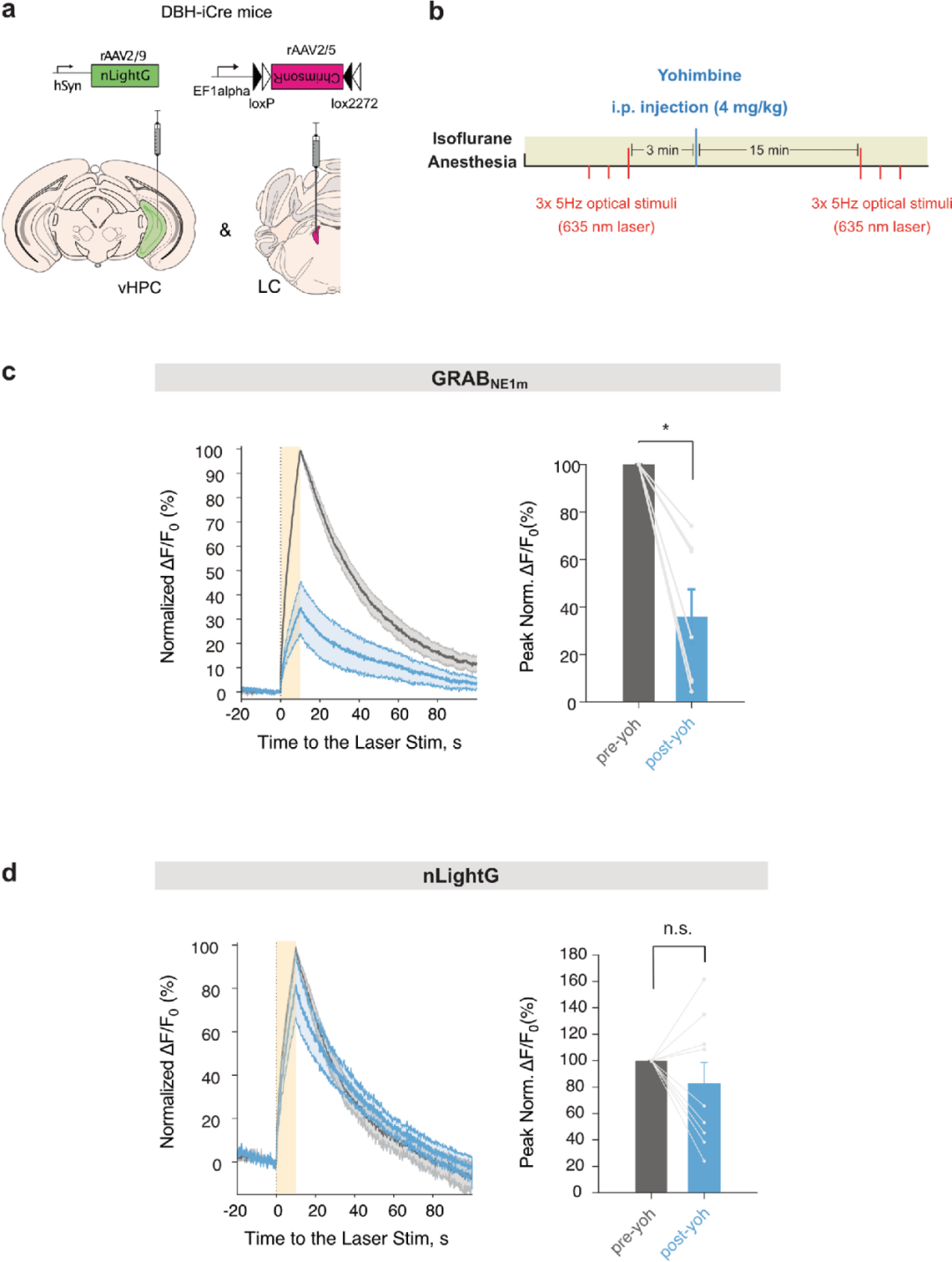
α2-AR在LC NE能神经元的突触前膜与胞体上高密度表达,可对NE释放产生反馈抑制。因此,Yoh等α2-AR拮抗剂会增强LC对外界刺激的固有兴奋性,进而增加NE释放。基于α2-AR的GRABNE1系列探针对靶向α2-AR的药物高度敏感,无法真实反映这类药物对内源性NE释放的影响,为验证nLightG和nLightR凭借其正交受体药理学特性能否克服这一局限,研究人员采用光纤光度法,在体平行对比了α2-AR亚型选择性拮抗剂作用下,nLightG、nLightR与GRABNE1m的响应差异。沿用已建立的提尾实验监测NE释放。小鼠分别注射生理盐水(Sal)、Trz(1 mg/kg)或Yoh(4 mg/kg),随后连续进行5次提尾刺激。结果显示,提尾可诱发nLightG产生稳定且可重复的信号升高(平均峰值ΔF/F0=8.7%),并在刺激全程持续存在。GRABNE1m(平均峰值ΔF/F0=4.8%)与nLightR组(平均峰值ΔF/F0=2.6%)也可检测到类似信号,但幅度更小。Trz可降低提尾诱导的nLightG、nLightR响应,却不影响GRABNE1m;与之相反,Yoh可增强nLightG、nLightR的提尾诱导响应,与该药物对LC系统已知的去抑制作用一致。而Yoh会显著抑制GRABNE1m的探针响应,与既往报道一致。
为确认Yoh的促NE释放效应是否通过α2-AR反馈环路介导、并依赖清醒状态下外界刺激对LC的调控,在麻醉小鼠中检测了其对腹侧海马(vHPC)光遗传学诱导NE释放的影响。在该条件下,Yoh可抑制GRABNE1m监测的光遗传学诱发NE信号,但不影响nLightG的信号。
综上,nLightG、nLightR具有与GRABNE1m截然不同的药理学特征,为在体研究α2-AR靶向药物对内源性NE系统的作用提供了重要工具。
图4.nLightG与nLightR的离体及在体性能测试
4.基于光遗传解析不同脑区的NE释放
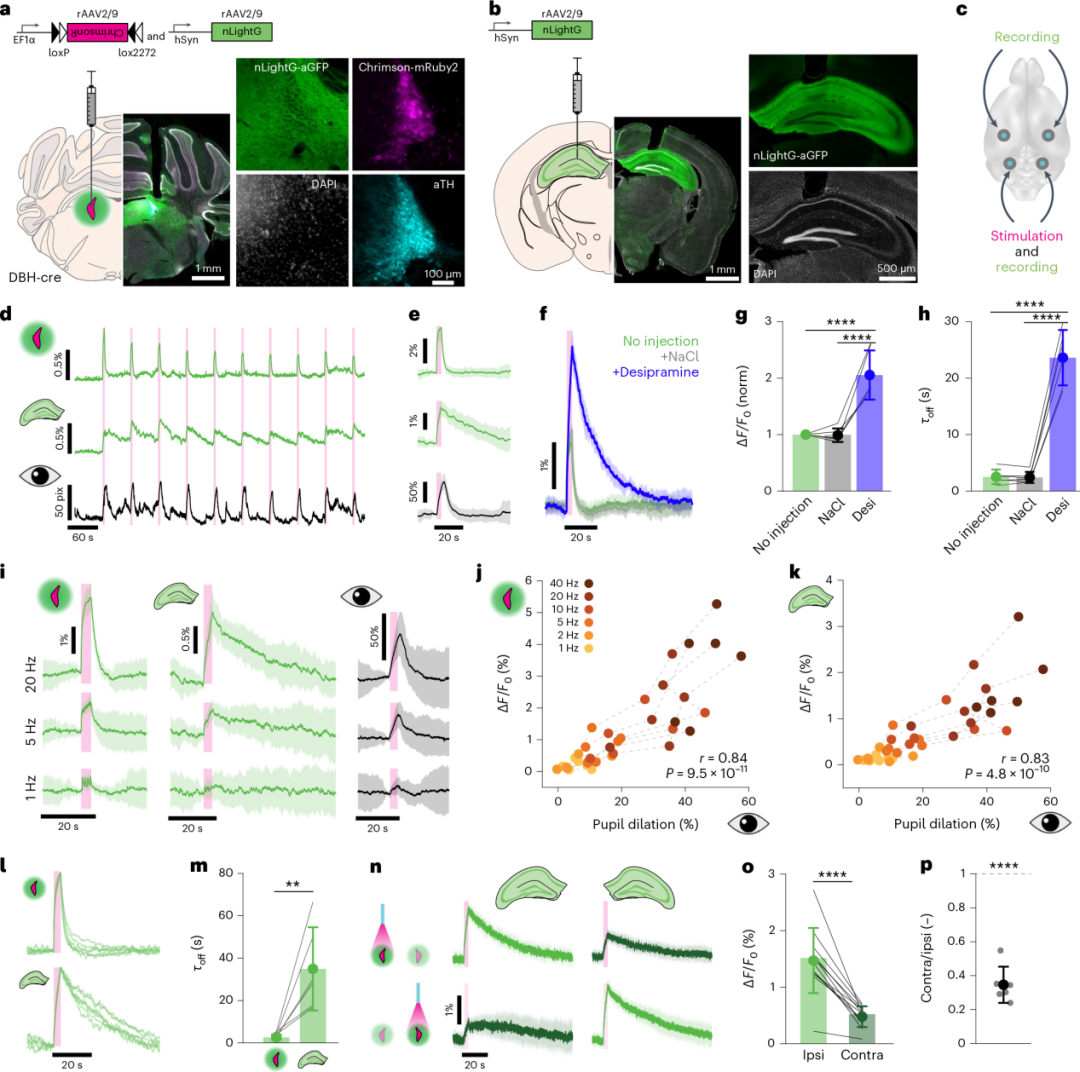
研究者利用高灵敏度探针nLightG,通过光纤光度法在双脑区同步检测光遗传诱发的NE释放。在DBH-Cre小鼠的双侧背侧海马(dHPC)注射rAAV2/9.hSynapsin1.nLightG,LC区共注射rAAV2/9.hSynapsin1.nLightG与rAAV2/9.hSynapsin1.DIO.ChrimsonR-mRuby2。采用595 nm光刺激LC(4 s脉冲串,40 Hz、20 ms脉宽,光纤末端功率10 mW),可在LC与dHPC中同步诱发NE信号;同时瞳孔直径随光刺激快速增大,可作为LC激活的另一指标。
为明确LC内NE重摄取机制对nLightG信号的作用,研究人员经腹腔注射Sal或NE转运体(NET)抑制剂地昔帕明后重复记录。Sal未改变nLightG响应特征,而地昔帕明可提升信号幅度并减慢其衰减动力学,证实nLightG响应依赖胞外NE。
随后探究光遗传激活LC的不同刺激频率,对LC、dHPC nLightG信号及瞳孔扩张的影响。刺激频率低至1 Hz时,LC区即可检测到nLightG信号;随光刺激频率升高,两脑区nLightG信号与瞳孔扩张均呈显著正线性相关。40 Hz刺激下,dHPC的nLightG信号衰减(τoff=37.3±21 s)远慢于LC(τoff=2.8±1.3 s),推测反映了局部NE重摄取机制的密度或功能差异。
最后利用nLightG探究dHPC NE能神经支配的偏侧化特征:单侧LC刺激可高效诱导同侧dHPC的NE释放,且同侧光遗传诱发的dHPC-nLightG信号约为对侧的3倍。
图6.利用nLightG对光遗传学诱导的NE释放进行在体双位点记录
5.dHPC NE释放的双光子成像
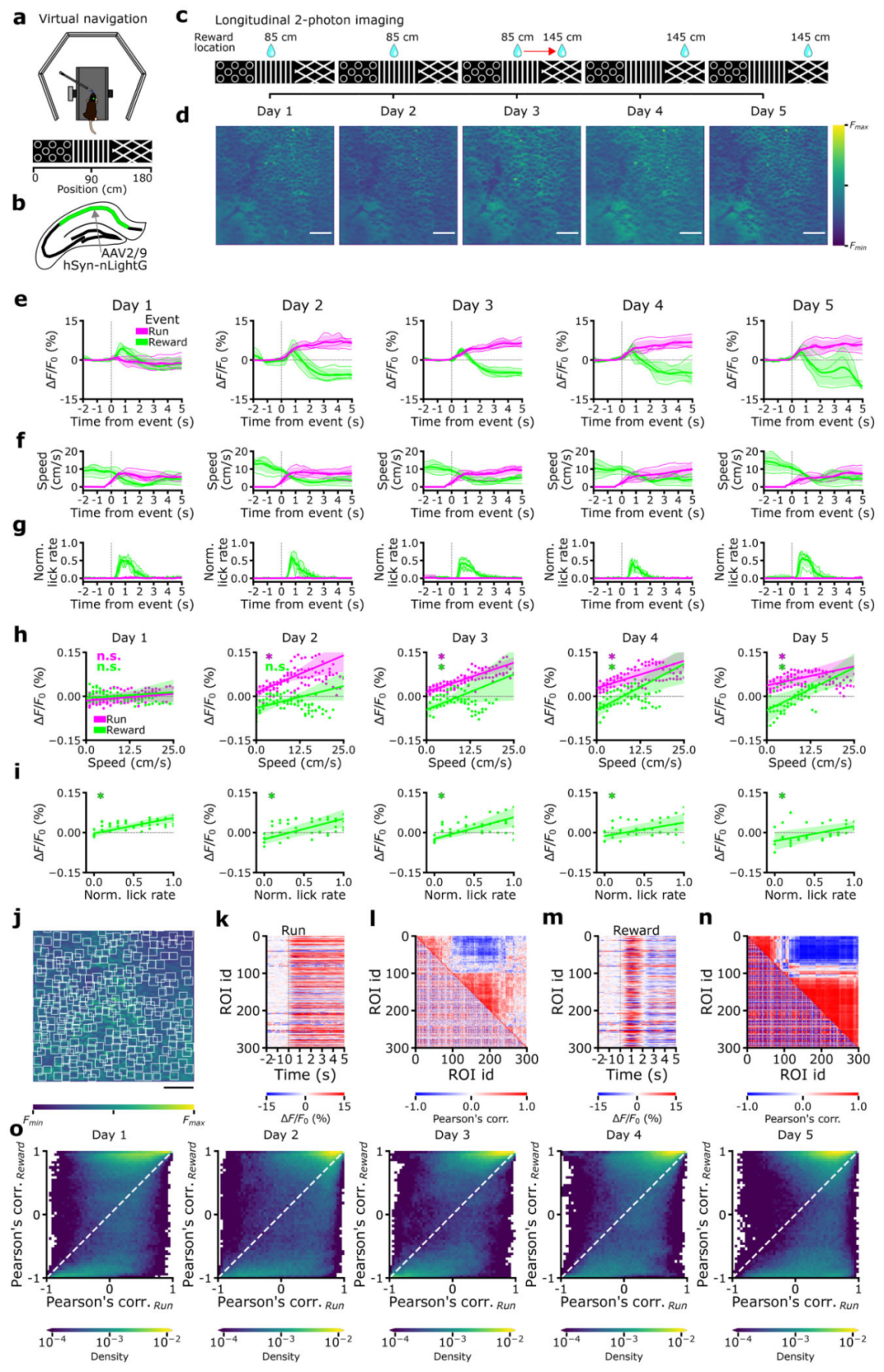
接下来,研究人员验证nLightG能否结合双光子激发,实现在体高空间分辨率的NE释放成像。在小鼠海马CA1区表达nLightG,并通过慢性光学窗,利用双光子显微镜对在虚拟通道中活动的清醒头部固定小鼠进行成像(n=4)。小鼠在通道固定位置获得水奖励,连续 5 天每日成像 1 次,且保持同一视野(FOV)。
已有研究显示LC投射神经元活性在运动及奖赏给予时更高,因此作者提出假设:nLightG信号与运动、奖赏呈正相关。以小鼠开始运动为时间点,对全FOV进行nLightG信号的事件触发平均分析(品红色):记录第1天,小鼠初始运动时nLightG信号与基线相近;而在第2-5天,运动后信号较基线显著升高;5天记录中,小鼠运动速度变化趋势基本一致;仅在第2-5天(第1天无此现象),nLightG信号幅度与运动速度呈正相关。为排除运动伪影,研究人员计算结构相似度(用于评估单帧图像相对于整个成像时间序列平均投影的结构信息变化),结果显示在nLightG信号发生变化的时间窗内,结构相似度保持恒定;对nLightG信号曲线进行时间重排后,原先观察到的信号正向偏移消失。
以小鼠抵达奖赏位置为时间节点,对全FOV nLightG信号进行事件触发平均分析(绿色):在所有记录天数中,nLightG信号均较基线呈一过性升高,随后回落。小鼠抵达奖赏位置后,舔舐频率升高,运动速度较基线降低。在全部记录天数中,nLightG信号幅度与舔舐频率呈正相关;第3-5天,信号幅度与运动速度呈正相关。在nLightG信号变化的对应时间窗内,结构相似度保持稳定;以奖赏位置触发时间为基准对nLightG信号曲线进行时间重排后,原有的信号变化消失。
最后,采用机器学习算法将FOV分割为以推定细胞为中心、经解剖学定位的感兴趣区(ROI)。分别以小鼠运动起始、抵达奖赏位置为时间节点,提取各ROI的nLightG事件触发平均信号;计算ROI配对间的皮尔逊相关系数,并构建互相关矩阵。在不同个体小鼠中,同一ROI配对在运动与奖赏两种行为状态下的皮尔逊相关系数存在差异,提示海马局部区域配对间的NE信号在不同行为条件下呈现差异化相关。
综上,本研究结果证实,nLightG探针结合双光子显微成像技术,可在清醒头部固定小鼠的海马中,实时成像由运动及奖赏位置调控的NE动态变化。
图7.利用nLightG对清醒行为小鼠的NE信号进行双光子成像
总结
nLightG在体NE检测的成功应用为后续研究提供了诸多方向:其一,凭借其药理学特性,nLightG可用于解析临床常用α2-AR激动剂与拮抗剂对在体行为诱发NE释放的影响,而GRABNE1m无法实现;其二,nLightG具备快速动力学特性,可精准解析不同条件对NE动态的影响,如在动物自然行为或光遗传刺激下,研究抗抑郁药、精神兴奋药等临床相关药物及基因操控的作用;其三,nLightG兼容双光子成像,可用于解析此前尚未探索的皮层及皮层下脑区NE信号的时空特征。综上,本研究开发的NE探针,极大完善了神经技术工具库,为高时空分辨率研究NE系统的生理功能提供了关键支撑。
本研究结果显示,相较于GRABNE1m,nLightG与nLightR对NE的选择性均优于DA;但在脑片灌注高浓度(50 μM)DA时,两种探针均产生可检测的响应。这提示,若在DA能神经支配密集的脑区(如基底神经节)使用此类探针,需通过严谨的实验设计区分这两种儿茶酚胺信号。
光纤光度记录的一个潜在局限是易受动物运动或血流动力学干扰产生伪影,这类伪影通常会同步影响405 nm与470 nm激发的荧光信号。为解决该问题,本研究采用双波长进行光度记录,以405 nm作为对照通道。对比两种波长的信号曲线发现,仅470 nm通道可检测到光遗传诱发的nLightG响应,405 nm通道无此响应。因此,光纤光度实验中检测到的信号为nLightG特异性响应。
双光子功能成像实验中,虽未开展功能缺失验证(如配体不敏感型nLightG),但结构相似度分析与nLightG信号曲线时间重排分析均有力证明,所观测到的nLightG信号并非运动相关伪影。
2026年2月26日,Tommaso Patriarchi教授团队开发出新一代绿色(nLightG2)与红色(nLightR2)基因编码NE荧光探针。经系统对比验证,两款探针较初代在亮度、动态范围、灵敏度及特异性上均显著提升。借助双色光纤光度法,nLightG2与nLightR2可精准解析睡眠进程中LC神经元活动与NE释放的时序耦合关系,并检测恐惧学习时基底外侧杏仁核(BLA)内NE释放与局部钙活动的协同变化。nLightR2可通过双色双光子成像,在虚拟导航中同步记录海马CA1区NE释放与星形胶质细胞钙信号;nLightG2则可通过双光子成像,在清醒小鼠视觉皮层(VC)中捕捉时空离散的微域级NE信号,为解析NE神经调控的时空机制提供核心工具。
我司可提供nLightG、nLightG2及nLightR2病毒产品,列表如下:

扫码添加客服
更多产品及详情欢迎咨询!


市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK