2026-03-30 阅读量:145
近十年间,国际神经科学领域迎来两项突破性技术创新:美国杜克大学团队开发的Split-TurboID邻近标记技术于2020年发表于《Nature》,加州大学洛杉矶分校(UCLA)Baljit S. Khakh教授实验室研发的NAPA光学邻近检测技术(Optical Neuron-Astrocyte Proximity Assay)于2018年发表于《Neuron》,均为领域内标志性成果。两项技术分别从分子组成和空间距离两个核心维度,首次实现活体脑组织内星形胶质细胞-神经元突触界面的精准解析,突破了该领域长期存在的技术瓶颈,为阐释突触调控机制与神经系统疾病病理进程提供了全新研究范式。
研究背景:三联突触的核心科学问题亟待破解
星形胶质细胞的突触周足突与神经元突触共同构成中枢神经系统的三联突触,是神经信号传递、发育调控与稳态维持的核心功能单元。长期以来,该领域存在两大关键科学难题:一是突触间隙的分子组成难以在活体状态下精准捕获,二是星形胶质细胞与突触间的纳米尺度空间互作无法动态观测。传统研究手段存在明显局限:或依赖体外细胞培养(脱离生理微环境),或具有细胞毒性(如HRP标记技术),或空间分辨率不足(常规光学成像),始终无法同时满足活体兼容、细胞特异性、高分辨率的研究要求。杜克大学与UCLA团队分别从分子标记捕获和空间距离测量两大方向攻关,所开发的两类技术形成高度互补,为三联突触研究提供了关键工具支撑。
核心突破一:Split-TurboID——活体捕获突触间隙分子的“精准捕捞器”
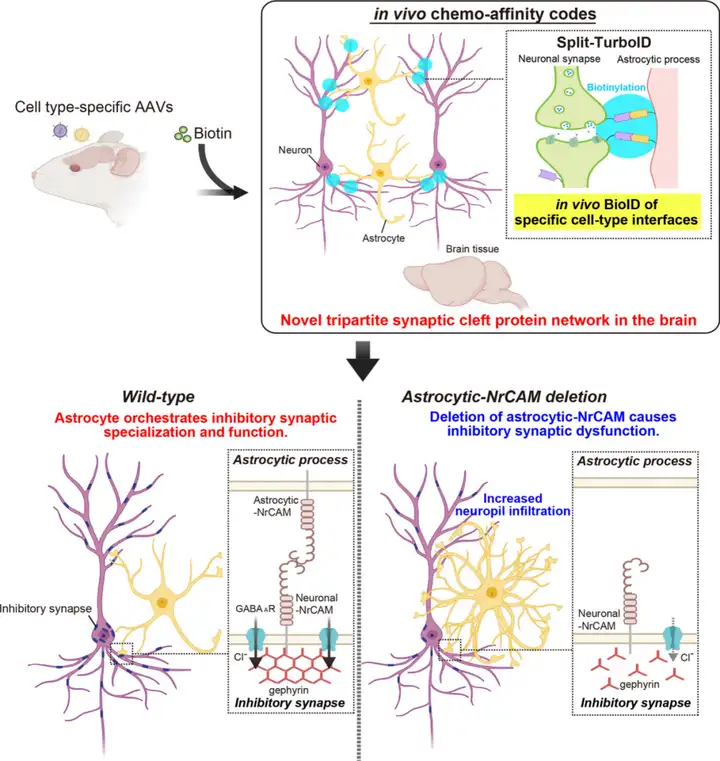
杜克大学团队开发的Split-TurboID是基于邻近依赖性生物素标记的前沿技术,核心优势为在活体水平特异性捕获星形胶质细胞-神经元突触间隙的蛋白质组,其工作原理围绕片段互补+细胞靶向展开:
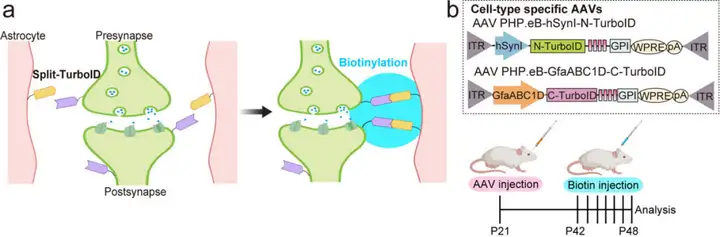
1.酶拆分与惰性设计:将高活性生物素连接酶TurboID拆分为N端(N-TurboID)与C端(C-TurboID)两个无催化活性片段,单独表达时无法启动生物素化反应,从根源避免非特异性标记。
2.细胞特异性靶向递送:借助腺相关病毒(AAV)载体与特异性启动子,将N-TurboID靶向表达于神经元细胞膜外表面,C-TurboID靶向表达于星形胶质细胞细胞膜外表面,实现跨细胞的精准分定位。
3.接触依赖的酶活性重构:仅当星形胶质细胞突起与神经元突触紧密接触时,两个无活性片段才会空间靠近并重组,恢复TurboID的生物素连接酶活性;非接触区域始终保持惰性,确保标记高度特异。
4.活体生物素化与蛋白质组鉴定:对小鼠连续7天皮下注射生物素(TurboID底物)后,重构酶可催化生物素与突触间隙10 nm范围内的互作蛋白发生共价结合;后续通过链霉亲和素纯化结合质谱分析,实现界面分子的高通量鉴定。
该技术成功捕获关键黏附分子NrCAM,并证实其通过星形胶质细胞与神经元的同源跨细胞互作,特异性调控抑制性突触的形成与功能,填补了星形胶质细胞调控突触功能的分子机制空白。
文章模式图
图1. Split-TurboID技术概览
核心突破二:NAPA——纳米尺度测量互作距离的“光学标尺”
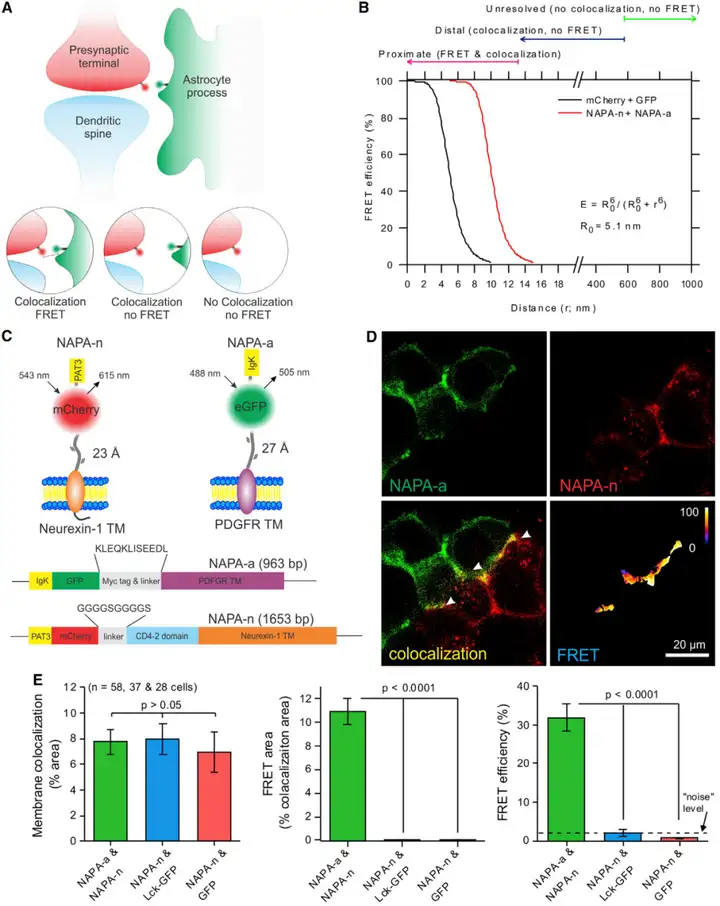
UCLA团队研发的神经元-星形胶质细胞邻近分析技术(NAPA,Neuron-Astrocyte Proximity Assay),基于荧光共振能量转移(FRET)原理,当供体的发射光谱与受体的吸收光谱重叠时,会发生FRET;能量转移效率由光谱重叠程度、供体量子产率、供体与受体偶极子的相对取向及供体-受体间距离(r)共同决定。核心优势为实时动态观测活体状态下星形胶质细胞与突触的空间互作距离,工作原理聚焦特异性探针+距离依赖信号:
1.双探针靶向构建:设计两种基因编码探针——NAPA-a(星形胶质细胞探针)与NAPA-n(突触探针)。NAPA-a以PDGFR跨膜结构域锚定星形胶质细胞膜外,携带GFP(FRET供体);NAPA-n以突触前膜特异性蛋白Neurexin-1为靶向序列(跨膜结构域和胞内C端结构域),携带mCherry(FRET受体),确保探针仅暴露于细胞外间隙。
2.细胞特异性高效表达:通过星形胶质细胞特异性启动子(GfaABC1D)与神经元特异性启动子(hSynapsin-1)分别驱动探针表达,AAV介导的靶向效率在星形胶质细胞中约90%、神经元中达80%,且无交叉表达干扰。
3.FRET信号的距离依赖性解析:优化探针使GFP与mCherry的FRET特征距离(R0,即能量转移效率为50%时的距离)为5.1 nm,表明在最大效率的5%至95%范围内,FRET对10 nm内的距离变化敏感:距离≤10 nm(紧密接触)时呈现荧光共定位并产生FRET信号;10-600 nm(中等邻近)时呈现荧光共定位但无FRET信号;>600 nm(无接触)时无信号关联,实现三重距离尺度的精准区分。
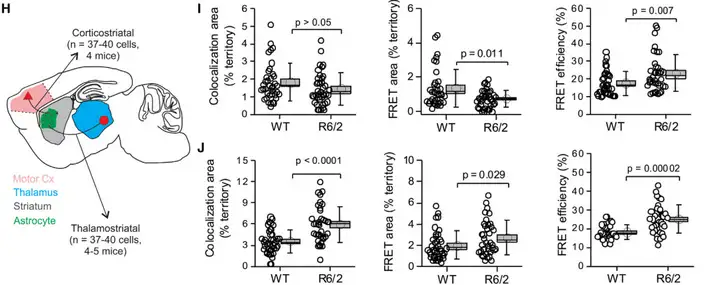
借助该技术,团队首次揭示纹状体星形胶质细胞与不同来源突触的通路特异性互作模式,并在亨廷顿病(HD)模型中发现早期星形胶质细胞-突触接触异常,为疾病早期诊断提供新型细胞病理标志物。
图2. NAPA技术评估星形胶质细胞-突触互作
图3. R6/2 HD模型小鼠中邻近性发生改变。R6/2小鼠中,紧邻皮质传入突触的星形胶质细胞突起数量减少,而紧邻丘脑传入突触的突起数量增加。(皮质与丘脑通路的上述改变早于突触前vGLUT1和vGLUT2免疫染色信号的丢失)
技术互补:全方位解析细胞间互作的“黄金组合”
Split-TurboID与NAPA虽原理不同,却形成高度互补:Split-TurboID聚焦分子组成,解决“突触间隙存在哪些互作蛋白”的问题,适用于高通量蛋白质组学筛选;NAPA聚焦空间距离,回答“细胞间如何动态接触”的问题,适用于活体动态成像。二者均具备活体兼容、细胞特异、无细胞毒性的核心优势,共同攻克了传统技术无法同时解析“分子组成”与“空间关系”的技术瓶颈。
参考文献:
1)Takano T, Wallace JT, Baldwin KT, et al. Chemico-genetic discovery of astrocytic control of inhibition in vivo. Nature. 2020;588(7837):296-302. doi:10.1038/s41586-020-2926-0
2)Octeau JC, Chai H, Jiang R, Bonanno SL, Martin KC, Khakh BS. An Optical Neuron-Astrocyte Proximity Assay at Synaptic Distance Scales. Neuron. 2018;98(1):49-66.e9. doi:10.1016/j.neuron.2018.03.003
我司可提供Split-TurboID、NAPA技术适配AAV载体,列表如下:

扫码添加客服
更多产品及详情欢迎咨询!


市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK