2026-04-14 阅读量:185
疾病简介
甲状腺功能亢进症(简称甲亢)是因甲状腺合成与释放过多甲状腺激素,引发代谢亢进、交感神经兴奋等高代谢症状的常见内分泌疾病,不仅严重影响患者的生活质量,还可诱发甲状腺危象、心房颤动、心力衰竭等致命并发症。在众多病因中,毒性弥漫性甲状腺肿(Graves’disease,GD)是导致甲亢最主要的原因,约占甲亢病例的60%-80%,其在人群中的总患病率约为1.0%-1.5%,且呈现显著的女性高发特征:据估算,约3%的女性和0.5%的男性在其一生中会患上GD[1]。
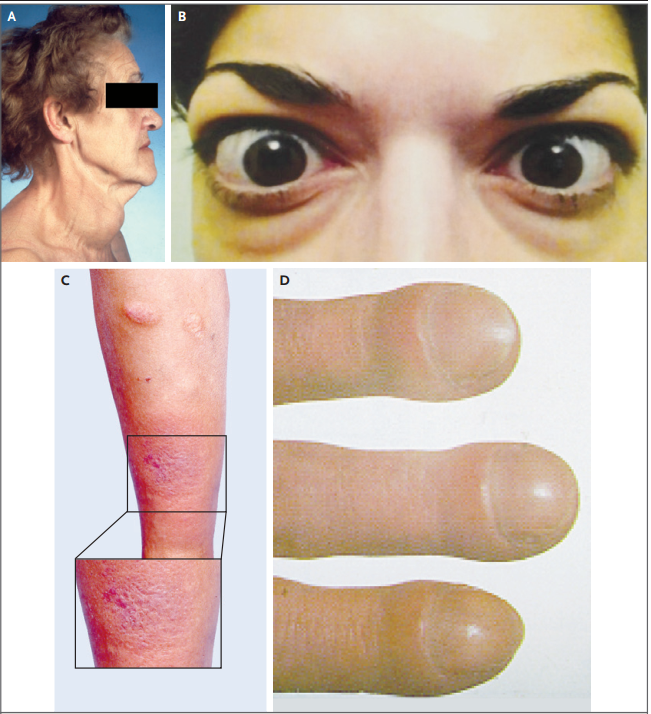
GD作为一种针对甲状腺的器官特异性自身免疫病,以弥漫性甲状腺肿、浸润性突眼和胫前黏液性水肿为典型临床表现,现有的抗甲状腺药物、放射性碘及手术治疗均存在局限性,如疗程长、复发率高或需终身替代治疗等[2-3]。因此,构建能够精准模拟人类GD特征的动物模型,对于深入解析其发病机制、研发安全有效的新型靶向治疗手段具有重要的科学价值与临床转化意义。
图1. GD的临床表现(Smith, Terry J et al., The New England journal of medicine, 2016.)
发病机制
GD的发病核心在于机体对自身促甲状腺激素受体(TSHR)的免疫耐受被打破[4]。
1.关键自身抗原——TSHR A亚基
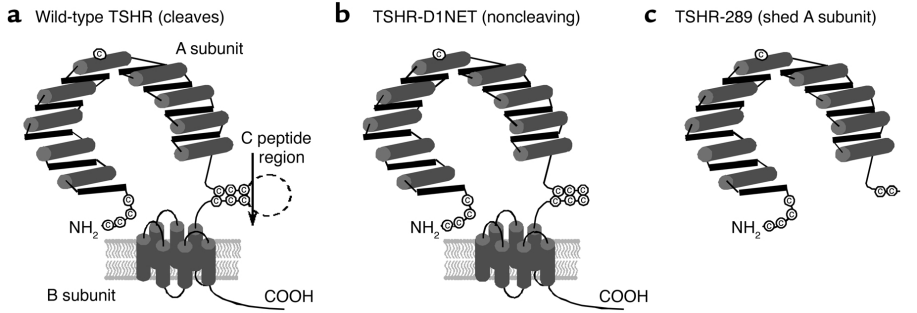
TSHR是位于甲状腺滤泡细胞膜上的G蛋白偶联受体。其胞外结构域在翻译后会经历分子内蛋白水解切割,产生由二硫键连接的A亚基(胞外端)和B亚基(跨膜端)[4-5]。在病理条件下,A亚基通过二硫键溶解作用从受体复合物上脱落并释放,这种可溶性的A亚基被认为是诱发自身免疫反应的关键“导火索”[5-6]。
2.致病性抗体——TSAb
脱落的A亚基被免疫系统识别,刺激B细胞分化为浆细胞,进而产生促甲状腺激素受体抗体(TRAb)。其中,刺激性抗体(TSAb)与TSHR结合后,模拟促甲状腺激素(TSH)的生理效应,持续激活cAMP通路,刺激甲状腺滤泡细胞增生并过度合成、分泌甲状腺激素,从而导致甲亢[4]。
3.A亚基是更优的免疫原
研究表明,与TSHR全长相比,A亚基具有更强的免疫原性。使用表达A亚基的腺病毒(Ad-TSHR289),能更有效地诱导小鼠产生TSAb,其成模率和甲亢严重程度远高于表达全长TSHR的Ad[7]。
图2. TSHR结构示意图:野生型亚基切割、低切割突变体(TSHR-D1NET)与游离A亚基模拟物(TSHR-289)的对比(Chen, Chun-Rong et al., The Journal of clinical investigation, 2003.)
GD造模
为了研究GD,学界探索了多种动物模型构建方法。早期造模方法普遍存在操作繁琐、成模率低、稳定性差等问题,如采用表达TSHR的细胞或重组TSHR蛋白进行免疫等[8]。而腺病毒(AdV)因其宿主范围广、可在体内高效表达外源蛋白等优点,成为GD造模的理想载体[9]。其中,表达人TSHR A亚基(氨基酸1-289)的重组腺病毒(Ad-TSHR289)是目前构建GD动物模型公认的成熟、有效工具;且研究表明,采用长期免疫方案,该工具亦可成功诱导Graves眼病(GO)的病理特征[10]。
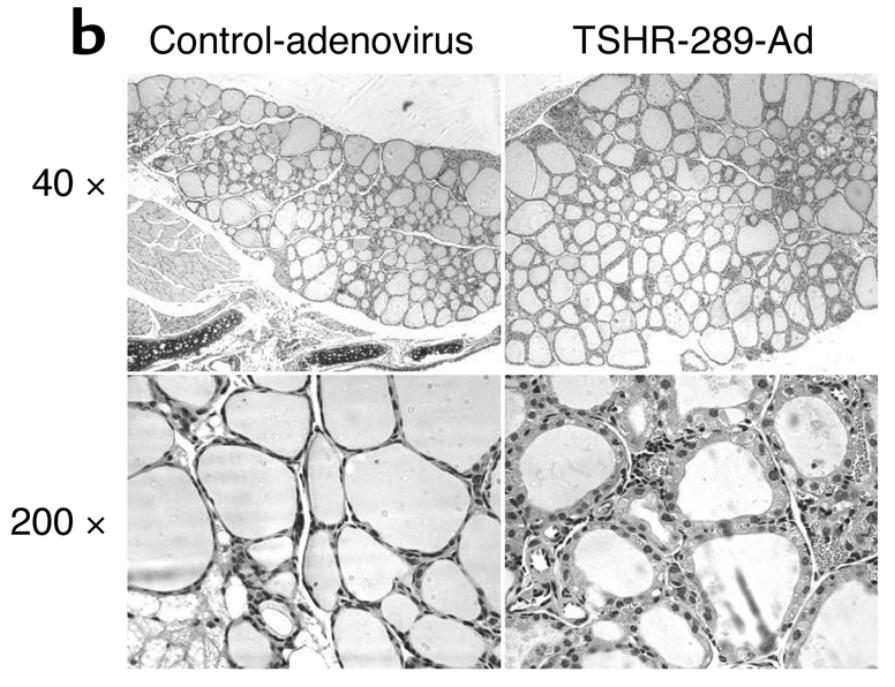
该模型常选用BALB/c小鼠(其天然具有Th2偏向性免疫背景,更易诱导刺激性抗体产生),经肌肉注射免疫后,AdV可介导TSHR A亚基在局部组织高效表达,进而打破机体对TSHR的免疫耐受,诱导产生高活性TSAb;后者与甲状腺滤泡细胞膜上的TSHR结合后,激活胞内cAMP信号通路,最终引发甲状腺肿大、甲状腺激素(FT3、FT4)分泌异常及类似人类GD的典型病理改变[7, 9]。
图3. 对照组与Ad-TSHR289免疫组小鼠甲状腺组织学比较(Chen, Chun-Rong et al., The Journal of clinical investigation, 2003.)
Ad-TSHR289应用场景
1.GD发病机制与免疫分子网络研究
2.GO的病理模拟与机制探索
3.创新药物的筛选与药效评价
4.抗原特异性免疫耐受治疗研发
5.遗传易感与环境因素研究
•••
应用案例
该研究聚焦环状RNA(circRNA)在GD免疫发病机制中的作用,采用Ad-TSHR289构建GD小鼠模型,结合细胞实验揭示circPHF16通过竞争性结合miR-378a-3p激活IL6ST信号轴,进而调控白细胞介素-17A(IL-17A)分泌的深层机制[11]。
关键方法
1.造模方案:对6-8周龄雌性BALB/c小鼠进行肌肉注射免疫,每3周1次,共3次,每次注射50 μL的Ad-TSHR289(病毒滴度1×10¹⁰ PFU/mL),末次免疫1周后收集血清和甲状腺组织进行评估。
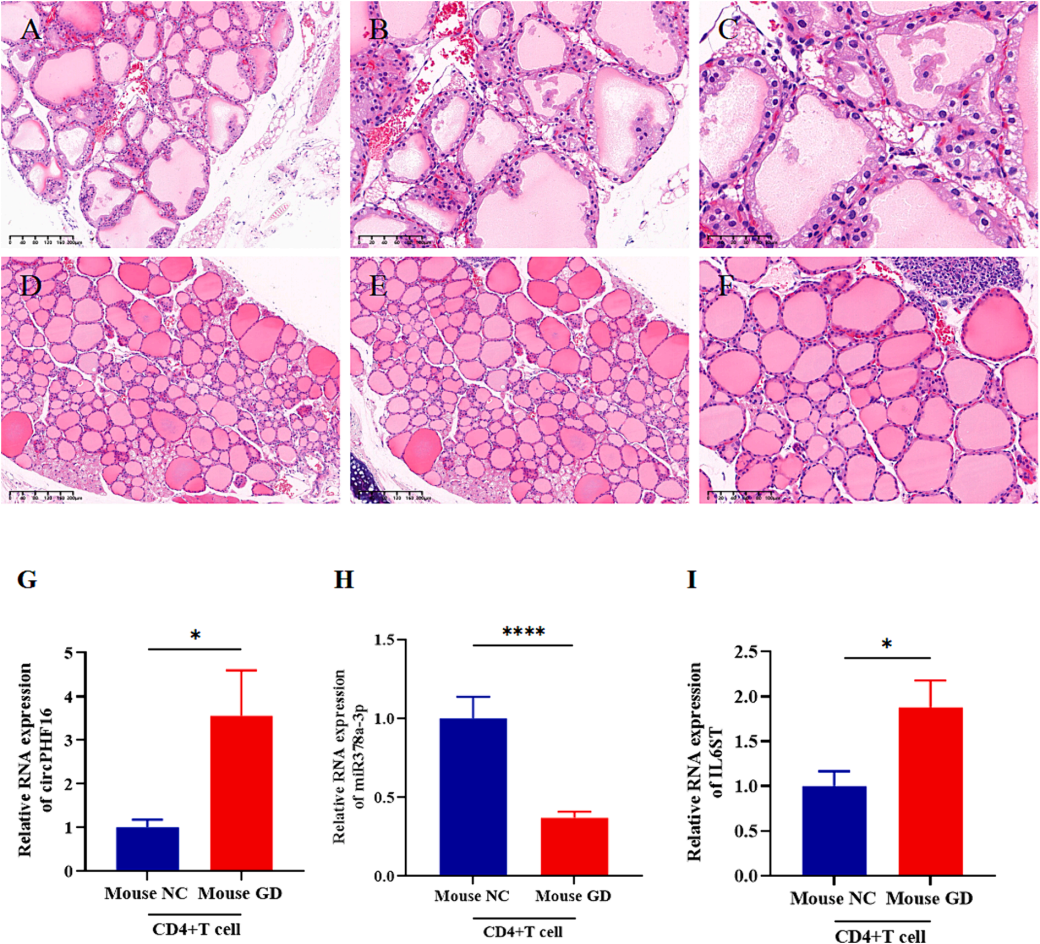
2.模型验证:造模成功率达80%,模型小鼠血清FT3、FT4、TRAb水平显著升高,甲状腺组织呈现肉眼可见的肿大,以及滤泡增生、滤泡上皮细胞肥大、胶质减少及间质淋巴细胞浸润等典型GD病理特征。
3.机制探究:通过RT-qPCR、ELISA、双荧光素酶报告基因实验等技术,结合GD患者外周血单核细胞(PBMCs)和Jurkat细胞(人T细胞白血病细胞系)实验,验证circPHF16/miR-378a-3p/IL6ST调控轴的功能。
图4. GD小鼠模型表征及circPHF16竞争性内源RNA(ceRNA)轴组分的调控特征(Jiang, Zhengrong et al., Cytokine, 2024.)
核心结果
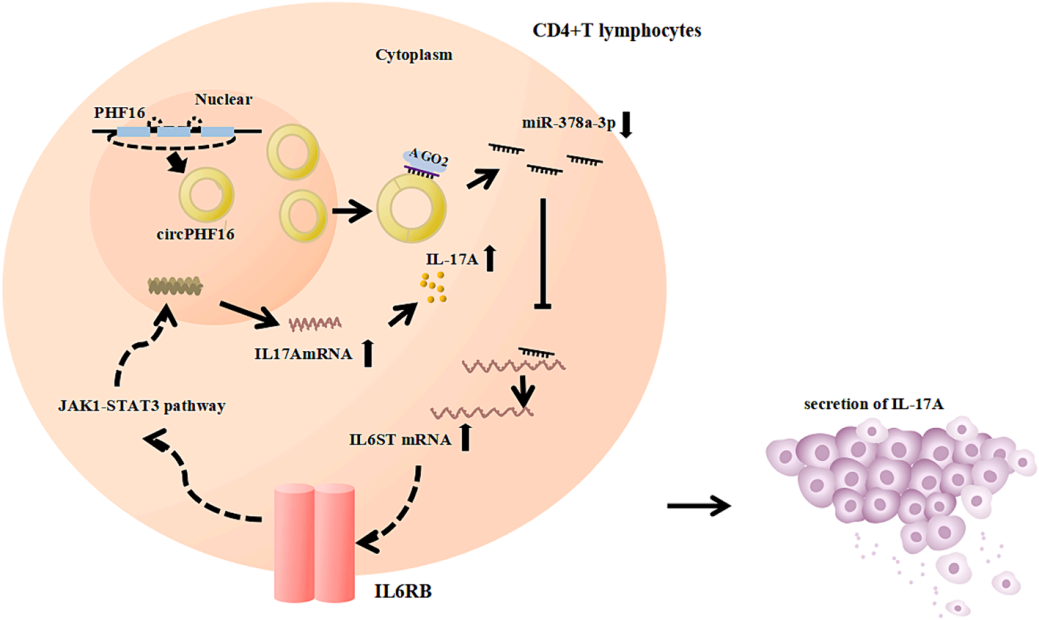
动物模型中,GD小鼠脾CD4⁺ T淋巴细胞中circPHF16和IL6ST mRNA表达上调,miR-378a-3p表达下调;证实circPHF16通过“海绵吸附”miR-378a-3p,解除其对IL6ST的抑制,进而激活JAK1-STAT3通路,最终促进致病性IL-17A的分泌。
图5. GD中circPHF16的分子机制:circPHF16作为ceRNA通过吸附miR-378a-3p调控IL6ST表达(Jiang, Zhengrong et al., Cytokine, 2024.)
研究价值
该研究不仅揭示了circRNA作为ceRNA在GD中的调控作用,同时验证了Ad-TSHR289构建的GD模型在分子机制研究中的可靠性,为GD诊断靶点和治疗策略开发提供了实验基础。
枢密科技特推出重组腺病毒Ad-CMV-TSHR289,作为国际公认的GD模型构建标准化工具,其表达效率高、免疫稳定性好、成模效果确切,可全面支撑GD发病机制研究与临床前药物筛选,欢迎咨询!
参考文献:
[1] Nyström HF, Jansson S, Berg G. Incidence rate and clinical features of hyperthyroidism in a long-term iodine sufficient area of Sweden (Gothenburg) 2003-2005. Clin Endocrinol (Oxf). 2013 May;78(5):768-76. doi: 10.1111/cen.12060. PMID: 23421407.
[2] Kahaly GJ, Bartalena L, Hegedüs L, Leenhardt L, Poppe K, Pearce SH. 2018 European Thyroid Association Guideline for the Management of Graves' Hyperthyroidism. Eur Thyroid J. 2018 Aug;7(4):167-186. doi: 10.1159/000490384. Epub 2018 Jul 25. PMID: 30283735; PMCID: PMC6140607.
[3] Smith TJ, Hegedüs L. Graves' Disease. N Engl J Med. 2016 Oct 20;375(16):1552-1565. doi: 10.1056/NEJMra1510030. PMID: 27797318.
[4] Rapoport B, McLachlan SM. TSH Receptor Cleavage Into Subunits and Shedding of the A-Subunit; A Molecular and Clinical Perspective. Endocr Rev. 2016 Apr;37(2):114-34. doi: 10.1210/er.2015-1098. Epub 2016 Jan 22. PMID: 26799472; PMCID: PMC4823380.
[5] Schwarz-Lauer L, Chazenbalk GD, Mclachlan SM, Ochi Y, Nagayama Y, Rapoport B. Evidence for a simplified view of autoantibody interactions with the thyrotropin receptor. Thyroid. 2002 Feb;12(2):115-20. doi: 10.1089/105072502753522347. PMID: 11916280.
[6] Chen CR, Hubbard PA, Salazar LM, McLachlan SM, Murali R, Rapoport B. Crystal structure of a TSH receptor monoclonal antibody: insight into Graves' disease pathogenesis. Mol Endocrinol. 2015 Jan;29(1):99-107. doi: 10.1210/me.2014-1257. PMID: 25419797; PMCID: PMC4280529.
[7] Chen CR, Pichurin P, Nagayama Y, Latrofa F, Rapoport B, McLachlan SM. The thyrotropin receptor autoantigen in Graves disease is the culprit as well as the victim. J Clin Invest. 2003 Jun;111(12):1897-904. doi: 10.1172/JCI17069. PMID: 12813025; PMCID: PMC161420.
[8] Kaithamana S, Fan J, Osuga Y, Liang SG, Prabhakar BS. Induction of experimental autoimmune Graves' disease in BALB/c mice. J Immunol. 1999 Nov 1;163(9):5157-64. PMID: 10528222.
[9] Nagayama Y, Kita-Furuyama M, Ando T, Nakao K, Mizuguchi H, Hayakawa T, Eguchi K, Niwa M. A novel murine model of Graves' hyperthyroidism with intramuscular injection of adenovirus expressing the thyrotropin receptor. J Immunol. 2002 Mar 15;168(6):2789-94. doi: 10.4049/jimmunol.168.6.2789. PMID: 11884447.
[10] Ungerer M, Faßbender J, Li Z, Münch G, Holthoff HP. Review of Mouse Models of Graves' Disease and Orbitopathy-Novel Treatment by Induction of Tolerance. Clin Rev Allergy Immunol. 2017 Apr;52(2):182-193. doi: 10.1007/s12016-016-8562-7. PMID: 27368808; PMCID: PMC5346423.
[11] Jiang Z, Huang L, Cai H, Bo L, Chen L, Yang X, Huang H. Circular RNA circPHF16 enhances IL-17A expression and secretion by sequestering miR-378a-3p to activate the IL6ST axis in Graves' disease. Cytokine. 2024 Sep;181:156681. doi: 10.1016/j.cyto.2024.156681. Epub 2024 Jul 3. PMID: 38963941.
扫码添加客服
更多产品及详情欢迎咨询!


市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK