2026-03-30 阅读量:172
突触作为神经系统中神经元间信号传递的基本结构单元,其结构可塑性是大脑功能调控的核心基础,与神经发育、环路活性调节及大脑的生理、病理状态密切相关。解析突触的结构动态变化,是理解大脑功能与神经行为的关键环节,但此前该领域的研究仍受限于技术手段的不足。传统研究多通过测量突触后区室树突棘体积、直径等参数分析突触可塑性,但这些方法无法反映突触前区室的变化。近年来发展的基于分裂荧光蛋白(split FPs)的突触可视化技术,虽能标记完整突触,却因FPs片段重构成熟耗时长、结合具有不可逆性,难以实现突触结构动态的实时监测,成为活体研究突触可塑性的重要技术瓶颈。
韩国科学技术院(KAIST)的Won Do Heo团队在Nature Methods(IF=48)发表了题为“Real-time visualization of structural dynamics of synapses in live cells in vivo”的研究成果,开发了一种名为SynapShot的新型突触可视化技术,该技术将二聚化依赖型荧光蛋白(ddFPs)与工程化突触黏附分子相结合,突破了传统技术的不可逆局限,实现了完整突触结构动态的实时、可逆可视化。研究证实,SynapShot可通过绿、红双色配置同时监测两个不同的突触群,且红移型SynapShot与蓝光光遗传学技术高度兼容,能在精准调控神经信号通路的同时,同步监测突触动态。更重要的是,该技术成功实现了对小鼠大脑在初级和高级行为中突触连接结构变化的活体实时监测,为神经科学领域研究突触可塑性与大脑功能、动物行为的关联提供了全新的工具。
枢密科技重磅推出突触可塑性研究革新工具——SynapShot系列病毒产品!突破传统split FPs类工具不可逆结合、无法追踪突触动态的瓶颈,以ddFPs为核心设计,实现突触连接高特异性标记与双向可逆实时监测,适配活细胞、活体双光子成像等主流实验,为神经环路解析、学习记忆机制探索、神经疾病突触病理研究等提供强大工具。选择枢密科技,解锁活体突触动态实时监测新维度!相关产品见文末~
1、SynapShot的开发与验证
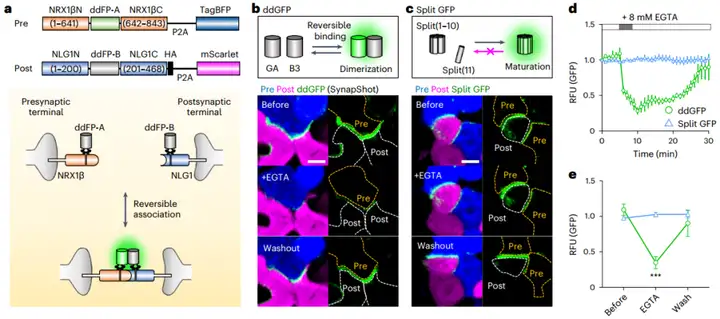
为开发一种能够实时报告突触连接动态的工具,研究者摒弃了传统的不可逆split FPs,转而采用了ddFPs。ddFPs由两个淬灭的FP衍生单体(拷贝A和拷贝B)组成,只有当二者发生异源二聚化时,拷贝A中的发色团才能被激活,发出明亮的荧光。这种结合是可逆的,因此研究者推测其可用于报告突触连接的动态变化。
研究团队以现有基于split FPs的SynView技术和哺乳动物跨突触绿色荧光蛋白(GFP)重构(mGRASP)技术为骨架,将ddGFP的拷贝A(GA)和拷贝B(B1或B3)分别插入到突触前分子神经连接蛋白1β(NRX1β)和突触后分子神经连接蛋白配体1(NLG1)的内部位点,构建了Pre-SynapShot和Post-SynapShot。进一步在人胚肾293T(HEK293T)细胞中分别表达这两种组分,随后将两种细胞共培养,从而筛选出了荧光信号最强的组合——SynView骨架下GA-NRX1β与B3-NLG1的组合、mGRASP骨架下GA-NRX1β与B1-NLG1的组合。
关键的验证实验在于,当使用EGTA螯合细胞外钙离子,使依赖钙离子的NRX-NLG复合物解离时,基于ddFPs的SynapShot荧光信号显著减弱,并在洗脱EGTA后完全恢复。相比之下,基于传统split FPs的传感器在相同处理下信号没有明显变化。这一结果直接证明了SynapShot能够可逆地报告NRX和NLG的相互作用,即突触连接的状态。此外,在原代培养的海马神经元中,SynapShot的绿色荧光信号特异性地出现在突触接触点,并能与内源性兴奋性和抑制性突触前、突触后标志物共定位,表明其能准确标记功能性突触。
图1. 利用SynapShot可视化可逆的突触连接
2. 利用SynapShot监测完整突触的结构动态
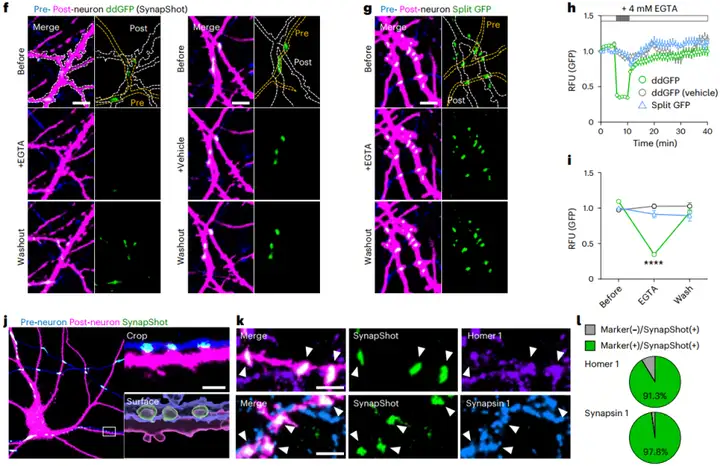
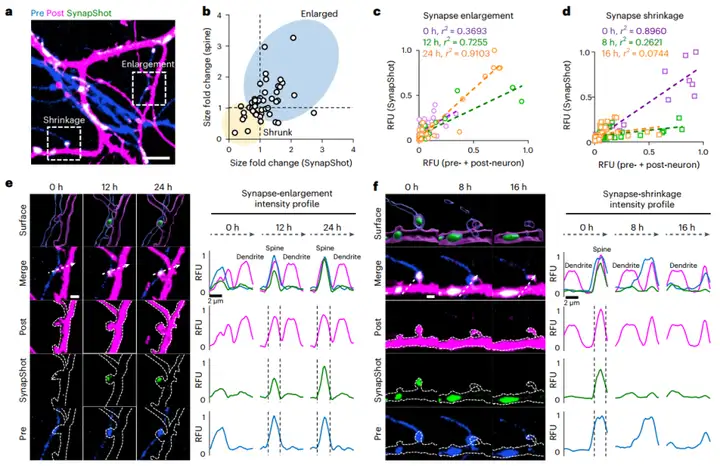
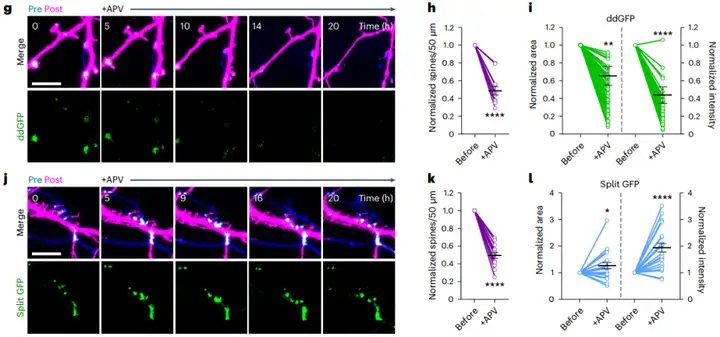
在证实了SynapShot的可逆性后,研究者进一步探究其是否能反映突触的结构变化。通过对培养神经元进行长达24小时的延时成像,他们发现树突棘的大小变化与SynapShot信号强度呈正相关:树突棘增大时信号增强,反之则信号减弱。为了模拟生理条件下的突触可塑性,他们使用NMDA受体拮抗剂APV处理神经元。结果显示,APV处理导致树突棘收缩,同时SynapShot信号也显著降低;而基于split GFP的突触标记工具的荧光信号在APV处理后保持稳定,甚至有所增强。这再次证实了SynapShot具备实时追踪与功能相关的完整突触结构变化的独特优势。
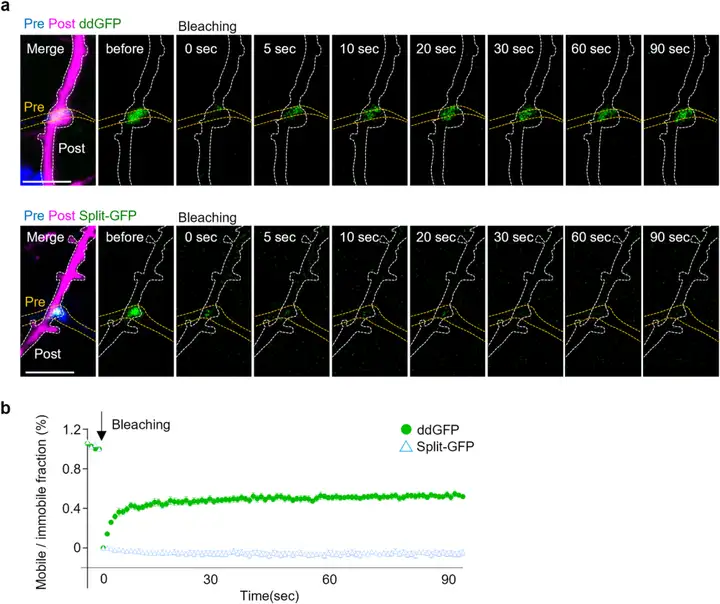
此外,光漂白后荧光恢复实验显示,SynapShot信号在单个突触光漂白后约30秒内即可恢复约50%,表明其分子交换迅速。相比之下,SynView信号几乎没有恢复,这归因于其split GFP片段的不可逆结合或漫长的成熟时间。
图2. 利用SynapShot监测完整突触的结构动态
图3. 单个突触中ddFP或split GFP信号里报告分子交换的检测
3. 双色SynapShot的构建及与光遗传学技术的兼容性
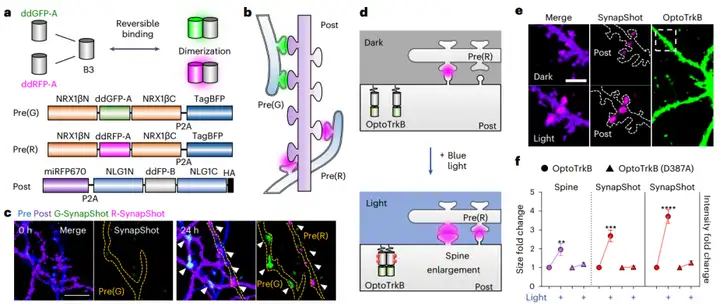
ddFPs的另一个显著优势是,其绿色(ddGFP)和红色(ddRFP)版本可以共用相同的拷贝B(B3)。利用这一特性,研究团队在绿色版本SynapShot(G-SynapShot)的基础上开发了红色版本的SynapShot(R-SynapShot)。通过将G-SynapShot和R-SynapShot的突触前组件(Pre-SynapShot)分别表达在不同的突触前神经元中,并将通用的Post-SynapShot表达在突触后神经元中,他们成功地在同一突触后神经元的树突上,同时观察到了由不同神经元突触前输入形成的绿色和红色荧光斑点。这一双色配置极大拓展了该平台的适用性,使得研究者能够追踪单个神经元上来自不同输入通路的突触动态。
由于红色荧光蛋白的激发光谱与蓝光激活的光遗传学工具(如OptoTrkB)不重叠,研究者将R-SynapShot与OptoTrkB共表达于神经元中,以研究突触后神经元内源性信号通路激活对突触结构的影响。结果显示,蓝光刺激OptoTrkB从而激活脑源性神经营养因子(BDNF)信号通路后,树突棘大小和R-SynapShot信号强度均显著增加;而对光不敏感的OptoTrkB突变体(CRY2D387A)进行刺激后,树突棘尺寸和荧光信号强度均未发生显著变化。这证明了R-SynapShot可与光遗传学技术完美兼容,为在精确控制特定信号通路的同时,实时观察突触动态提供了可能。
图4. 双色SynapShot的构建及与光遗传学技术的兼容性
4. 在行为小鼠中实现实时突触动态的监测
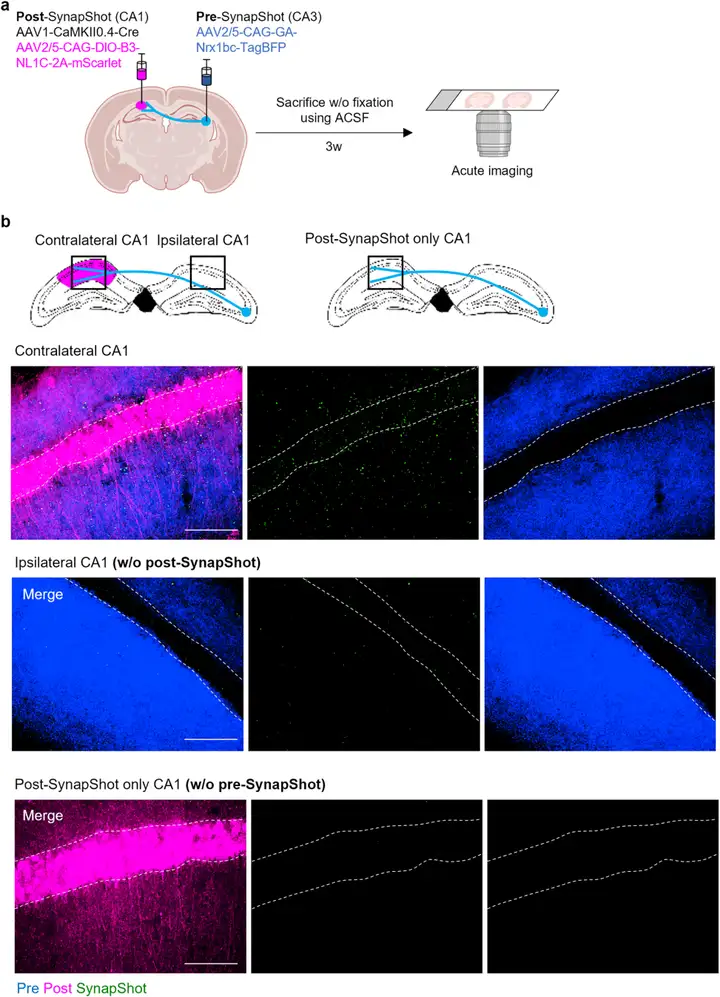
为验证SynapShot在活体动物中的适用性,研究者将SynapShot系统包装到腺相关病毒(AAV),并首先在海马CA3-CA1环路进行了初步验证。他们将Pre-SynapShot病毒注射于小鼠海马CA3神经元(其轴突投射至对侧CA1区),并将Cre依赖的Post-SynapShot病毒注射于对侧CA1神经元。通过急性脑片成像,他们在对侧CA1区检测到特异性SynapShot荧光信号,而无Post-SynapShot表达的同侧CA1区、仅表达Post-SynapShot的CA1区均未检测到荧光信号,初步证实了该系统在体内的有效性。
图5. CA3-CA1环路中的SynapShot标记
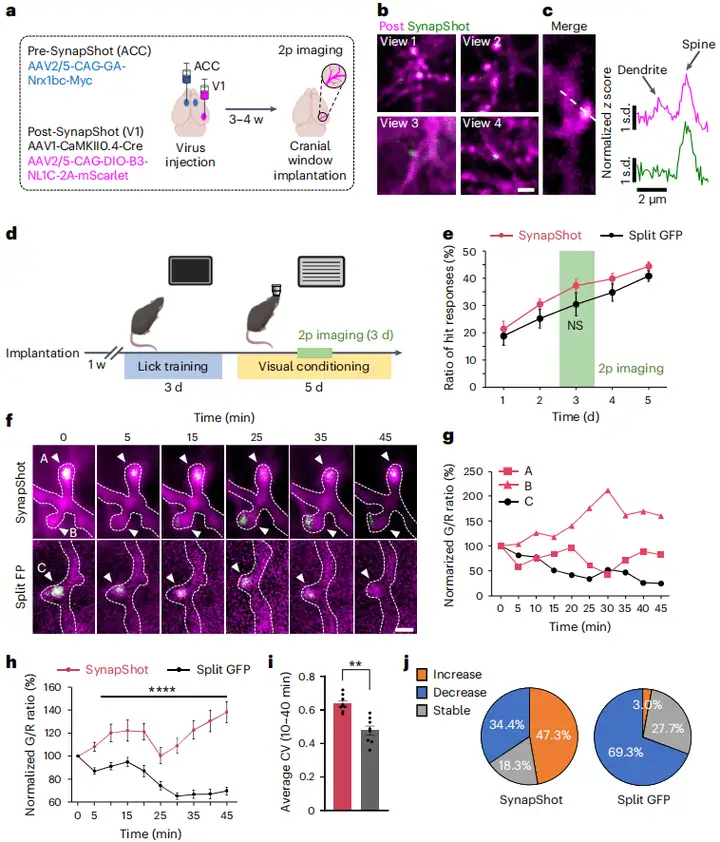
随后,研究团队将该技术应用于前扣带回皮层(ACC)-初级视觉皮层(V1)环路,进一步验证SynapShot在活体中的检测效果。他们将Pre-SynapShot病毒注射于ACC神经元,并将Cre依赖的Post-SynapShot病毒注射于V1神经元。通过双光子成像,他们在清醒小鼠的V1神经元树突上观察到了稀疏分布的SynapShot荧光信号,且信号仅特异性定位于树突棘头部,证实了ACC-V1环路中存在特异性突触连接。此外,在视觉辨别学习任务中,他们比较了SynapShot和mGRASP在监测学习相关突触变化时的表现。结果显示,在学习过程中,V1神经元树突棘上SynapShot的ddGFP信号(G)与树突荧光信号(R)的比值(G/R比值)在部分树突棘上呈现动态变化,有的增强,有的减弱,说明与学习相关的突触强度变化可在活体中被追踪。而大多数mGRASP信号则表现出非特异的、普遍的减弱。通过计算变异系数和统计信号增强或减弱的斑点比例,SynapShot均显示出比mGRASP更高的灵敏度和分辨能力。
图6. 视觉辨别任务期间ACC-V1环路中的SynapShot信号
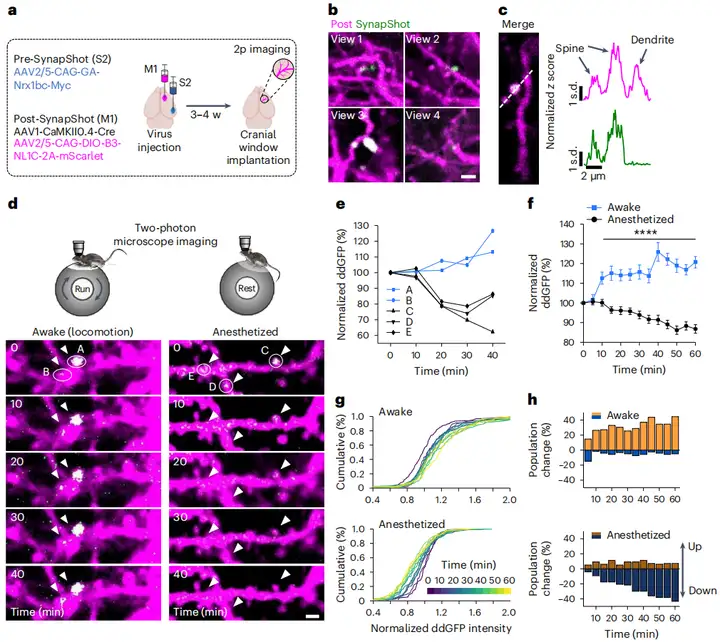
此外,在另一个涉及次级躯体感觉皮层(S2)-初级运动皮层(M1)环路的研究中,研究者比较了清醒运动小鼠和麻醉状态下小鼠的SynapShot信号。跑步机上运动小鼠的SynapShot信号整体平均水平随时间呈上升趋势,且单个突触的信号变化方向具有独立调控的特性:部分突触信号增强、部分减弱,说明行为过程中每个突触连接的强度均受到动态调控;而麻醉小鼠的SynapShot信号整体平均水平随时间持续下降。这充分证明了SynapShot能够在清醒自由活动、进行复杂行为的动物中,实时监测单个突触的结构可塑性,揭示了突触动态与行为状态之间的紧密关联。电生理记录也表明,表达SynapShot本身并不会干扰神经元的突触功能,确保了其作为报告系统的可靠性。
总结
该研究成功开发了名为“SynapShot”的基因编码荧光指示剂,实现了在活细胞和活体动物中实时、可逆地监测完整突触的结构动态。其核心突破在于摒弃了传统split FPs的不可逆结合,转而采用基于ddFPs的分子设计,从而首次实现了对突触连接形成与消除过程的双向、动态追踪。
SynapShot技术具备多项显著优势:其一,其双色配置(绿/红)允许在同一动物或同一神经元上同时追踪两个不同突触群体的动态变化;其二,红移版本与蓝光光遗传学工具兼容,为研究特定分子信号通路如何调控突触可塑性开辟了新途径;其三,其在体实验的成功,尤其是在复杂行为任务中展现出的高灵敏度和特异性,证明了它是研究学习、记忆、感觉运动整合等高级脑功能背后突触机制的有力工具。
尽管SynapShot目前对多聚甲醛等固定剂敏感,限制了其在传统组织学中的应用,但这恰与需要实时监测的活体研究形成互补。未来的工作可以通过分子工程改造,进一步提升ddFPs的稳定性,拓展其应用场景。总体而言,SynapShot的诞生为神经科学领域提供了一扇新的窗口,使我们得以窥见活体大脑中突触动态的真实面貌,有望极大地推动我们对突触可塑性在生理及病理状态下作用机制的理解。
我司可提供SynapShot病毒产品,列表如下:

扫码添加客服
更多产品及详情欢迎咨询!


市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK