2026-03-09 阅读量:150
神经调节技术是动物研究中解析复杂行为背后的神经环路机制以及治疗人类神经系统疾病的核心工具。目前主流的神经调节技术各有利弊:传统的脑深部电刺激(DBS)虽已广泛应用于临床,但缺乏细胞类型特异性,且为有创植入式操作;光遗传学凭借其毫秒级的高时间精度极大推动了神经科学的发展,但其依赖于微生物来源的通道蛋白和植入式光纤,带来了免疫原性和组织损伤的风险;化学遗传学则通过药物实现无植入调控,但其起效和消退依赖于药物的药代动力学,时间分辨率较低。因此,开发一种无需颅内植入物、兼具高时空精度与双向调节能力、并可靶向特定神经元亚型的神经调控技术,对于实现神经环路的精准解析以及推进神经系统疾病的临床治疗具有变革性意义。而磁场因其卓越的组织穿透性和安全性,为实现这一目标提供了可能。
美国康奈尔大学Michael G Kaplitt等人在Science Advances期刊(IF=11.7)发表题为“Bidirectional regulation of motor circuits using magnetogenetic gene therapy”的研究成果,开发并验证了一种全新的磁遗传学调控系统。该系统的核心为单一融合蛋白Nb-Ft-TRPV1,由靶向内源性铁蛋白(Ft)的新型纳米抗体(Nb)与经过改造的哺乳动物TRPV1离子通道融合而成,可通过单一腺相关病毒(AAV)载体递送,且无需颅内植入物。研究团队在帕金森病(PD)相关运动环路中的开展了一系列精巧实验,证实该系统可在清醒、自由活动的小鼠体内,借助临床常用的磁共振成像(MRI)或经颅磁刺激(TMS)设备产生的磁场,实现对特定神经元的远程、双向、可逆且时间精准的调控,既能诱发特定运动表型,也可有效改善PD模型小鼠的运动障碍。这一研究不仅为神经环路的解析提供了强大的新工具,也为未来神经系统疾病的基因治疗与无创物理调控相结合开辟了新的方向。
枢密科技重磅推出磁遗传学工具——Nb-Ft2-TRPV1Ca²⁺(激活型)与Nb-Ft-TRPV1Cl⁻(抑制型)!可在磁场作用下分别介导钙离子内流激活、氯离子内流抑制神经元活动。通过单AAV载体递送该融合蛋白,可捕获内源性Ft,使特定神经元获得对磁场的响应能力。该系统可适配临床MRI与TMS设备产生的磁场,实现无创驱动,支持快速、可逆的神经元双向调控,克服了光遗传学需植入光纤、化学遗传学响应延迟的局限,为神经环路精准操控、神经疾病机制研究及治疗策略探索提供突破性工具。选择枢密科技,开启磁遗传学研究新纪元!相关产品见文末~
1、靶向Ft的功能性Nb的筛选与体外验证
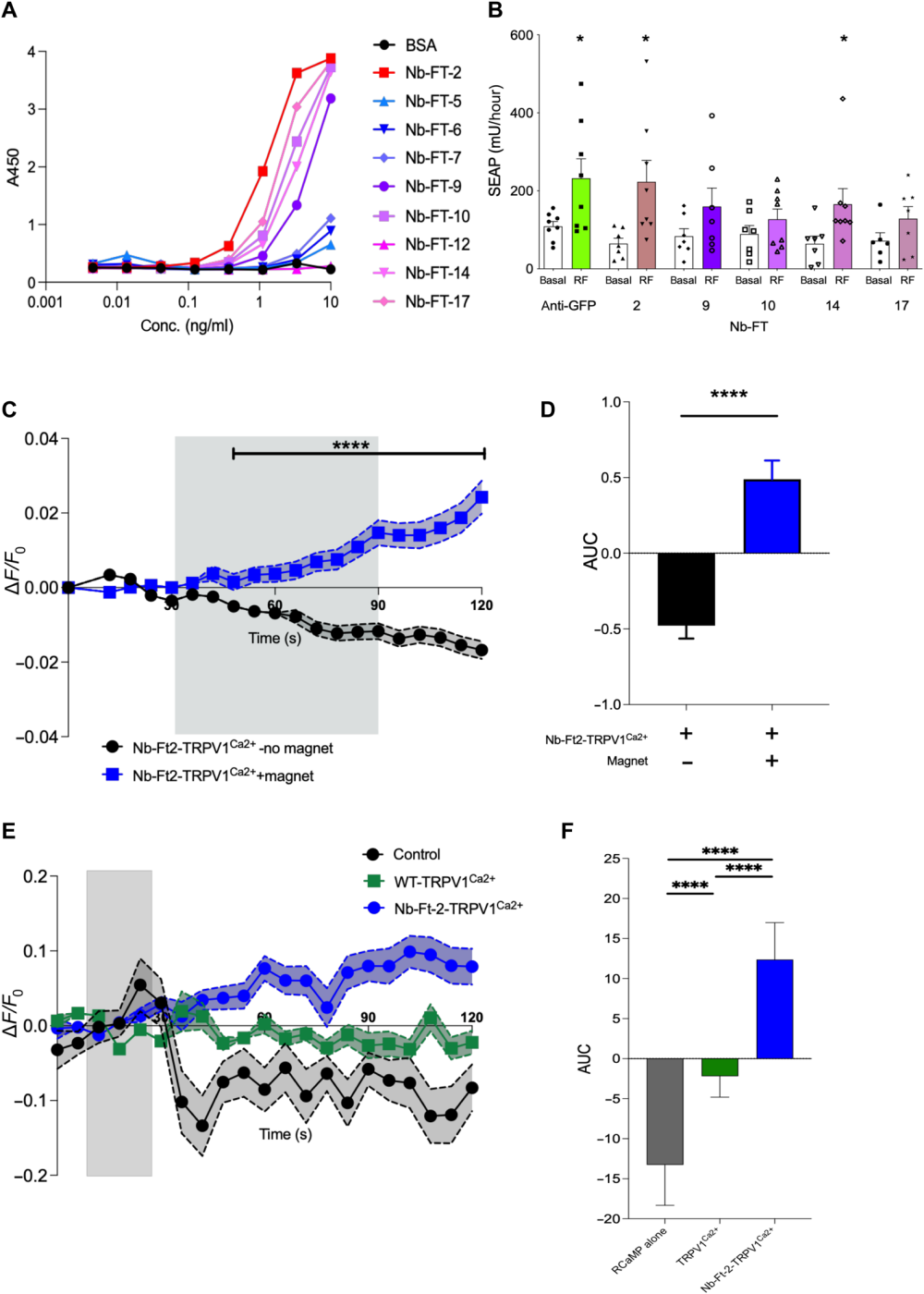
为实现无需外源性Ft共表达的单载体递送,研究者首先通过噬菌体展示技术构建免疫组库并进行淘选,筛选能够结合内源性Ft的Nb,最终获得多个可同时结合人源、鼠源Ft的Nb克隆。经酶联免疫吸附试验筛选出5株对人Ft亲和力最高的克隆后,进一步通过钙依赖性分泌型碱性磷酸酶(SEAP)报告基因检测其磁致升钙能力,同时结合免疫沉淀试验验证其对鼠源内源性Ft的结合能力,结果显示克隆2(Nb-Ft-2)对人Ft亲和力最高,且能最有效地富集鼠源内源性Ft,为最优候选克隆。
将克隆2与TRPV1通道融合构建Nb-Ft2-TRPV1Ca2+后,该融合通道可在人胚肾293T细胞和小鼠Neuro2A细胞中实现正常的细胞表面表达;功能验证显示,振荡磁场(293T细胞)或静磁场(Neuro2A细胞)处理下,表达该融合蛋白的细胞均出现显著钙内流,表现为钙依赖性荧光探针信号显著增强。此外,该融合蛋白的cDNA序列仅2.9 kb,可被包装进单个AAV载体实现神经元转导。以上结果表明,筛选到的Nb(Nb-Ft-2)可有效介导磁场能量向离子通道门控的转换,为后续体内实验提供了最优的候选分子。
图1. 磁响应性Ft结合Nb的筛选与验证
2、磁遗传学激活纹状体间接通路可改变小鼠运动行为
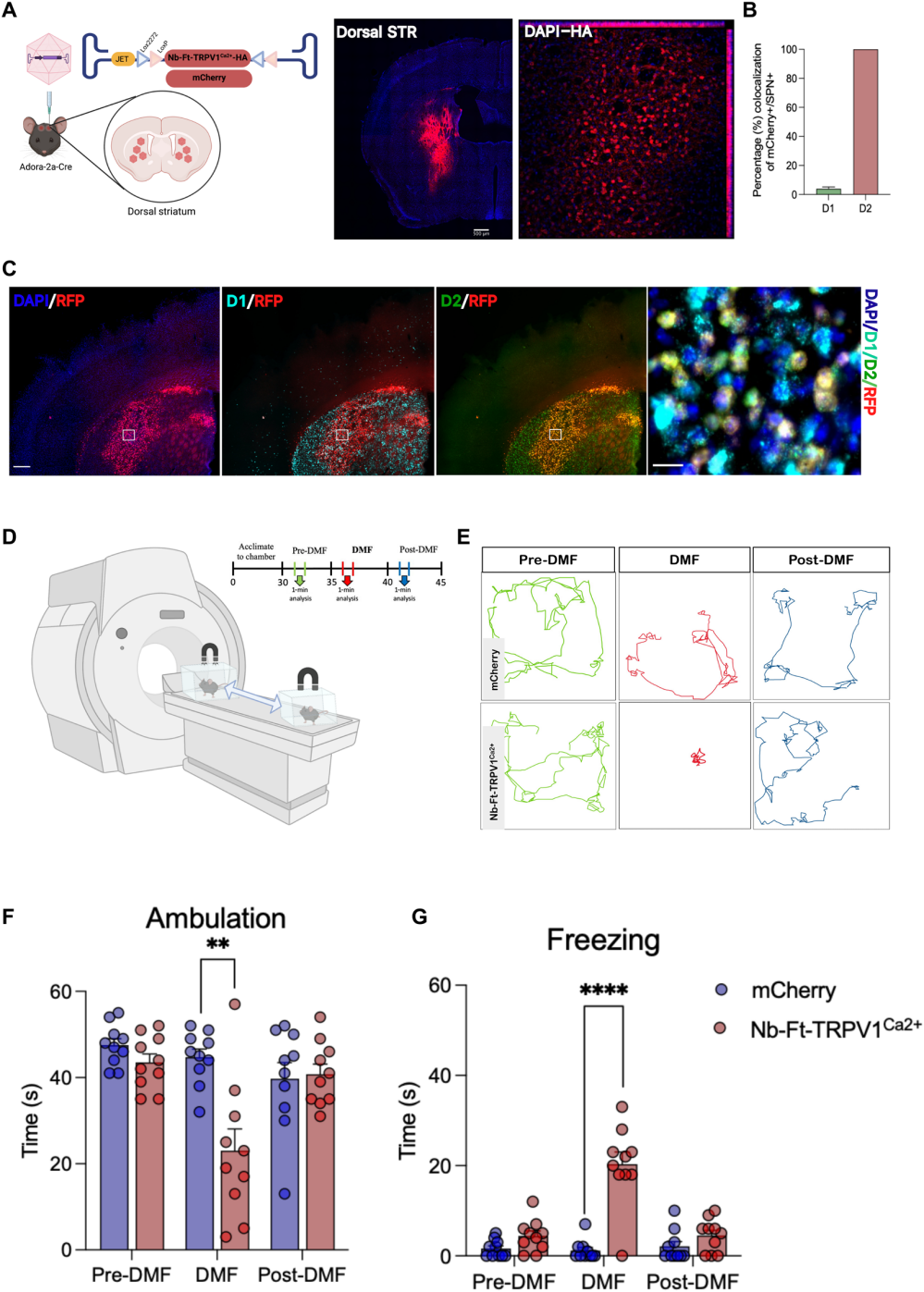
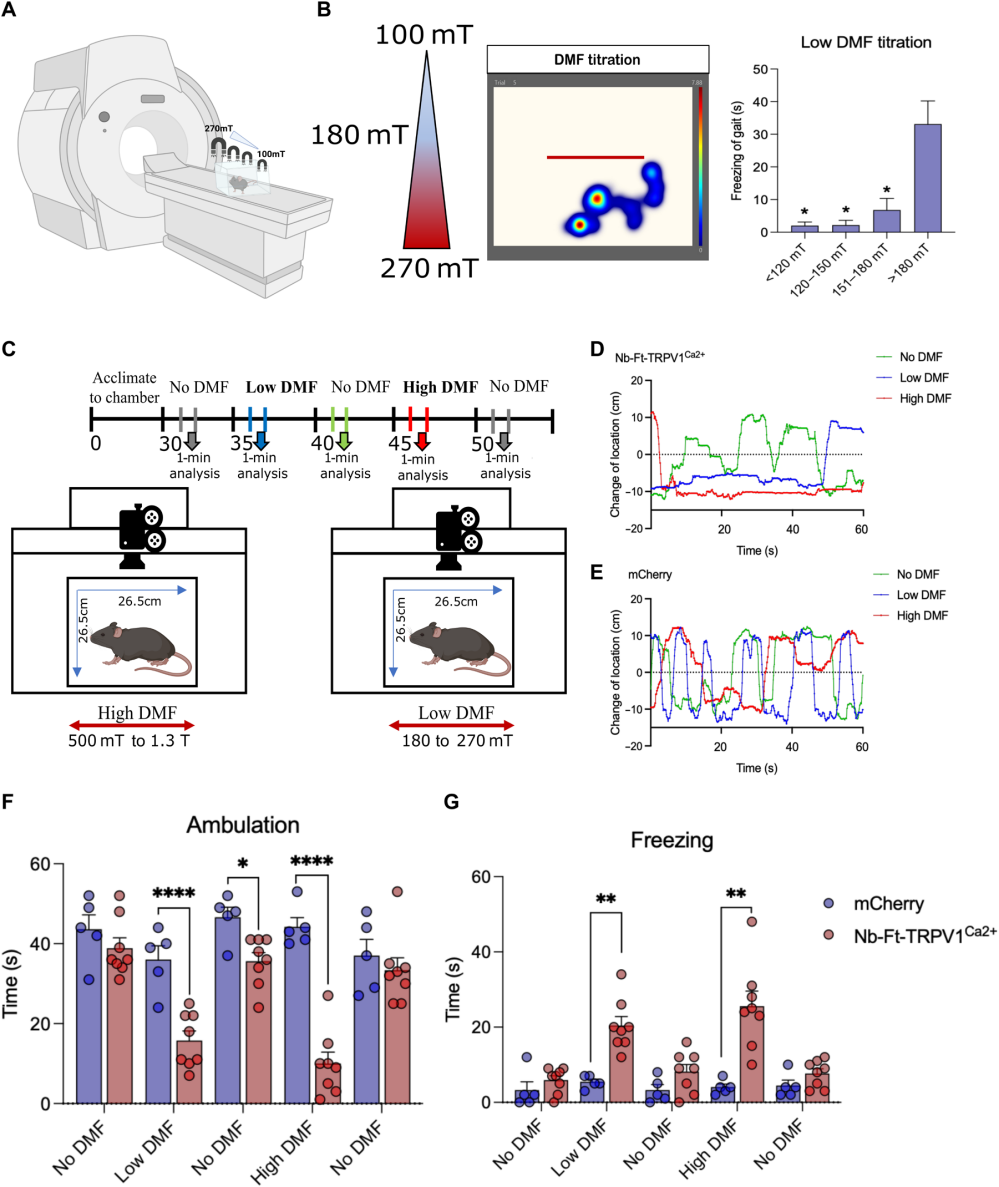
为验证该系统的体内功能,研究者首先靶向了基底神经节运动环路中的关键通路——间接通路。该通路的起始神经元位于纹状体,是一类表达多巴胺D2受体的棘状投射神经元(简称D2 iSPNs),它们发送抑制性投射至苍白球外部(GPe),最终通过兴奋苍白球内部(GPi)抑制丘脑,从而抑制运动。研究者利用A2a-Cre转基因小鼠(其Cre重组酶特异性表达于D2 iSPNs中),将Cre依赖的兴奋性磁遗传学病毒AAV1/2-JET-DIO-Nb-Ft-TRPV1Ca2+-HA立体定位双侧注射至背侧纹状体,从而实现对iSPNs的精准标记与功能操纵。组织学分析证实了病毒在D2神经元中的高效且特异的表达,且其轴突投射可追踪至靶区GPe。行为学结果显示,当这些小鼠被置于3T磁共振成像设备产生的静磁场(DMF)中时,其运动活动显著减少,并出现明显的步态冻结现象。该行为在磁场暴露后40-60秒内出现,撤去磁场后1分钟内即可恢复正常,而对照mCherry组小鼠则无此变化。通过精确测量笼内不同位置的磁场强度,研究者进一步确定了诱导该行为效应的磁场强度阈值为180 mT:小鼠仅在进入场强高于此阈值的区域时才表现出冻结行为,且撤去磁场后行为迅速恢复正常,这一结果在低场强和高场强条件下均得到了重复验证。以上结果证明了磁遗传学激活特定神经环路可实时、可逆地调控动物行为。
图2. iSPNs中Nb-Ft-TRPV1Ca2+的选择性表达在磁场作用下诱发PD样运动表型
图3. 在D2 iSPNs中表达的Nb-Ft-TRPV1Ca2+经高DMF和低DMF处理后诱发步态冻结
3、磁遗传学刺激增强体内纹状体神经元活动
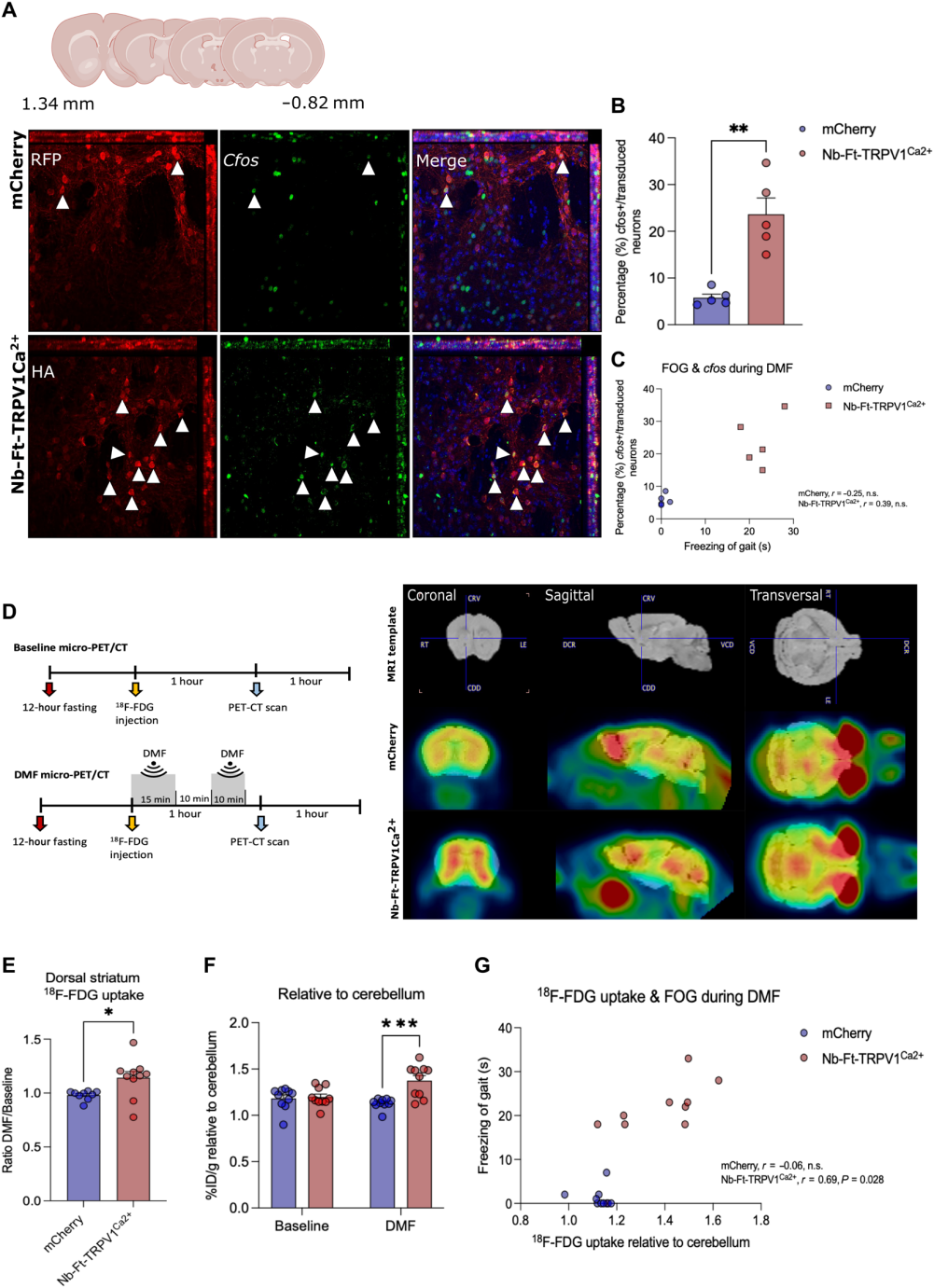
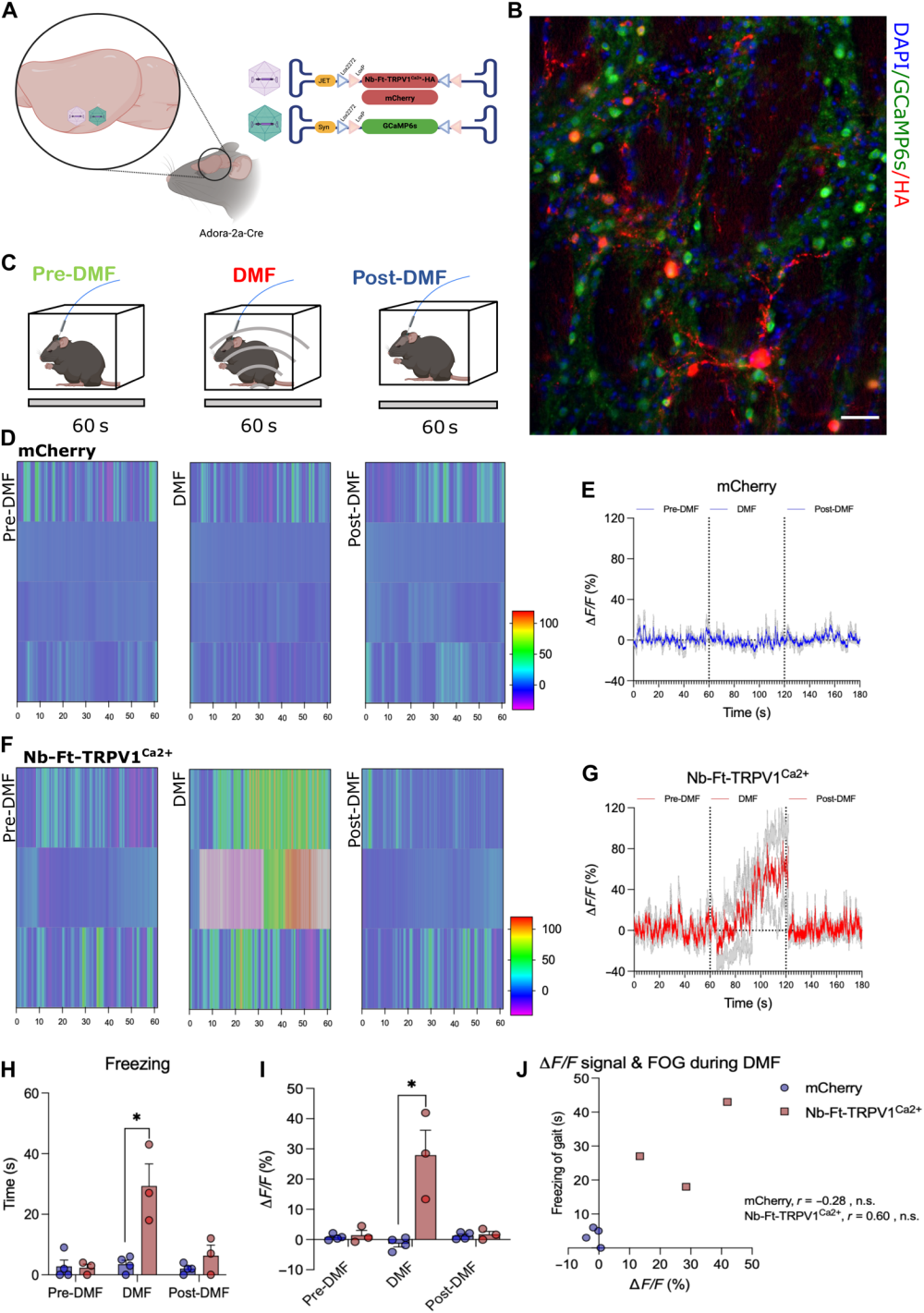
为将行为变化与神经元活动直接关联,研究者采用了多种独立的技术手段。首先,免疫组织化学染色显示,在磁场暴露后,表达Nb-Ft-TRPV1Ca2+的纹状体神经元中即刻早期基因c-Fos的阳性率显著高于对照组。其次,利用18F-氟代脱氧葡萄糖(18F-FDG)微正电子发射断层扫描/计算机断层扫描(PET/CT)成像发现,磁场暴露显著增加了表达Nb-Ft-TRPV1Ca2+小鼠纹状体的葡萄糖摄取(能量代谢)水平,且该水平与小鼠的冻结时间呈正相关。最后,研究者结合光纤记录技术与钙指示剂GCaMP6s,在自由活动小鼠中实时监测D2 iSPNs的群体活动。结果表明,当小鼠进入磁场区域时,表达Nb-Ft-TRPV1Ca2+的小鼠纹状体GCaMP信号显著增强,同时伴随运动冻结,而对照组无此现象。c-Fos、PET/CT和光纤记录这三组数据从基因表达、能量代谢和实时钙离子信号三个维度共同证实,磁场确实有效激活了被磁遗传学系统靶向的纹状体D2 iSPNs。
图4. DMF激活Nb-Ft-TRPV1Ca2+增强纹状体神经元c-Fos表达与葡萄糖代谢
图5. Nb-Ft-TRPV1Ca2+可增强背侧纹状体的钙瞬变
4、临床级TMS设备可有效驱动磁遗传学效应
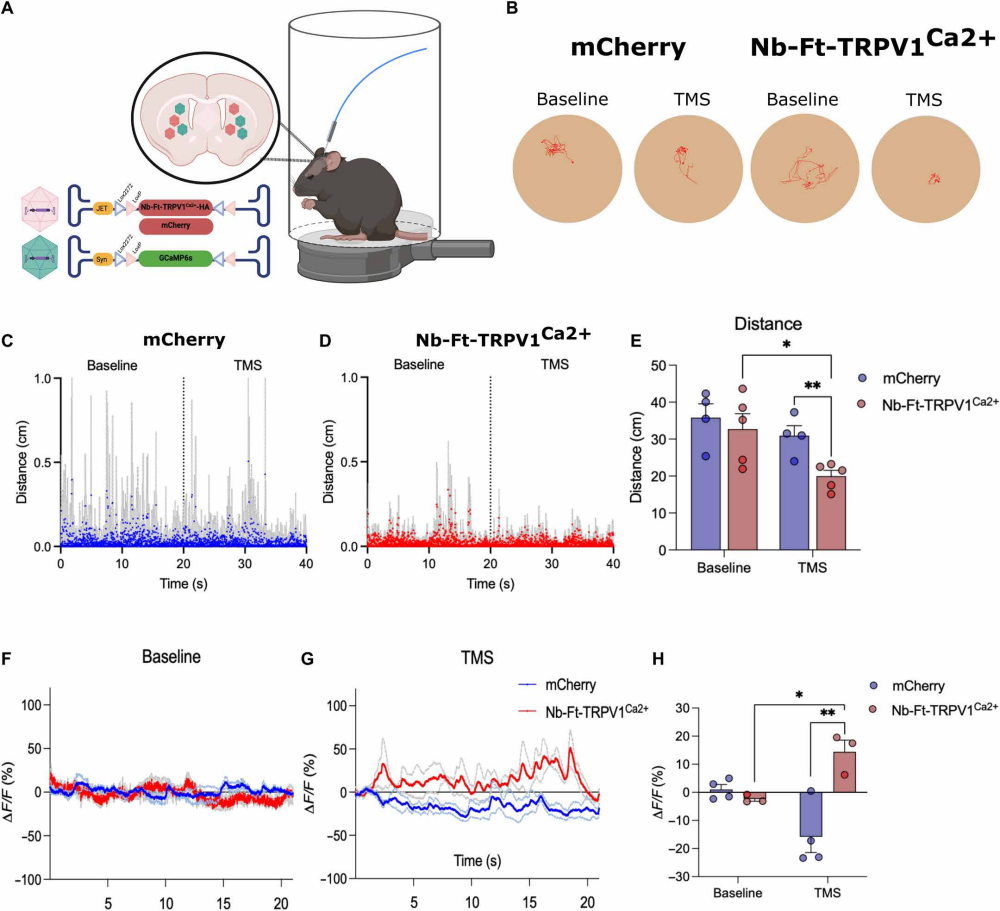
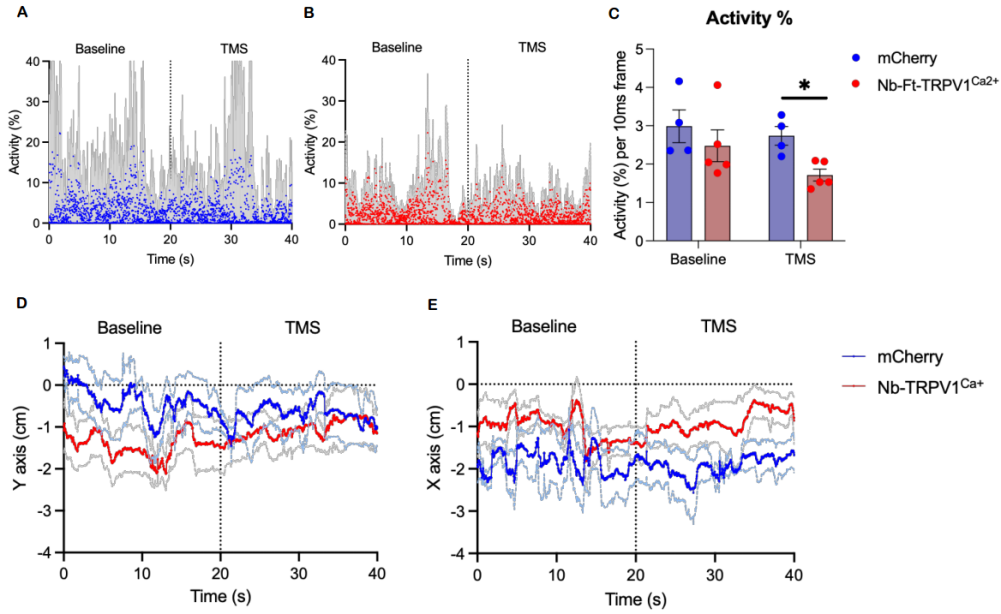
鉴于需靠近MRI设备才能发挥效应的技术临床治疗转化潜力有限,研究者转向了更为便携且已在临床治疗中广泛应用的TMS设备。使用商用TMS线圈(20%输出容量,50次双脉冲/秒,刺激间隔1秒)对表达Nb-Ft-TRPV1Ca2+的小鼠进行刺激,同样观察到了显著的运动抑制和冻结行为,其效果与MRI刺激一致。结合光纤记录发现,TMS刺激在诱导行为冻结的同时,也引发了纹状体GCaMP信号的快速增强。该结果证实,现有临床TMS设备(远低于其最大输出容量)即可驱动该磁遗传学系统,为其临床转化奠定了重要基础。
图6. TMS处理可增强Nb-Ft-TRPV1Ca2+介导的运动冻结及背侧纹状体钙瞬变
5、磁遗传学对野生型小鼠的环路特异性调控
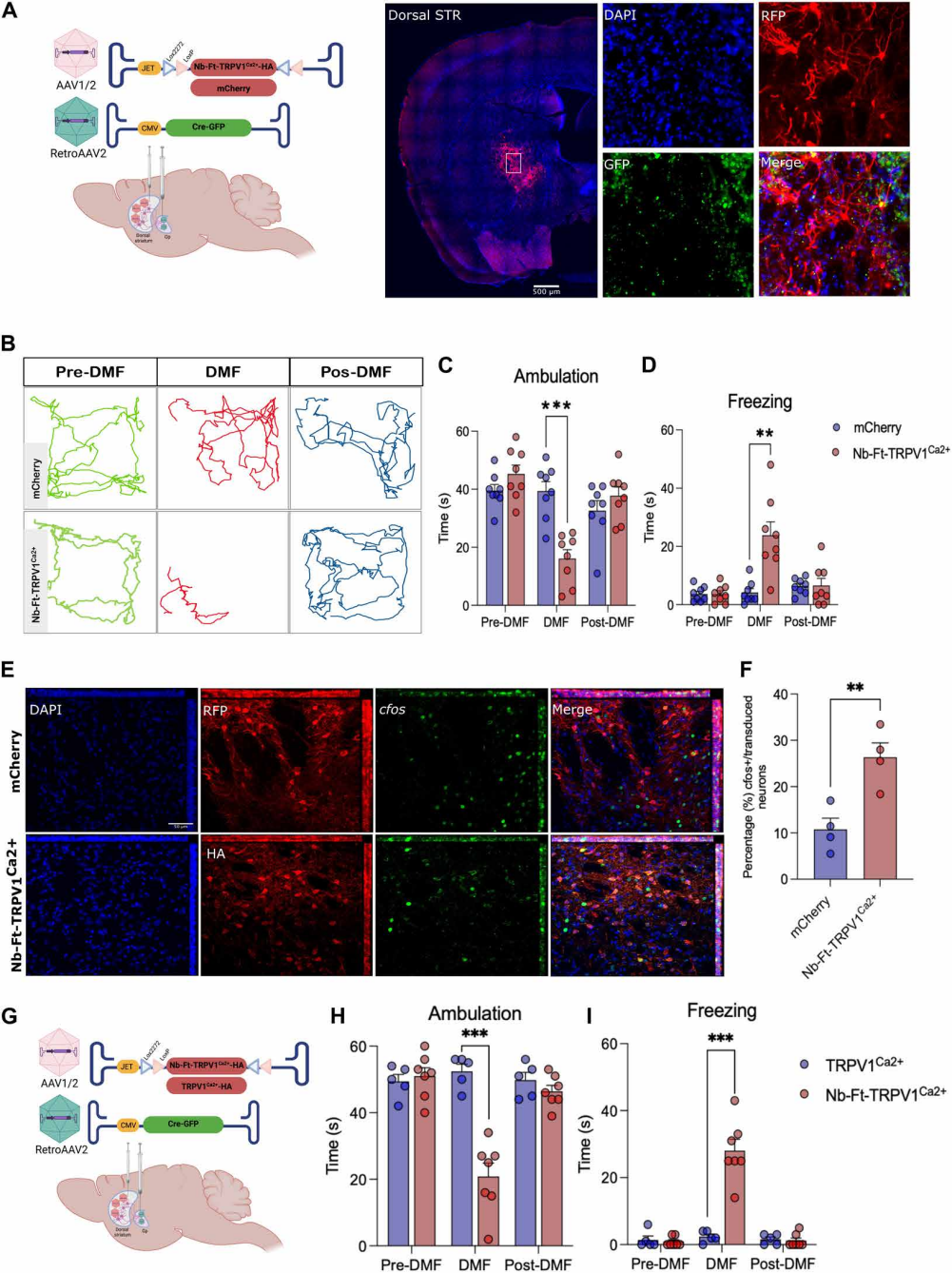
为实现对特定投射环路而非全脑某一类型神经元的靶向,且突破Cre转基因鼠的应用限制,研究者在野生型(WT)小鼠中使用双病毒策略:首先在背侧纹状体注射Cre依赖的磁遗传学病毒AAV1/2-JET-DIO-Nb-Ft-TRPV1Ca2+-HA,然后在纹状体投射的主要下游脑区GP注射表达Cre的逆行病毒AAV2/Retro-CMV-Cre-GFP。使得只有投射到苍白球的背侧纹状体神经元才能表达Nb-Ft-TRPV1Ca2+。组织学共定位分析证实了这种策略成功地将通道表达限制在纹状体-GP环路上。行为学结果显示,这些WT小鼠在磁场中同样表现出显著的冻结行为和运动减少,其效果与在转基因小鼠中观察到的一致。此外,作为对照,仅表达TRPV1Ca2+而不含Nb的构建体在磁场中不能诱导相应的行为变化,再次证明Nb介导的Ft偶联是磁响应所必需的。
图7. 纹状体-GP通路中AAV介导的Nb-Ft-TRPV1Ca2+选择性表达,在磁场存在下诱导WT小鼠PD样运动行为
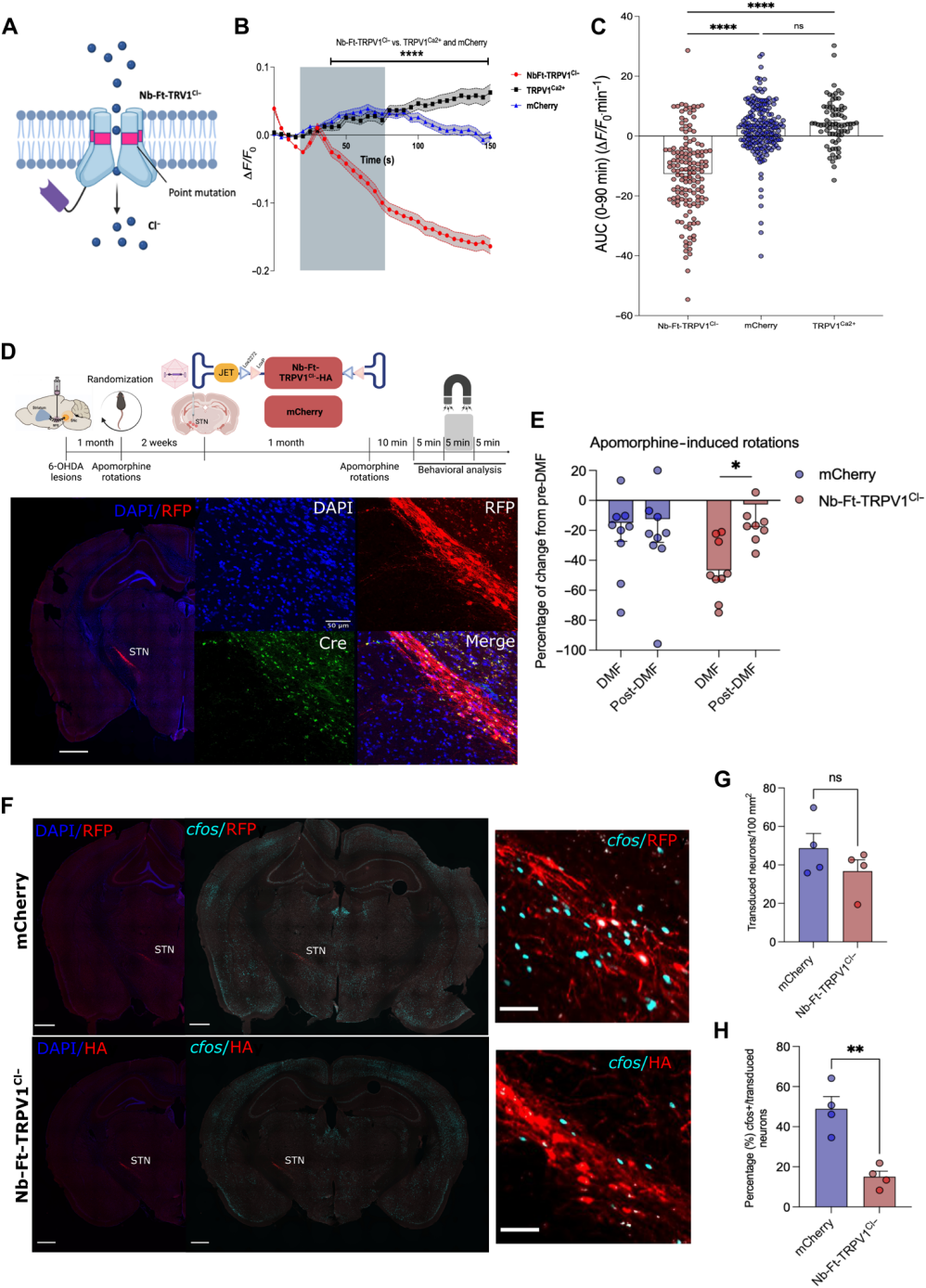
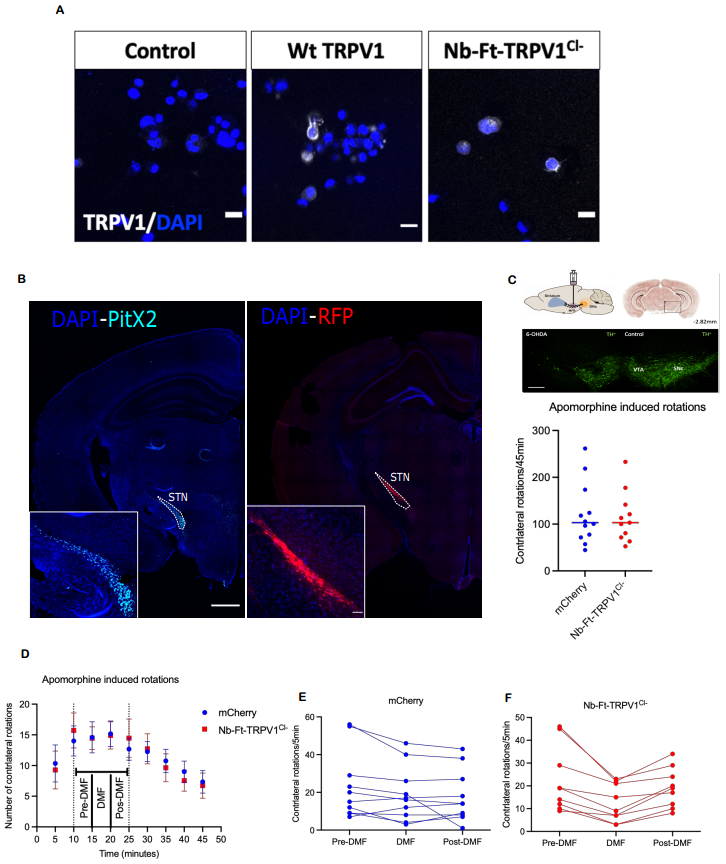
6、抑制性磁遗传学系统改善PD模型小鼠的运动功能
为构建抑制性工具,研究者通过点突变将TRPV1改造为高氯通透性变体(Nb-Ft-TRPV1Cl⁻)。体外氯离子荧光成像证实,表达该抑制性构建体的细胞在磁场暴露后,胞内氯离子浓度显著升高,提示通道开放可介导氯离子内流。随后,研究者将这一抑制性系统应用于经典的PD运动核团——丘脑底核(STN)。在单侧黑质多巴胺能神经元6-羟基多巴胺(6-OHDA)损伤的PitX2-Cre小鼠(STN神经元特异性表达Cre)的STN中注射Cre依赖的抑制性磁遗传学病毒AAV1/2-JET-DIO-Nb-Ft-TRPV1Cl−-HA。行为学测试显示,磁场暴露可显著改善阿扑吗啡诱导的对侧旋转行为,旋转次数较无磁场条件及对照组均明显减少。同时,STN脑区的c-Fos免疫组化染色证实,磁场暴露有效抑制了表达该通道神经元的活动。这些结果证明,磁遗传学不仅可用于激活,也可用于抑制特定深部脑区神经元,并对疾病模型的行为产生积极的治疗性干预效果。
图8. Nb-Ft-TRPV1Cl⁻可抑制STN神经元的活性并改善PD模型小鼠的运动功能障碍
总结
该研究成功开发了一种单AAV载体递送的新型磁遗传学系统,通过将最优纳米抗体Nb-Ft2与改造后的TRPV1通道融合,实现对内源性Ft的捕获,从而赋予特定神经元亚群对磁场的敏感性。研究团队在PD相关运动核团与环路中,利用MRI和TMS设备产生的磁场,实现了对神经元活动的双向、可逆、无创调控,并验证了其在解析环路功能和干预疾病模型中的巨大潜力。
这项工作的核心突破在于:首先,AAV单载体设计解决了此前系统复杂、递送困难的问题,使其更利于临床转化;其次,证实了临床现有的TMS设备足以驱动该系统,极大提升了技术的可及性;最后,成功构建抑制性磁遗传学工具,完善了磁遗传学的双向调控工具箱。
尽管该技术未来仍需对其长期安全性(如对细胞铁代谢的影响)与精确作用机制开展深入研究,但该成果无疑为神经科学研究提供了一种强大的新范式,并为未来基于基因治疗的无创物理调控神经疾病疗法奠定了坚实的基础,具有重要的科学意义与广阔的转化前景。
我司可提供Nb-Ft-TRPV1病毒产品,部分列表如下:

扫码添加客服
更多产品及详情欢迎咨询!


市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK