2026-03-16 阅读量:228
创伤后应激障碍(PTSD)和焦虑症患者常常陷入一个怪圈:越想摆脱恐惧,恐惧反而越缠越紧。目前最主流的治疗方法——暴露疗法,通过让患者反复接触引发恐惧的刺激,帮助他们认识到这些刺激其实并不危险,从而建立起新的安全记忆来对抗旧的恐惧。这个方法确实帮助了很多人,但临床上一直存在一个令人困惑的现象:部分患者在治疗后,虽然对原来的恐惧对象不再那么害怕,却开始对原本安全的事物产生新的恐惧——一个因车祸害怕开车的人,治好了开车恐惧,却开始害怕坐地铁、坐公交。这种“恐惧泛化”让治疗陷入了进退两难的境地。恐惧泛化的本质,是大脑失去了区分危险与安全的能力。传统观点认为这是恐惧记忆本身太强导致的,但这就无法解释一个矛盾:为什么患者对原始恐惧的反应已经减轻,分辨能力反而更差了?这说明,消退训练本身可能触发了某种独立的神经机制,在消除旧恐惧的同时,意外地损害了大脑的“安全识别系统”。
徐州医科大学吴坤伟、李灿、曹君利教授团队的最新研究,正好揭开了这个谜底。他们在《美国国家科学院院刊》(PNAS)发表题为“Fear extinction induces maladaptive generalization via noradrenergic and GABAergic systems”论文,发现恐惧消退训练会意外激活一条从脑干蓝斑核(LC)通往海马齿状回(DG)的去甲肾上腺素(NE)能通路。LC释放的NE作用于DG内GABA能中间神经元上的β1受体,进而通过蛋白激酶A/cAMP反应元件结合蛋白(PKA/CREB)信号通路上调颗粒细胞(GCs)表面α4-GABAA受体功能,增强紧张性抑制,最终过度抑制参与情境分辨的GCs,导致大脑失去区分能力——该怕的不怕了,不该怕的反而怕了。这个发现的意义在于,它把暴露疗法的“副作用”从模糊的临床观察变成了具体的神经机制,为优化治疗提供了明确的靶点和时间窗口。未来或许可以通过精准干预这些分子靶点,在保留消退训练疗效的同时,阻断恐惧泛化的发生,让心理治疗真正进入精准医学的时代。
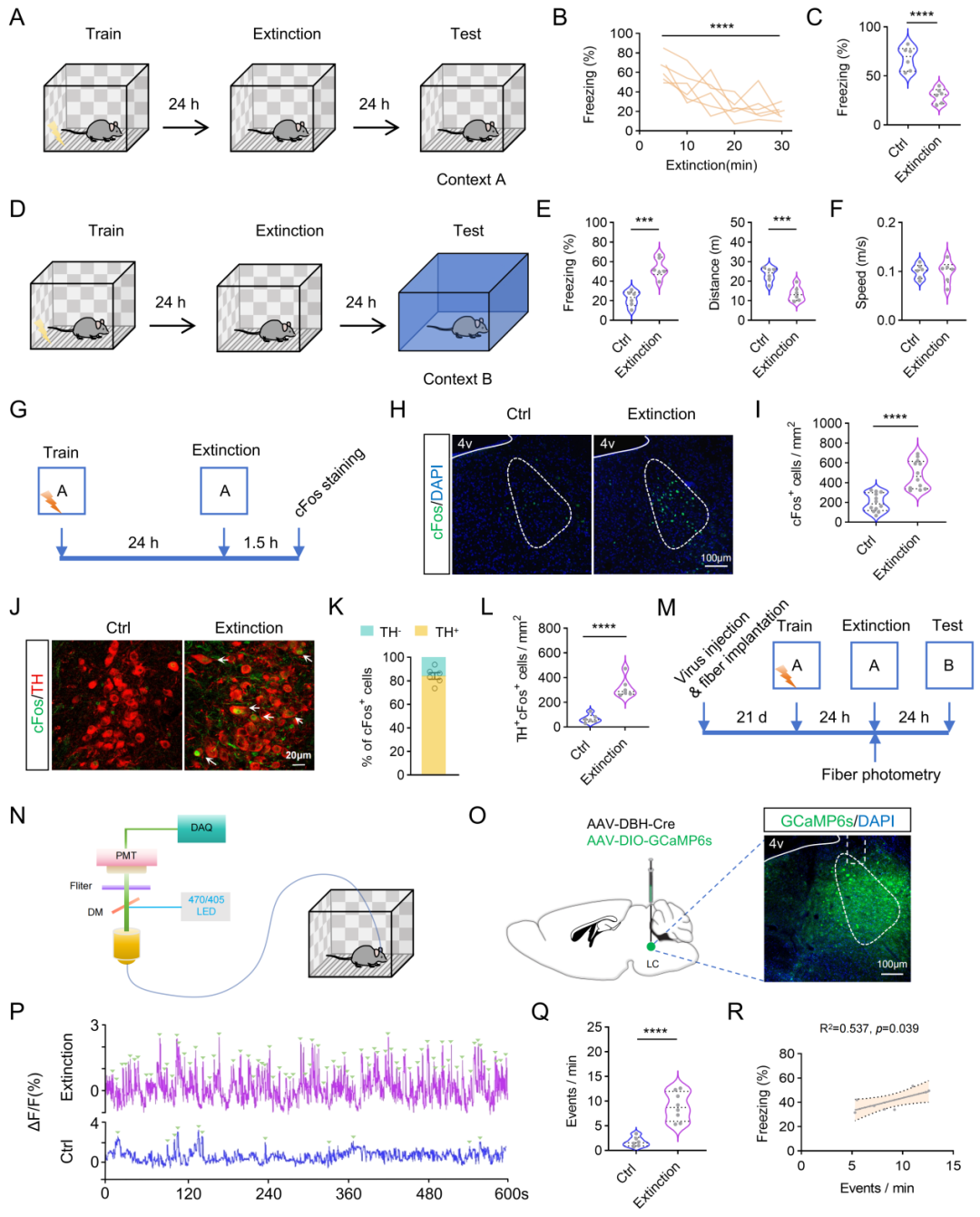
研究团队通过情境恐惧条件化模型发现,恐惧消退训练虽成功降低小鼠对原始危险环境的恐惧,却意外导致其对相似安全环境产生显著的恐惧泛化,表现为僵直反应增加、探索行为减少。行为学分析显示,消退训练损害了小鼠区分威胁与安全环境的能力——未经历消退训练的小鼠能区分危险与安全情境,而经历消退训练的小鼠不仅对原始危险环境的恐惧反应下降,还对安全环境产生过度恐惧。这一发现揭示,恐惧消退训练实则是一把“双刃剑”:在消除特定情境恐惧的同时,会损害大脑的威胁辨别能力,导致适应不良的恐惧泛化。
那么,究竟是哪个脑区介导了这一悖论性现象?研究人员将目光投向蓝斑核(LC)——脑内NE能神经元的主要起源核团,广泛参与应激、觉醒和情绪调节。他们发现恐惧消退训练显著激活了LC中的NE能神经元,且这类神经元的激活水平与后续的恐惧泛化行为呈正相关,即LC-NE神经元越活跃,小鼠的恐惧泛化越严重。为了验证因果关系,研究团队运用化学遗传学技术进行操控:在消退训练后立即抑制LC-NE神经元,可以特异性阻断恐惧泛化的发生,而不影响原始情境下的消退记忆;反之,直接激活LC-NE神经元(无需消退训练)就足以诱导出恐惧泛化。值得注意的是,这一效应具有严格的时间窗口——只有在消退训练后的记忆巩固阶段进行干预才有效,若在泛化测试前干预则无效,提示临床干预的“黄金时间窗口”至关重要。
图1. 恐惧消退诱发恐惧泛化并激活LC-NE系统
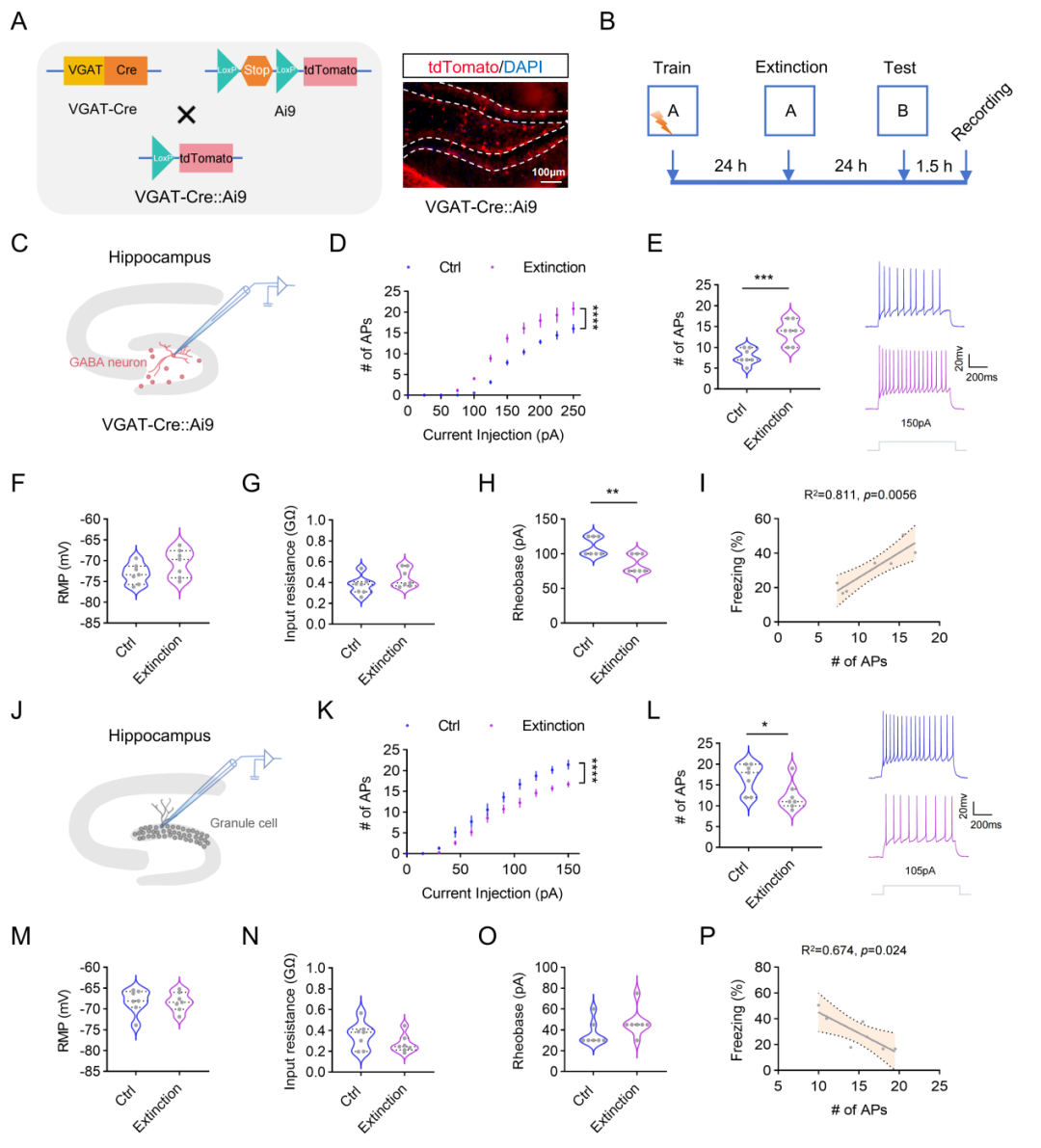
LC-NE神经元向海马齿状回(DG)有密集投射,而DG是情境辨别和模式分离的核心脑区。研究团队通过光纤记录技术发现,消退训练期间DG的NE释放显著增加,且这种增加与泛化行为正相关。更重要的是,在泛化测试时DG的NE释放水平显著高于消退记忆测试时,证实DG NE信号特异性参与恐惧泛化的表达。通过脑区局部给药发现:DG局部给予β-肾上腺素能受体(β-AR)拮抗剂普萘洛尔可有效阻断恐惧泛化;化学遗传学激活LC→DG通路(无需消退训练)足以诱导恐惧泛化,而这一效应可被DG局部给予普萘洛尔所阻断。这些结果证明LC→DG神经环路及其介导的β-AR激活是恐惧泛化的关键调控机制。通过电生理记录发现:消退训练后DG中的GABA能中间神经元兴奋性升高,而GCs兴奋性下降。有趣的是,GABA能神经元的兴奋性与恐惧泛化行为呈正相关,而GCs的兴奋性与恐惧泛化行为呈负相关。为了验证因果关系,研究团队利用AAV-shRNA病毒特异性敲低GABA能神经元上的β1-AR。结果显示:敲低β1-AR可有效阻断恐惧泛化,同时恢复GCs的正常兴奋性。
图2. 恐惧消退双向调控DG神经元兴奋性
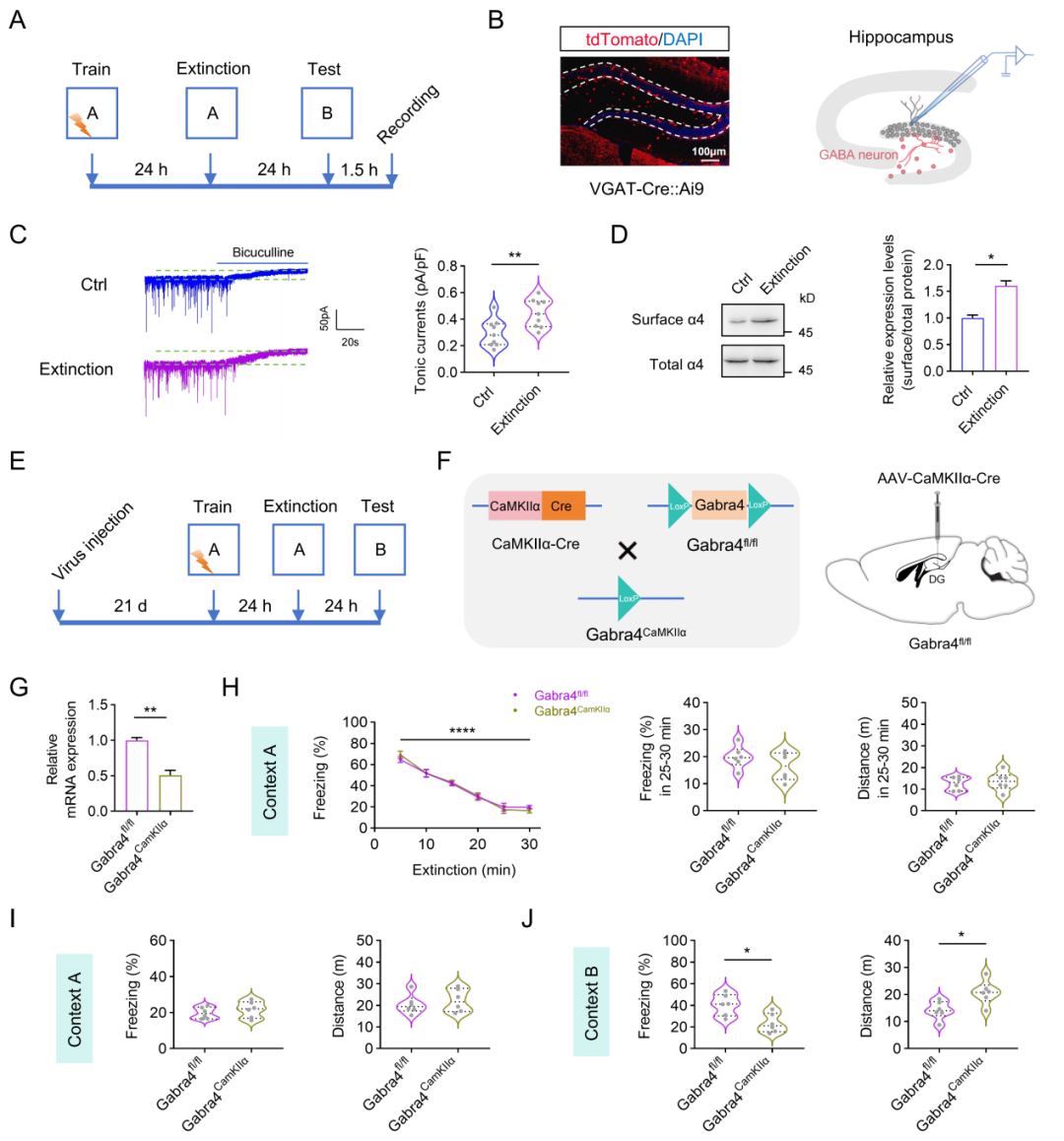
进一步研究发现,消退训练促进了DG内GABA能神经元的GABA释放,并选择性增强了GCs上α4-GABAAR介导的紧张性抑制电流,同时该受体在GCs膜表面表达增加。条件性敲除GCs中α4-GABAAR可有效阻断恐惧泛化,证实该受体是介导恐惧泛化的必需分子元件。机制研究表明,消退训练触发了DG中蛋白激酶A/cAMP反应元件结合蛋白(PKA/CREB)信号通路的持续激活——这一激活在训练后1小时即可出现,并持续至少7天,形成一种持久性的“分子记忆”。这种持续的信号激活驱动α4-GABAAR在GCs膜表面的长期表达,导致GCs兴奋性持续抑制。在消退训练后立即向DG局部注射PKA抑制剂或CREB抑制剂,能够有效阻断恐惧泛化的发生,并恢复GCs的正常兴奋性。这一结果不仅证实了PKA/CREB信号通路的核心调控作用,同时为临床干预恐惧泛化提供了明确的分子靶点。
图3. GCs上的α4-GABAAR介导恐惧消退诱发的恐惧泛化
结论
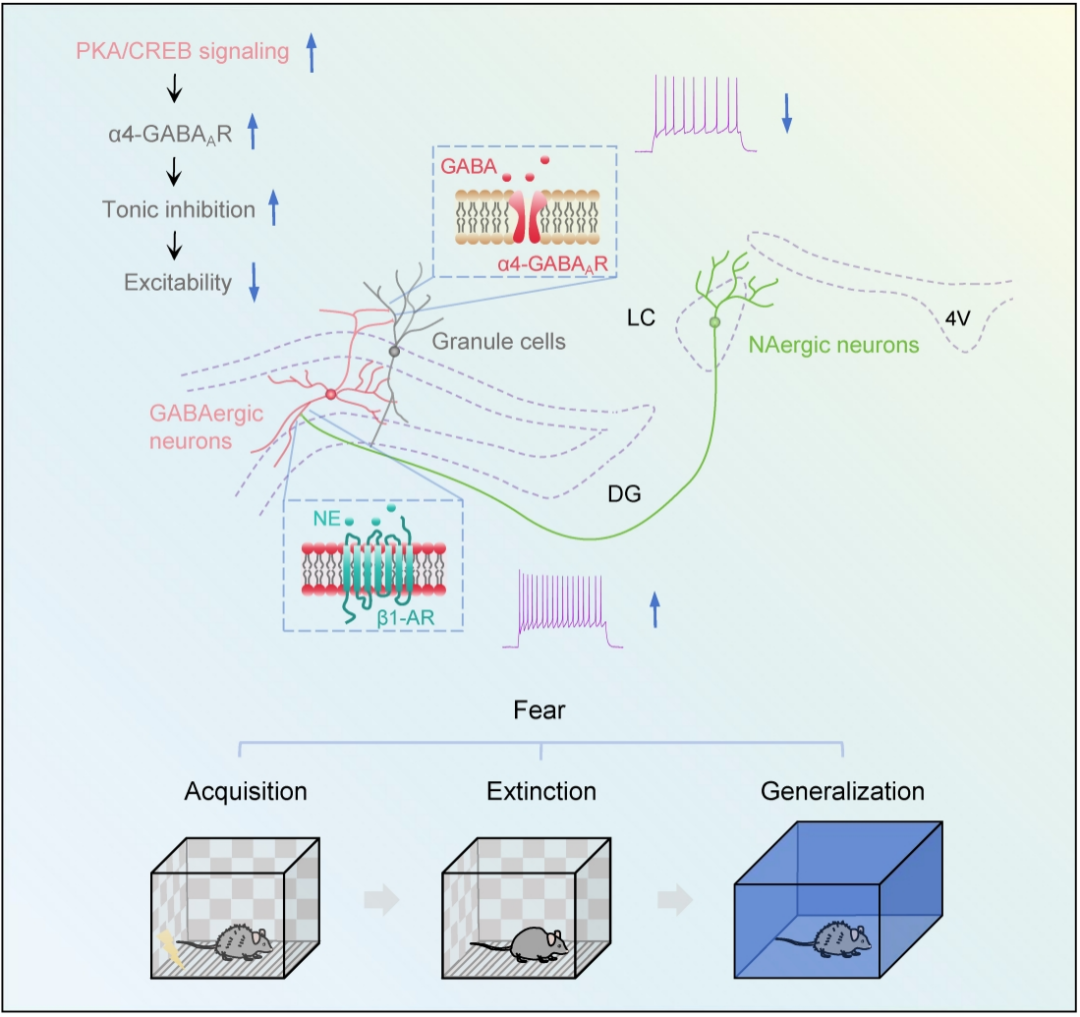
综上所述,本研究系统揭示了恐惧消退训练诱发恐惧泛化的神经环路和分子机制,阐明了“LC→DG”NE能通路通过β1-AR→PKA/CREB→α4-GABAAR级联反应,导致GCs过度抑制、情境辨别能力受损。这一发现不仅解释了暴露疗法可能存在的“副作用”及其神经生物学基础,也为开发精准的干预策略、推动个体化治疗提供了新的靶点和理论依据。
图4. 文章总结图
徐州医科大学江苏省麻醉学重点实验室吴坤伟教授、曹君利教授,江苏省免疫与代谢重点实验室李灿教授为本文共同通讯作者。硕士研究生郑爱秋、俞丹、孟欣为共同第一作者,硕士研究生龚淑敏、叶嘉乐,本科生周慧参与本研究。合作研究者还包括江苏省麻醉学重点实验室马钧教授、安述明教授、陈默副教授。本研究获国家自然科学基金委、江苏省科技厅及教育厅资助。
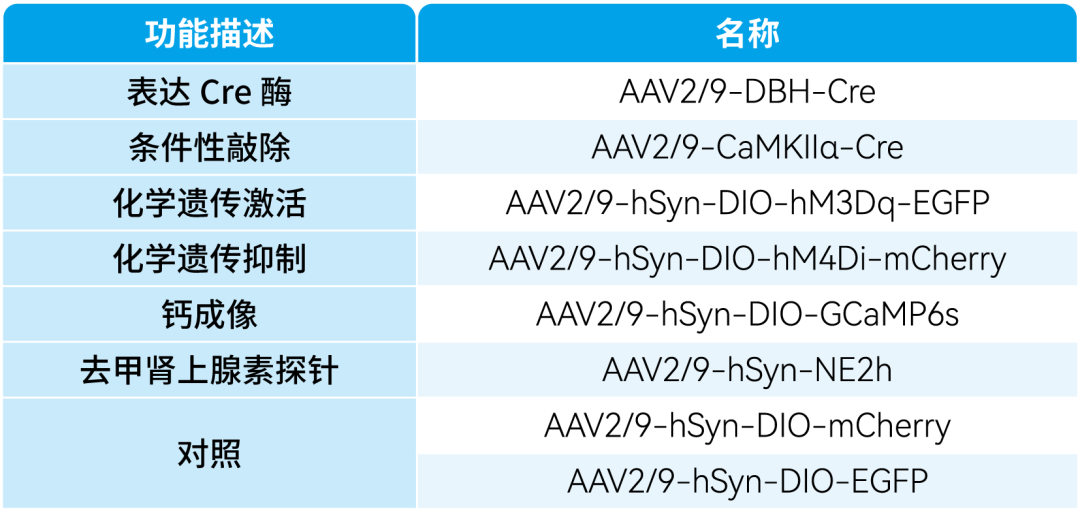
本文使用的来自枢密科技的病毒产品,列表如下:
扫码添加客服
更多产品及详情欢迎咨询!


市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK