2026-03-09 阅读量:175
肠易激综合征(IBS),尤以腹泻型为甚,是一类患病率极高的脑-肠轴互动紊乱疾病,慢性内脏痛是其最为严重且难治的核心症状。目前一线治疗方案包括饮食调整、解痉药以及肠道靶向药物,但对多数患者而言,仅能产生有限且短暂的缓解效果。内脏痛复发率高,加之长期用药可能带来的不良反应,凸显出对新型、可持续治疗途径的迫切需求。IBS慢性内脏痛的病理生理机制十分复杂,涉及外周肠道因素与中枢神经系统(CNS)功能异常之间的动态相互作用。越来越多的证据(包括本团队既往研究)表明,中枢加工异常或中枢敏化是其中的关键机制。神经影像学研究一致显示,IBS患者大脑中负责疼痛感知、放大与调控的网络存在功能与结构改变。这种以中枢为核心的观点,将IBS重新定义为不仅是外周肠道疾病,更是可通过直接神经调控进行干预的疾病。
研究表明,内侧前额叶皮层(mPFC)在整合疼痛的认知评价与情绪维度中发挥不可或缺的作用。临床观察也显示,IBS患者mPFC脑区的灰质体积与脑血流量存在异常。然而,mPFC调控内脏痛所依赖的具体细胞类型、神经环路及分子机制在很大程度上仍未被阐明。这种在细胞与环路层面机制认识的缺失,阻碍了精准靶向神经调控疗法的研发。
重复经颅磁刺激(rTMS)作为一种无创技术,可调节皮层兴奋性并影响皮层下疼痛处理通路,在理论上是治疗以中枢调控异常为基础的慢性痛的理想策略。然而,将其专门用于腹泻型肠易激综合征(IBS-D)慢性内脏痛的研究仍极为匮乏,既缺少可靠的临床证据,也缺乏来自临床前模型的机制阐释。因此,将rTMS转化为该病的有效治疗手段仍面临两个核心未解问题:第一,用于缓解IBS-D相关内脏痛的最佳皮层靶点尚未被系统鉴定;第二,rTMS发挥潜在疗效的神经生物学机制(包括细胞基础及对神经可塑性的长期影响)仍完全未知。因此,系统鉴定一个异常兴奋且可作为可靠rTMS靶点的疼痛处理脑区,是推动该领域发展的关键前提。
近期,苏州大学神经科学研究所徐广银教授与苏州大学附属第一医院消化内科李锐教授作为共同通讯作者,在Gut期刊(IF=25.8,中科院一区Top)发表了题为“Low-frequencyrepetitive transcranial magnetic stimulation attenuates visceral pain in IBS with diarrhoea via inhibition of the medial prefrontal cortex”的研究论文。本研究首先通过系统性临床研究,鉴定出伴有内脏痛的IBS-D患者中持续异常激活的脑区,结果提示mPFC为关键神经底物。随后,本研究采用多学科手段,利用新生期母婴分离(NMD)慢性内脏痛小鼠模型,从细胞(mPFC谷氨酸能(mPFCGlu)神经元)、环路(前扣带回皮层(ACC)-mPFC通路)及分子(NR2A(Grin2a编码,NMDA受体的关键组成部分)介导的谷氨酸能高兴奋性)层面解析mPFC调控内脏痛的机制。这些机制发现直接指导了干预策略的优化,并使我们提出假说:通过低频rTMS(lf-rTMS)抑制mPFC过度兴奋可有效缓解内脏痛。最后,本研究将上述发现转化回临床,在表型明确的IBS-D患者队列中验证了靶向mPFC的rTMS方案的治疗潜力。综上所述,本研究构建了一条从临床观察到机制阐释再回归临床应用的完整转化路径,首次证实mPFC可作为IBS-D患者慢性内脏痛的重要神经调控靶点。
1.mPFC高兴奋性与IBS-D患者的内脏痛相关
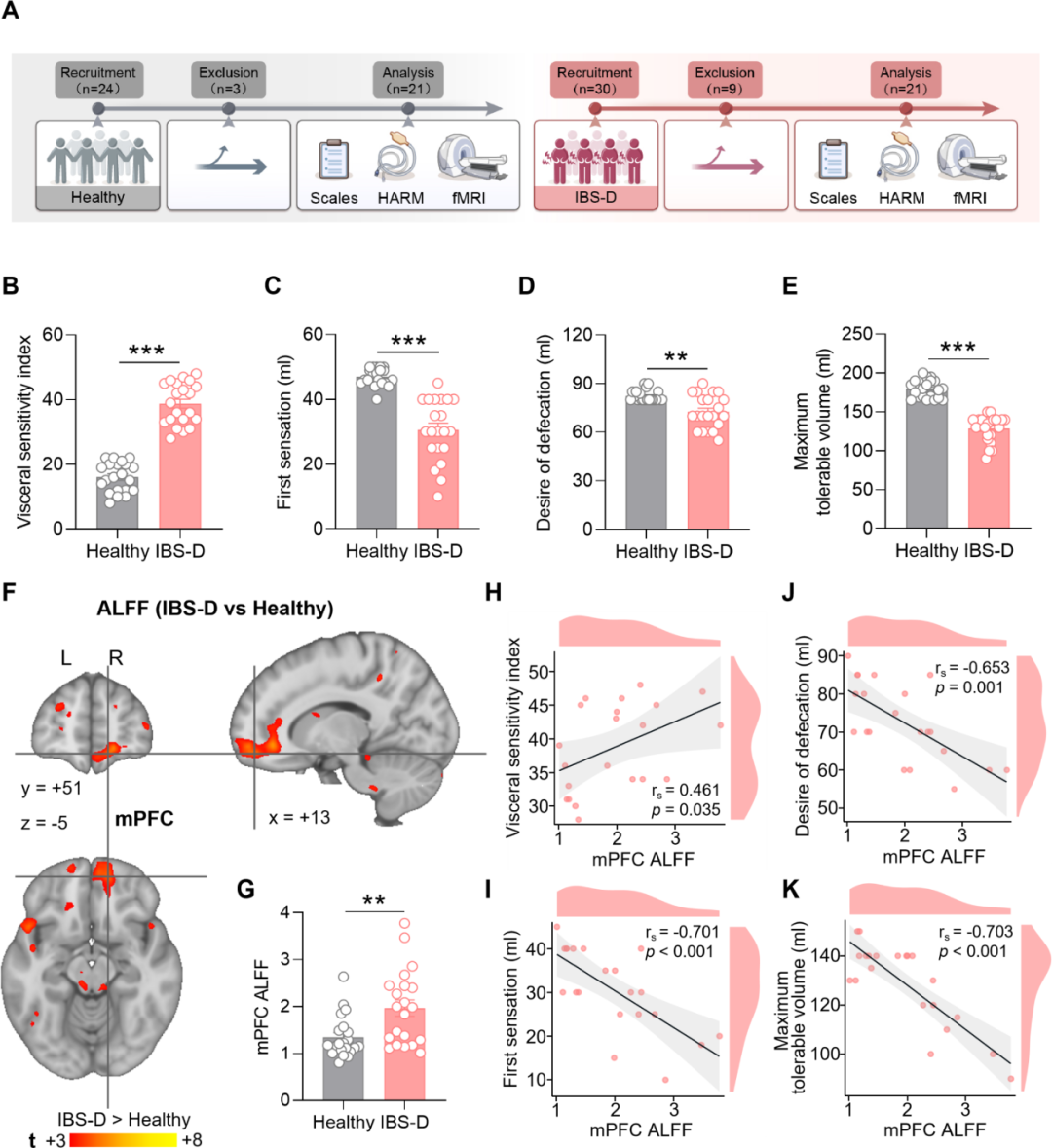
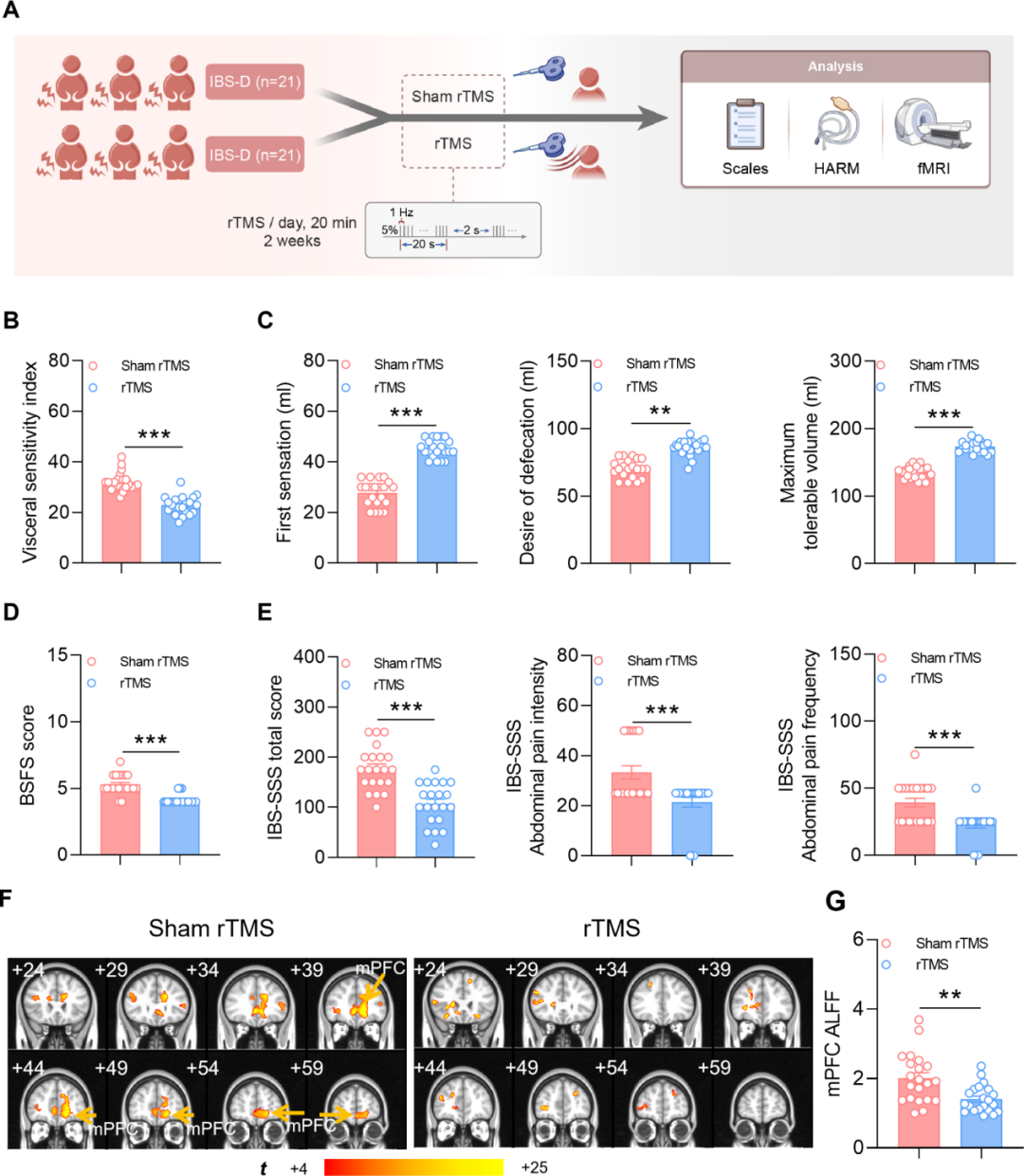
为系统鉴定持续过度兴奋且可作为IBS-D患者新型治疗靶点的脑区,本研究最终纳入21例IBS-D患者和21例健康对照者。与健康对照组相比,IBS-D患者的内脏敏感性指数(VSI)评分显著更高。肛门直肠测压结果进一步客观反映了这种内脏高敏感状态:与对照组相比,IBS-D组患者的直肠初始感觉阈值、排便欲阈值及最大耐受容量均显著降低。上述结果为IBS-D队列存在内脏痛敏增强提供了可靠证据。
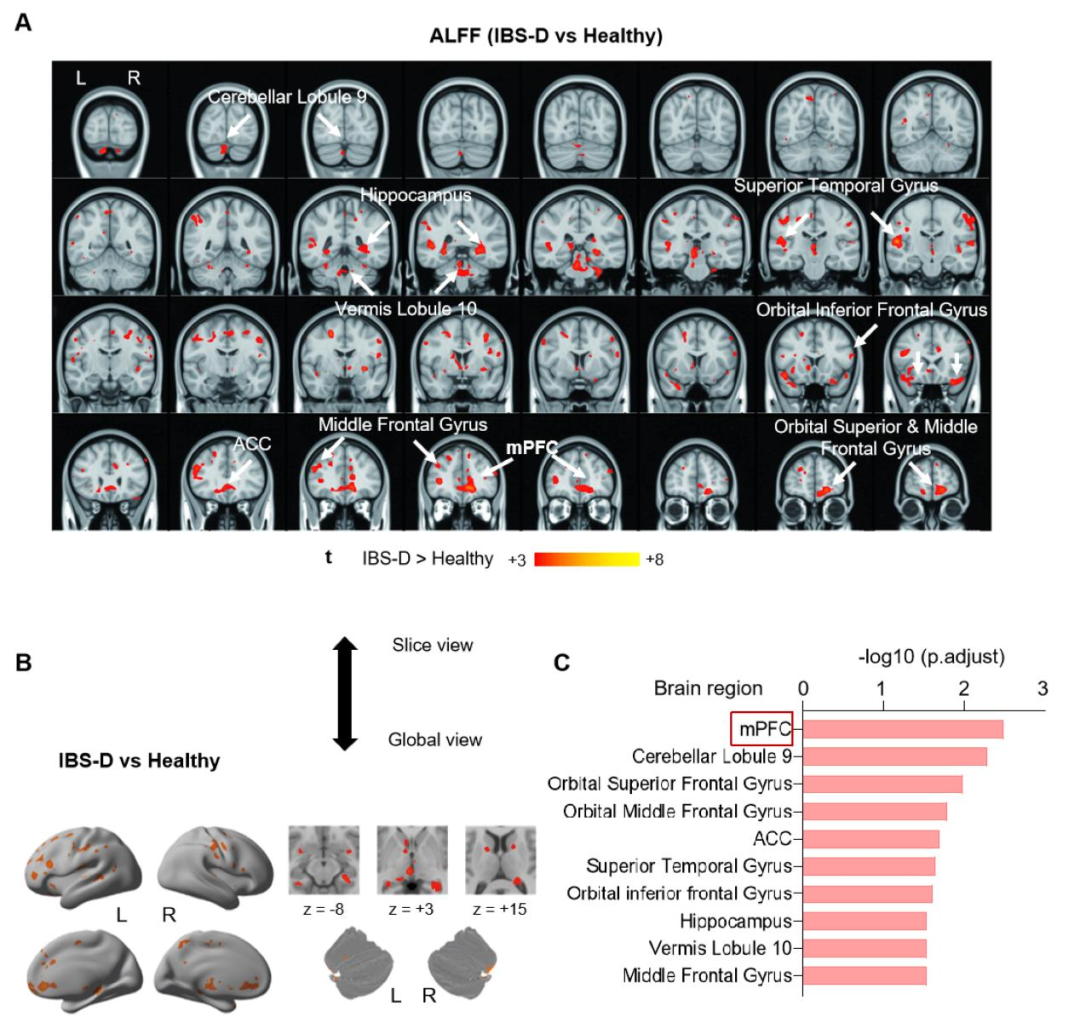
随后,通过功能磁共振成像(fMRI)分析反映脑区自发性神经活动的低频振荡振幅(ALFF)变化,探究该内脏高敏感状态的中枢神经机制。全脑分析显示,IBS-D患者多个脑区的ALFF显著升高,包括mPFC、小脑蚓9小叶、眶额上回、前扣带回皮层(ACC)、海马等(经错误发现率FDR校正的p<0.05;团块大小>50个体素)。值得注意的是,mPFC的ALFF升高幅度最为显著。相关性分析显示,IBS-D患者mPFC的ALFF与VSI评分呈正相关,与肛门直肠测压指标呈负相关。此外,还分析了VSI评分与其他脑区ALFF的相关性,结果显示其统计学显著性均低于mPFC。综上所述,这些发现强烈提示:mPFC高兴奋性是IBS-D患者内脏痛的中枢神经基础,有望成为IBS-D神经调控治疗的潜在靶点。
图1.mPFC高兴奋性与IBS-D患者的内脏痛相关
图2.IBS-D患者中神经活动发生改变的脑区
2.mPFCGlu神经元参与调控内脏痛
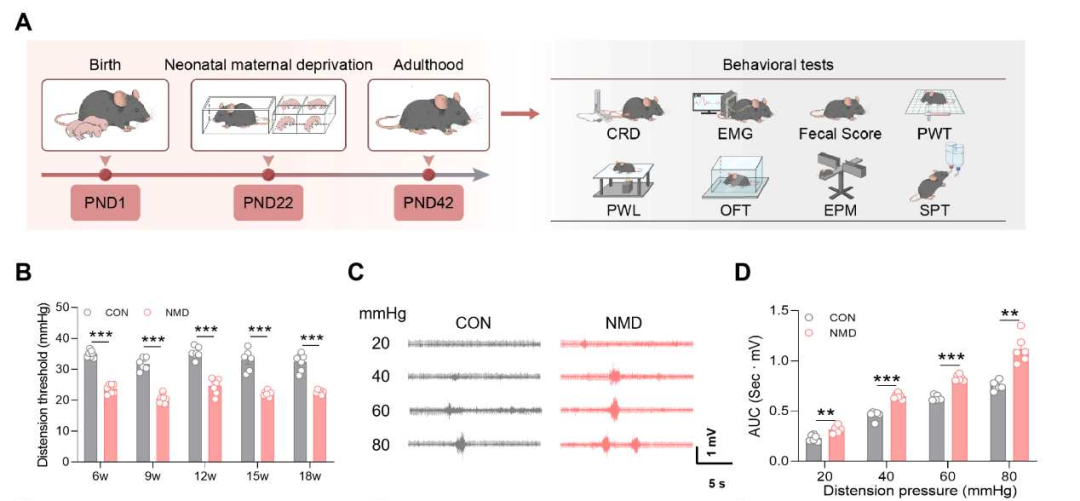
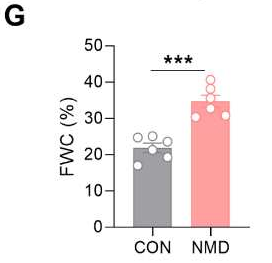
为明确mPFC兴奋性与内脏痛之间的因果关系,本研究采用了可模拟IBS-D相关慢性内脏痛的新生期母婴分离(NMD)小鼠模型。NMD小鼠的内脏痛反应显著增强,且该表型可持续至18周龄。值得注意的是,该模型小鼠躯体痛未见明显改变,提示其疼痛表型具有内脏特异性。与IBS-D患者临床特征一致,NMD小鼠还表现为粪便含水量(FWC)升高及焦虑样行为增强;而蔗糖偏好实验未见异常,提示其奖赏加工过程未受影响。
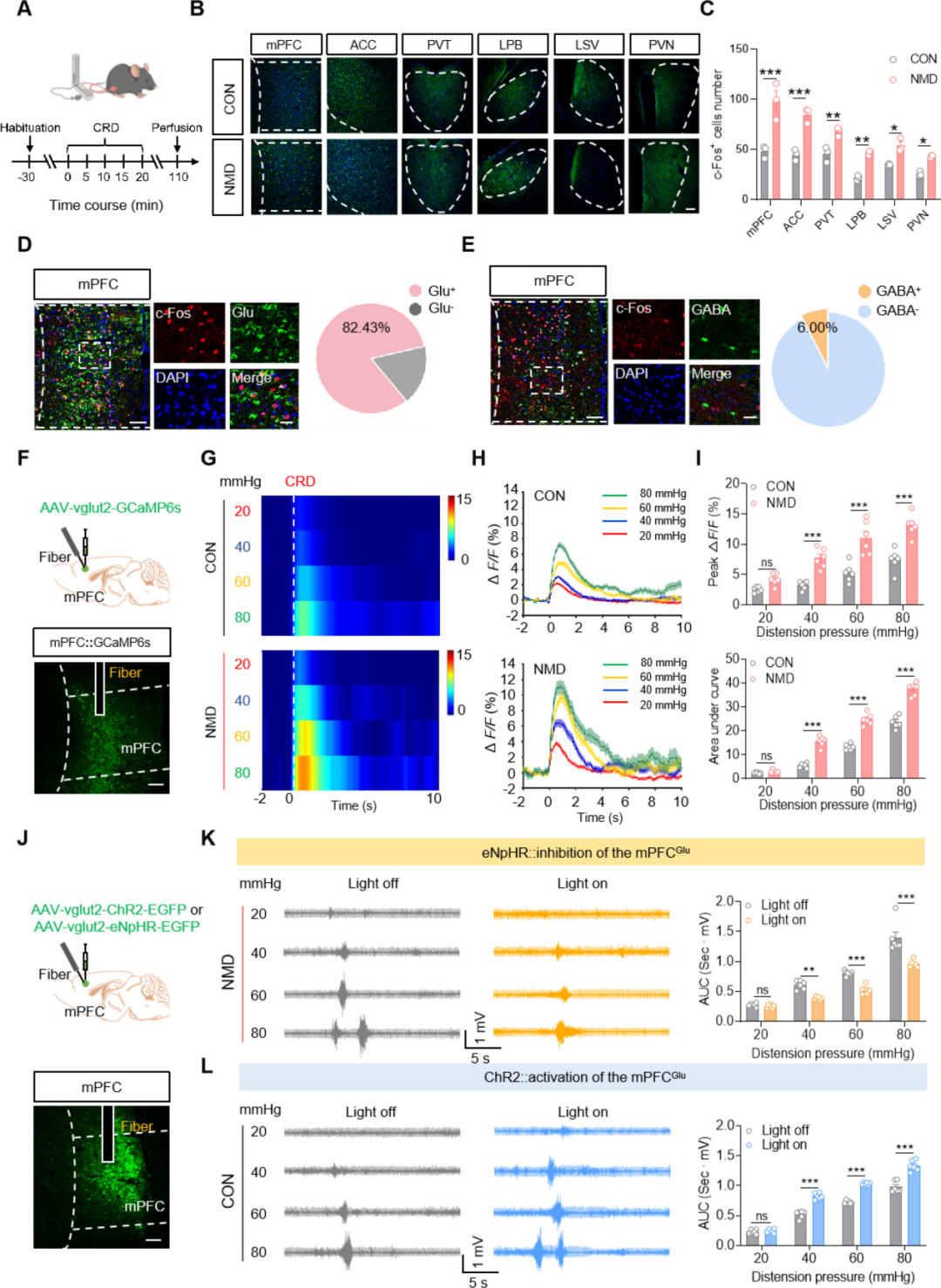
为鉴定被激活的特异性脑区,在结直肠扩张(CRD)刺激后对神经元活性标志物c-Fos进行免疫荧光染色,结果显示多个脑区被激活。值得注意的是,NMD小鼠mPFC区c-Fos表达显著升高,与人类神经影像学结果一致。进一步定量分析显示,CRD激活的mPFC神经元以谷氨酸能神经元为主:82.43%的c-Fos阳性细胞与谷氨酸共定位,仅6%与γ-氨基丁酸(GABA)共定位。上述结果提示,mPFCGlu神经元是内脏痛激活的主要神经元类型。
为直接实时观察内脏痛状态下该类神经元的活动,进行了在体光纤光度记录。结果显示,对结肠施加梯度压力刺激可诱发mPFCGlu神经元的钙信号活动,且NMD小鼠的钙依赖性荧光信号显著增强。
最后,为阐明mPFCGlu神经元在内脏痛中的调控作用,采用光遗传学技术调控mPFCGlu神经元活性,并通过肌电图(EMG)评估内脏痛反应。将表达谷氨酸能神经元特异性光敏感蛋白的病毒载体精准定位注射至mPFC后,共定位分析显示近81.7%的EGFP阳性细胞为谷氨酸能神经元。使用589 nm黄光抑制mPFCGlu神经元可显著缓解NMD小鼠的内脏痛;相反,采用473 nm蓝光激活mPFCGlu神经元则可诱导对照(CON)小鼠出现内脏痛相关行为。综上,上述结果证实mPFCGlu神经元参与调控内脏痛。
图3.NMD可诱导小鼠出现内脏痛与腹泻
图4.mPFCGlu神经元参与内脏痛的调控
3.前扣带回皮层输入对mPFCGlu神经元的兴奋作用是内脏痛的神经基础
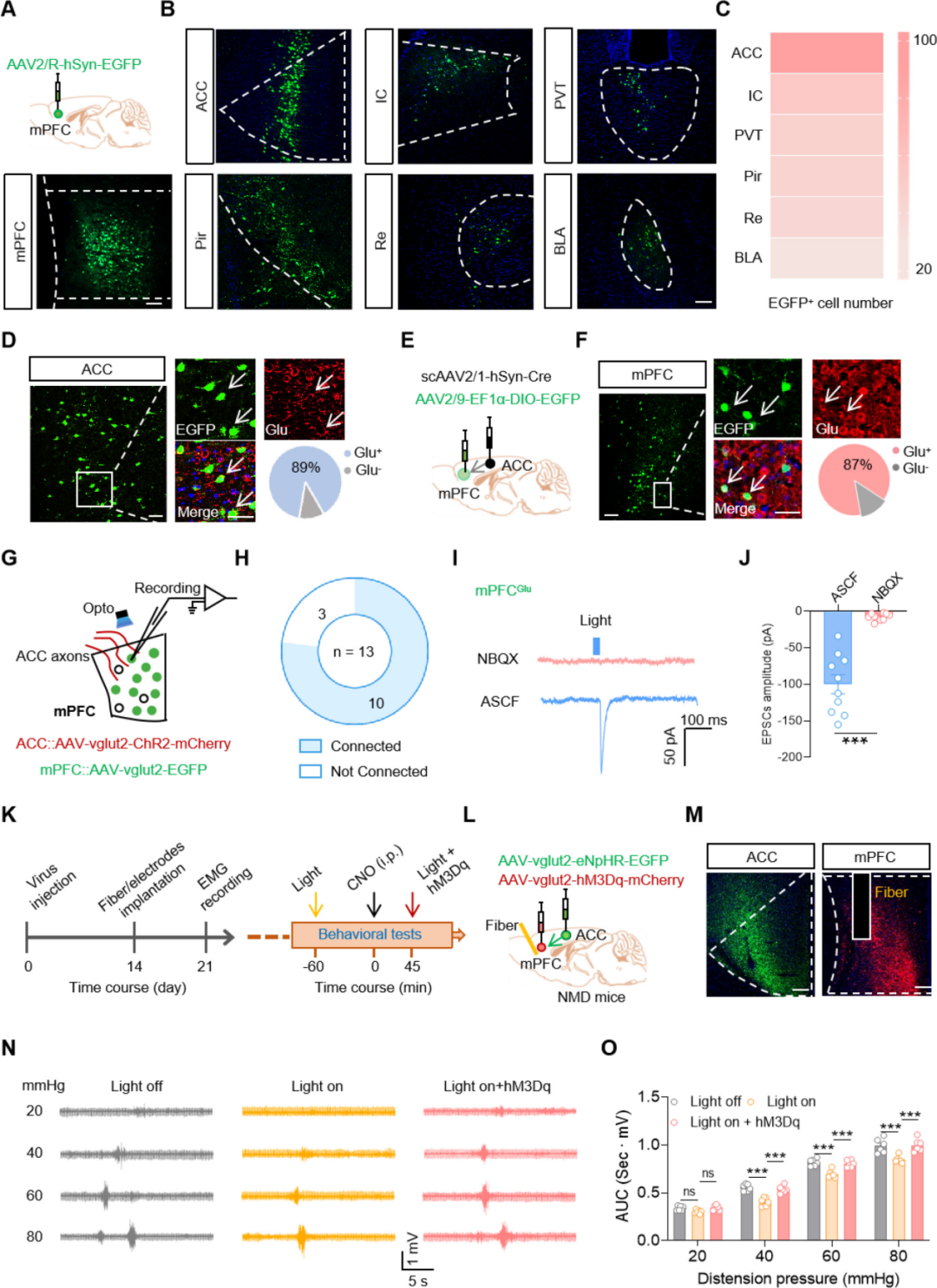
接下来,探讨了mPFCGlu神经元高兴奋性的内在机制。将逆行示踪病毒AAV2/R-hSyn-EGFP注射至mPFC,结果显示其接收来自多个脑区的主要神经输入,包括前扣带回皮层(ACC)、岛叶皮层、丘脑室旁核、梨状皮层、连结核以及基底外侧杏仁核。定量分析表明,ACC提供的神经输入最为丰富,且这些投射神经元主要与谷氨酸抗体共定位。此外,通过顺行单突触示踪策略进一步验证了ACC-mPFC神经环路:将AAV2/1-hSyn-Cre病毒注射至ACC,同时将AAV2/9-DIO-EGFP病毒注射至mPFC。病毒注射3周后,mPFC内绝大多数EGFP阳性神经元均与谷氨酸抗体共定位。对mPFC内表达ChR2的ACC谷氨酸能(ACCGlu)神经末梢进行光遗传学激活,可在mPFCGlu神经元上诱发出兴奋性突触后电流(EPSCs),该电流可被2,3-二羟基-6-硝基-7-氨甲基芴(NBQX)完全阻断。综上,上述结果表明ACCGlu神经元向mPFCGlu神经元发出兴奋性投射。
为进一步明确该通路在内脏痛调控中的功能作用,联合采用光遗传学与化学遗传学操控。具体而言,向NMD小鼠ACC注射AAV2/9-vglut2-eNpHR-EGFP,同时在mPFC注射AAV2/9-vglut2-hM3Dq-mCherry。光遗传学抑制mPFC内ACCGlu神经末梢可显著改善内脏痛相关行为。关键的是,这一镇痛效应可被CNO(氯氮平N-氧化物)介导的mPFCGlu神经元化学遗传学激活所阻断。上述结果证实,ACC-mPFC神经通路的激活是内脏痛相关行为表达所必需的。
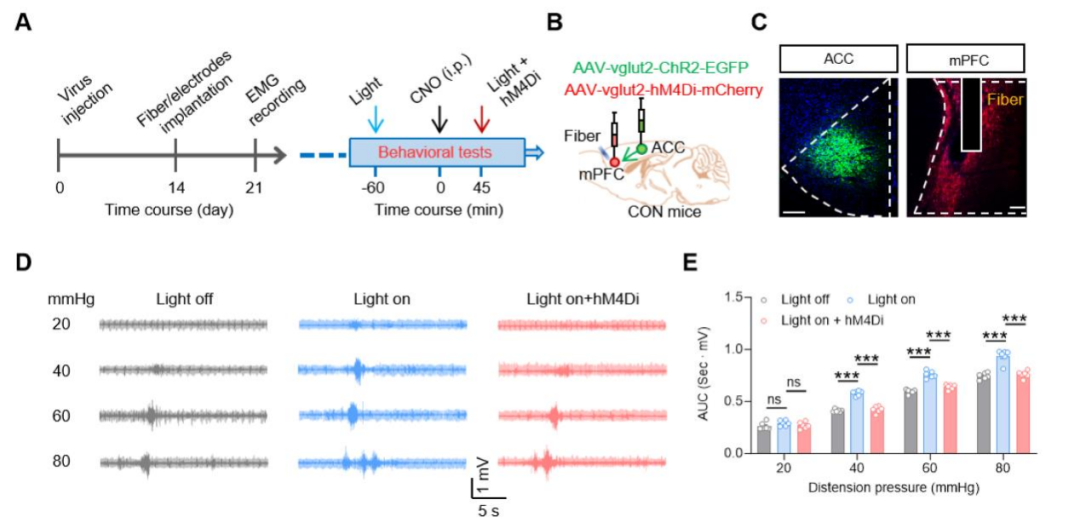
进一步验证了该通路调控的行为特异性。在光遗传学抑制ACC→mPFC通路的过程中,NMD小鼠的焦虑样行为、自发活动、机械痛阈、热痛阈及奖赏相关行为均未发生明显改变,证实该调控具有内脏伤害感受特异性。相反,在CON小鼠中,光遗传学激活mPFC内ACCGlu神经末梢可诱发内脏痛相关行为,而该效应可被CNO介导的mPFCGlu神经元抑制所逆转。
图5.ACC输入对mPFCGlu神经元的兴奋作用是内脏痛产生的重要机制
图6.ACCGlu-mPFCGlu环路的激活可诱导CON小鼠产生慢性内脏痛
4.抑制mPFCGlu神经元中的NR2A可缓解NMD小鼠的内脏痛
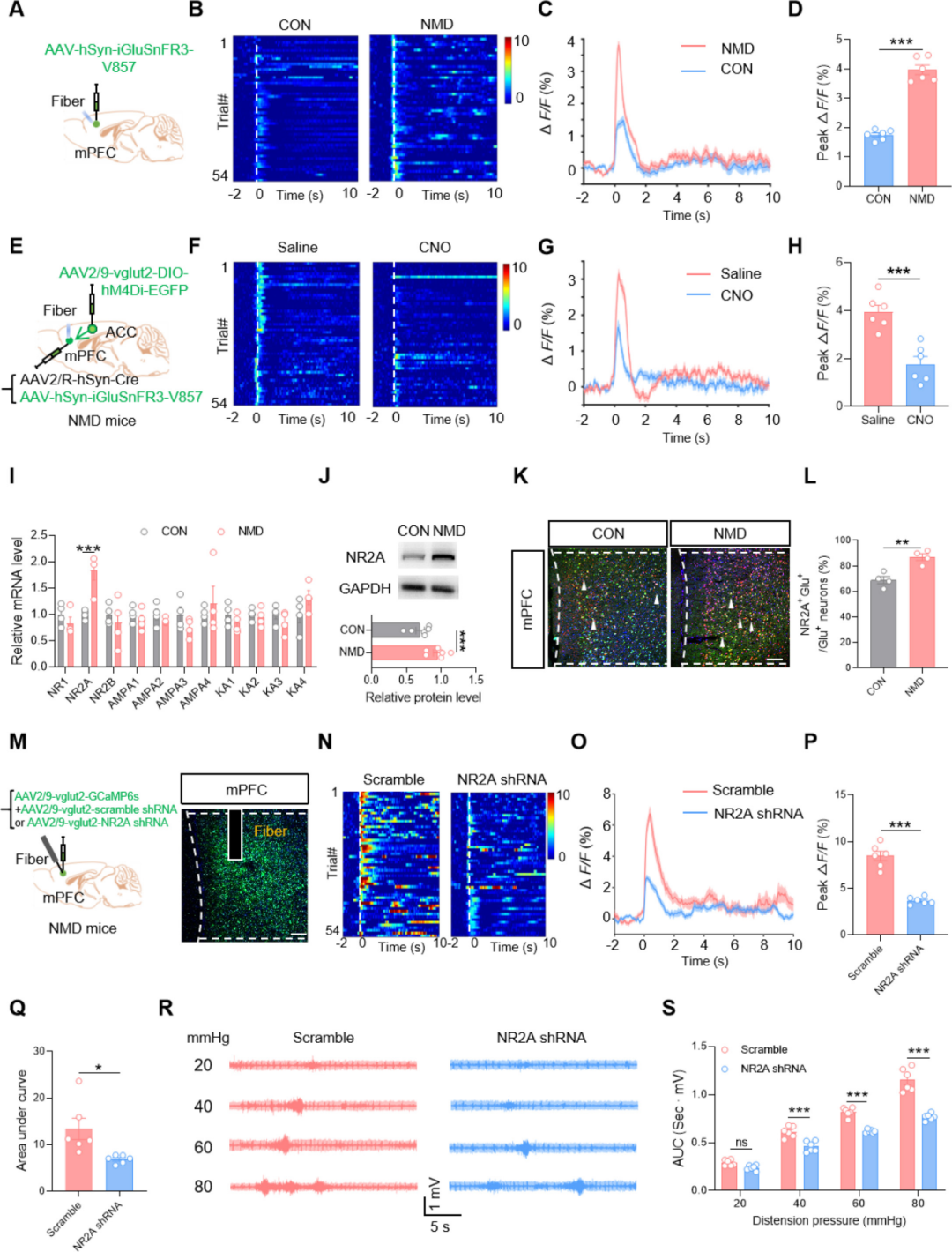
为阐明经ACC激活的mPFCGlu神经元在慢性内脏痛中的作用及机制,本研究利用病毒载体在mPFC中表达谷氨酸荧光探针(iGluSnFR3-V857)。光纤光度记录显示,与CON小鼠相比,CRD刺激可诱发NMD小鼠mPFC区谷氨酸释放量显著升高。为进一步验证这种升高的谷氨酸释放是否来源于ACC输入,采用化学遗传学方法抑制ACCGlu-mPFC通路。与生理盐水对照组相比,化学遗传学抑制该环路可显著降低CRD刺激期间的谷氨酸释放,证实ACC输入对mPFC的谷氨酸能张力具有关键调控作用。
鉴于谷氨酸的核心作用,随后检测了其受体(NMDAR、AMPAR、KAR)在mPFC中的表达谱。实时荧光定量PCR分析显示,NMD小鼠NMDAR的NR2A(Grin2a编码)亚基特异性上调,其他亚基无明显变化。通过蛋白质免疫印迹(WB)在蛋白水平证实了该上调,免疫荧光染色结果显示NR2A主要定位于mPFCGlu神经元中。
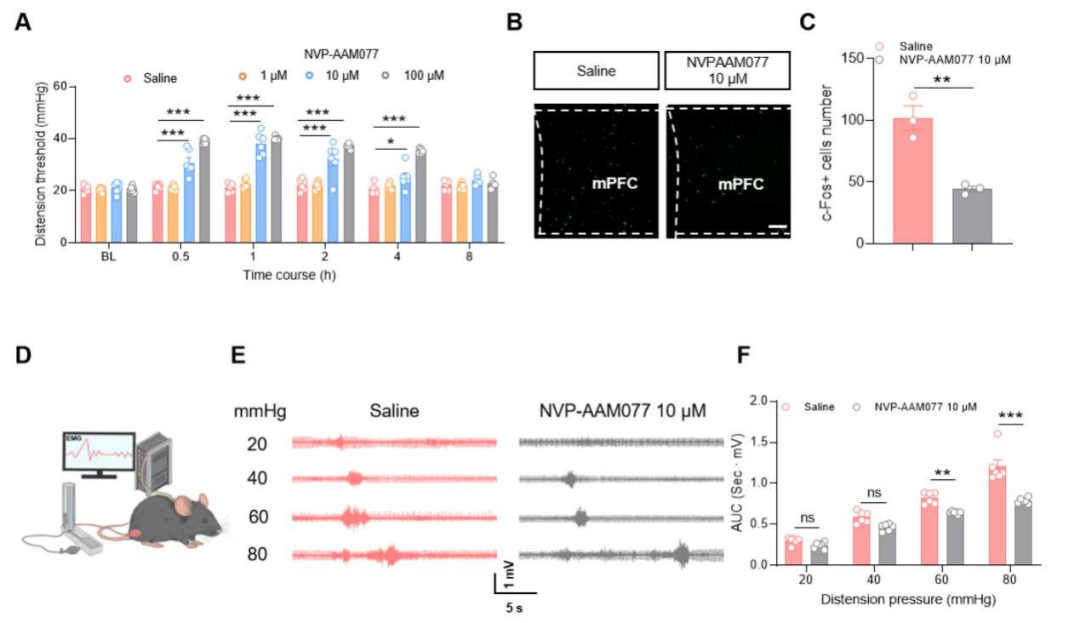
随后探讨了NR2A上调在内脏痛中的功能意义。结果显示,向mPFC内微量注射NR2A特异性拮抗剂NVP-AAM077(10 μM和100 μM)可显著缓解NMD小鼠的内脏痛。有效剂量10 μM NVP-AAM077还可降低CRD诱导的神经元激活,表现为c-Fos表达减少以及EMG记录中内脏痛反应减弱。
为进一步明确mPFCGlu神经元中NR2A是否参与调控内脏痛,本研究在该类神经元中特异性敲低Grin2a。结果显示,敲低mPFCGlu神经元Grin2a不仅可抑制CRD刺激诱发的神经元钙信号活动,还可显著改善NMD小鼠的内脏痛相关行为,提示NR2A上调是内脏痛病理性激活的关键分子基础。综上,本研究结果表明:mPFCGlu神经元中NR2A的表达上调,是介导NMD小鼠内脏痛发生的关键分子机制。
图7.抑制mPFCGlu神经元中的NR2A可缓解NMD小鼠的内脏痛
图8.NVP-AAM077以时间依赖性方式降低mPFC的活性
5.低频重复经颅磁刺激通过纠正mPFCGlu神经元高兴奋性及相关可塑性异常缓解NMD小鼠内脏痛
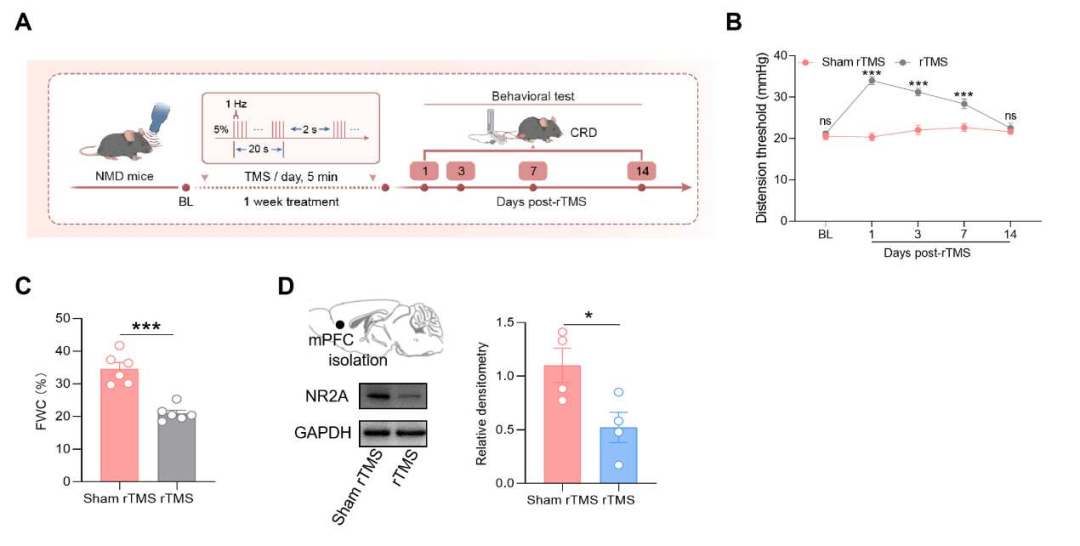
鉴于慢性内脏痛中观察到的mPFCGlu神经元过度活跃,本研究拟采用临床可行手段抑制mPFC,以实现成果转化。尽管靶向mPFC的重复经颅磁刺激(rTMS)已展现出临床应用前景,但其长期疗效(尤其是低频方案)的内在机制仍不明确。本研究首先证实,对NMD小鼠mPFC施加1 Hz低频(lf)rTMS连续干预1周,可显著升高内脏痛阈,且镇痛效应可维持7天。将干预疗程延长至连续2周后,其镇痛作用显著延长,痛阈升高可维持至治疗后42天,同时小鼠FWC亦得到明显改善。
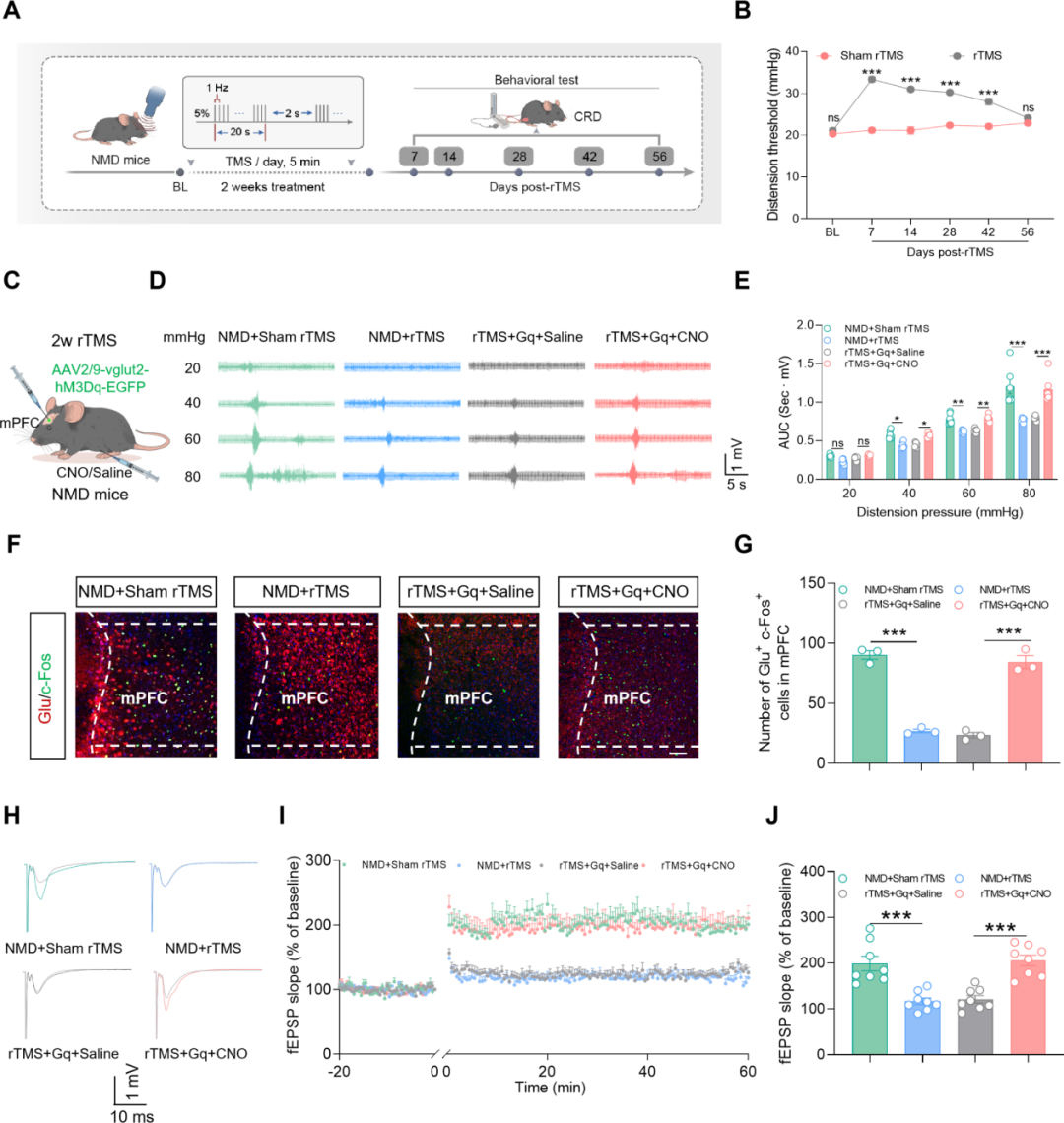
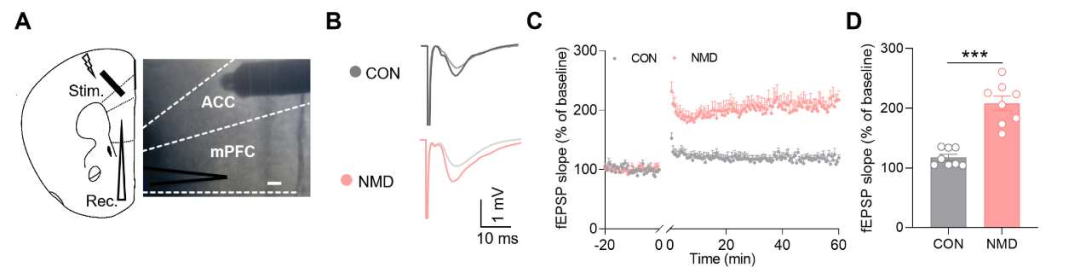
值得注意的是,化学遗传学激活mPFCGlu神经元可逆转lf-rTMS对内脏痛的改善作用,提示mPFCGlu神经元活性是lf-rTMS发挥内脏痛镇痛效应的关键。在观察到行为学改善后,评估了rTMS干预后的神经元活性。免疫荧光染色和WB结果显示,与sham rTMS组相比,lf-rTMS可显著降低mPFCGlu神经元c-Fos表达,并伴随mPFC内NR2A表达下降。此外,与生理盐水组相比,化学遗传学激活可显著提高mPFCGlu神经元的兴奋性,提示lf-rTMS通过降低mPFCGlu神经元兴奋性缓解内脏痛。随后,刺激ACC并同步记录mPFC区的长时程增强(LTP)。结果显示,NMD小鼠mPFC区LTP呈显著病理性增强;而lf-rTMS干预可将ACC诱发的mPFC异常LTP恢复至正常水平。化学遗传学激活mPFCGlu神经元则可逆转上述改善效应,使LTP无法恢复正常。上述结果表明,逆转异常突触可塑性增强,至少是lf-rTMS维持长期镇痛疗效的关键机制之一。
图9.lf-rTMS通过恢复NMD小鼠mPFCGlu神经元的正常兴奋性并改善其突触可塑性,从而缓解内脏痛
图10.rTMS可缓解NMD小鼠的内脏痛,并降低其mPFC中NR2A的表达
图11.与CON小鼠相比,ACC刺激可在NMD小鼠的mPFC中诱发出更显著的LTP
6.lf-rTMS通过降低mPFC神经元兴奋性,持续缓解IBS-D患者的内脏痛
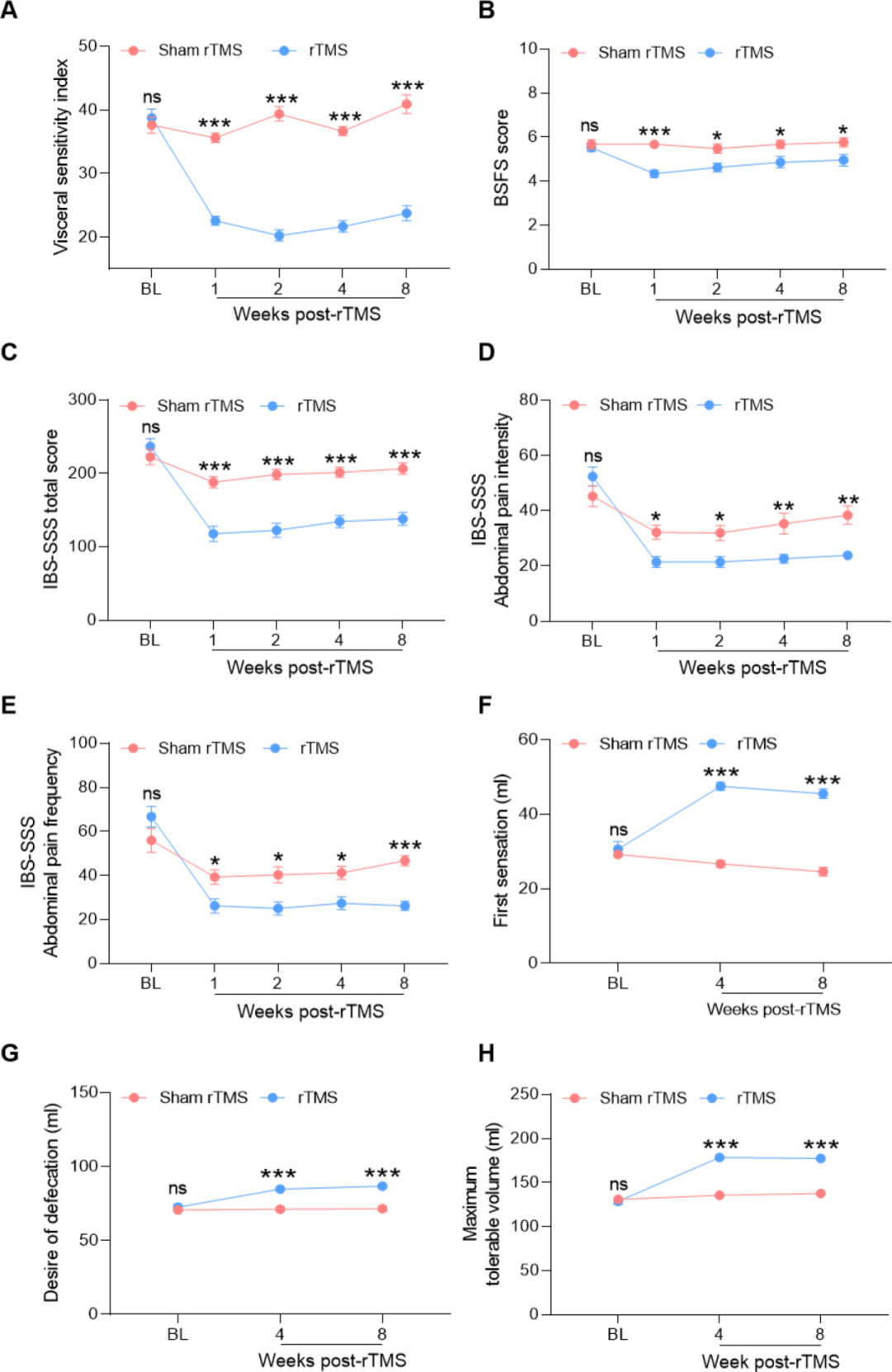
基于前期小鼠机制研究的结果,作者提出假说:mPFC可作为lf-rTMS干预人类患者的可行治疗靶点。为验证该假说,本研究将42例IBS-D患者按1:1比例随机分为两组,分别接受连续2周的伪刺激(sham)rTMS或靶向mPFC的lf-rTMS干预。结果显示,与sham rTMS组相比,lf-rTMS组在多个临床维度均表现出显著疗效。具体而言,lf-rTMS显著缓解了患者内脏痛,表现为VSI评分显著降低,以及直肠初始感觉阈值、排便欲阈值及最大耐受容量显著升高。此外,lf-rTMS还显著改善了患者的排便习惯(布里斯托大便性状量表(BSFS)评分降低)。在整体病情评估上,lf-rTMS组IBS症状严重程度评分系统(IBS-SSS)的总分及腹痛分项评分均较对照组显著下降,表明患者整体症状负荷得到有效减轻。机制研究发现,上述临床症状的改善伴随着mPFC区活动的显著降低(基于fMRI)。最后,为期8周的随访评估证实,该治疗效应在疗程结束后至少可维持8周。综上所述,本研究提供了强有力的临床证据,表明抑制mPFC的过度激活是缓解IBS-D患者慢性内脏痛的一种有效且长效的策略。
图12.lf-rTMS通过降低mPFC神经元兴奋性,缓解IBS-D患者的内脏痛
图13.lf-rTMS可对IBS-D患者的症状产生长效缓解作用
总结
综上所述,本研究不仅为阐释慢性内脏痛的中枢神经机制提供了全新的理论框架,更重要的是,为开发精准神经调控治疗策略奠定了关键基础。尤其值得关注的是lf-rTMS技术在慢性内脏痛治疗中的创新性应用,该技术通过调控mPFC功能发挥治疗效应,从而为临床实践提供了一种全新的非药物干预手段。上述研究成果具有重要的转化医学价值,为IBS及其他功能性胃肠道疾病的治疗开辟了新的研究方向。
本研究共同通讯作者为苏州大学神经科学研究所徐广银教授、苏州大学附属第一医院消化内科李锐教授;共同第一作者为苏州大学附属第一医院消化内科翁瑞霞博士、苏州大学神经科学研究所博士研究生林威。该研究得到国家自然科学基金、国家重点研发计划、江苏省自然科学基金等项目资助。徐广银教授与李锐教授课题组长期致力于内脏疼痛的神经环路机制研究,并积极推动基础研究成果向临床应用转化。
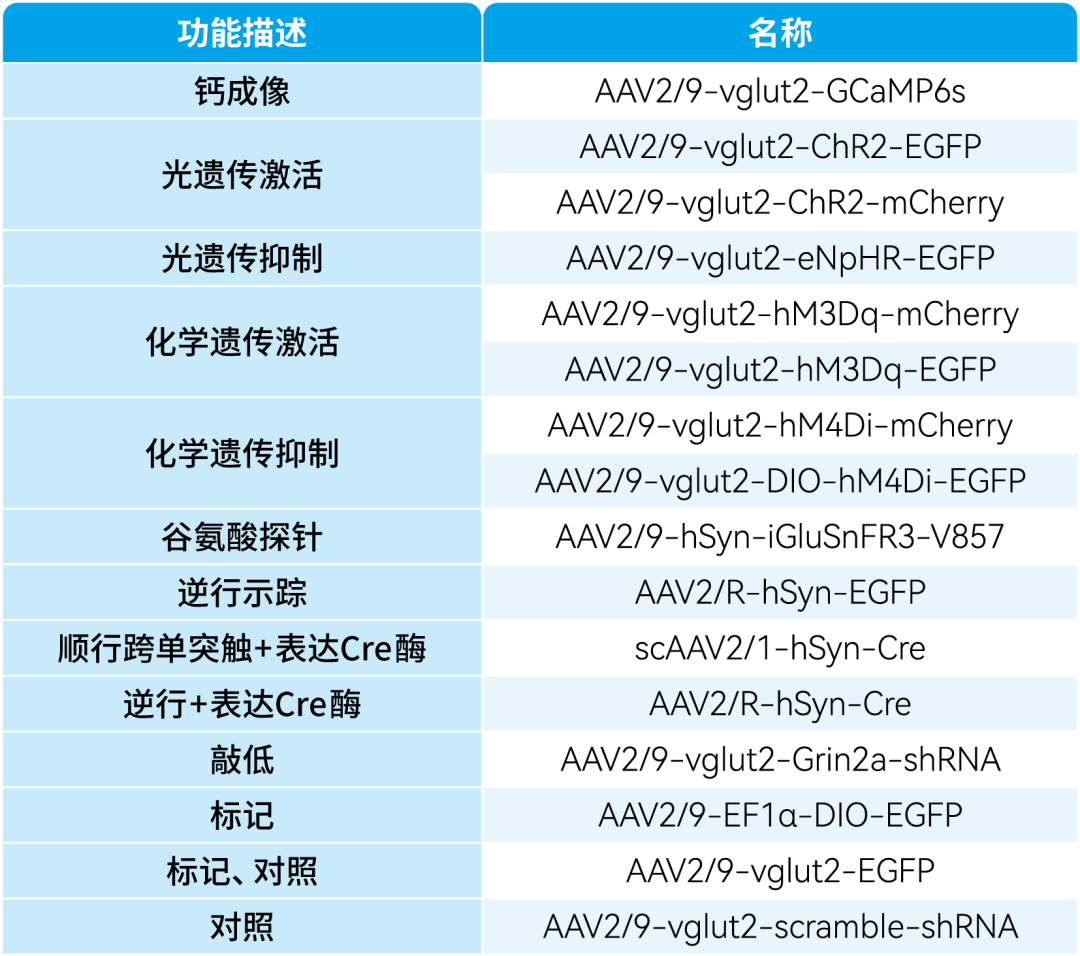
本文使用的病毒产品均来自枢密科技,列表如下:
扫码添加客服
更多产品及详情欢迎咨询!


市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK