2026-03-16 阅读量:230
社会隔离(SI)已成为21世纪日益严峻的公共卫生挑战。流行病学研究表明,SI是焦虑症的重要环境风险因素,长期孤独的个体焦虑易感性显著增高。然而,尽管慢性隔离已知会扰乱神经内分泌信号和边缘回路功能,但SI如何从分子层面驱动“社交缺失”向“病理性焦虑”的转化,仍是神经科学领域悬而未决的核心问题。现有研究为该领域提供了部分线索:一方面,铁作为神经元功能必需的微量元素,其稳态失调具有强神经毒性,不仅与帕金森病(PD)等神经退行性疾病密切相关,还会导致焦虑患者的海马体出现异常铁沉积;另一方面,α-突触核蛋白(α-Syn)作为PD病理核心蛋白,同时在突触调节和海马体抑郁机制中表现出多效性作用,可能与铁代谢存在双向交互作用;此外,糖皮质激素(GCs)作为机体主要应激激素,在SI个体中持续升高,且已知其可重塑海马体回路。但这些研究均为独立探索,尚未明确铁代谢与α-Syn在SI诱导焦虑中的协同作用,更未揭示三者(应激激素-铁-α-Syn)之间的分子关联及下游调控通路。
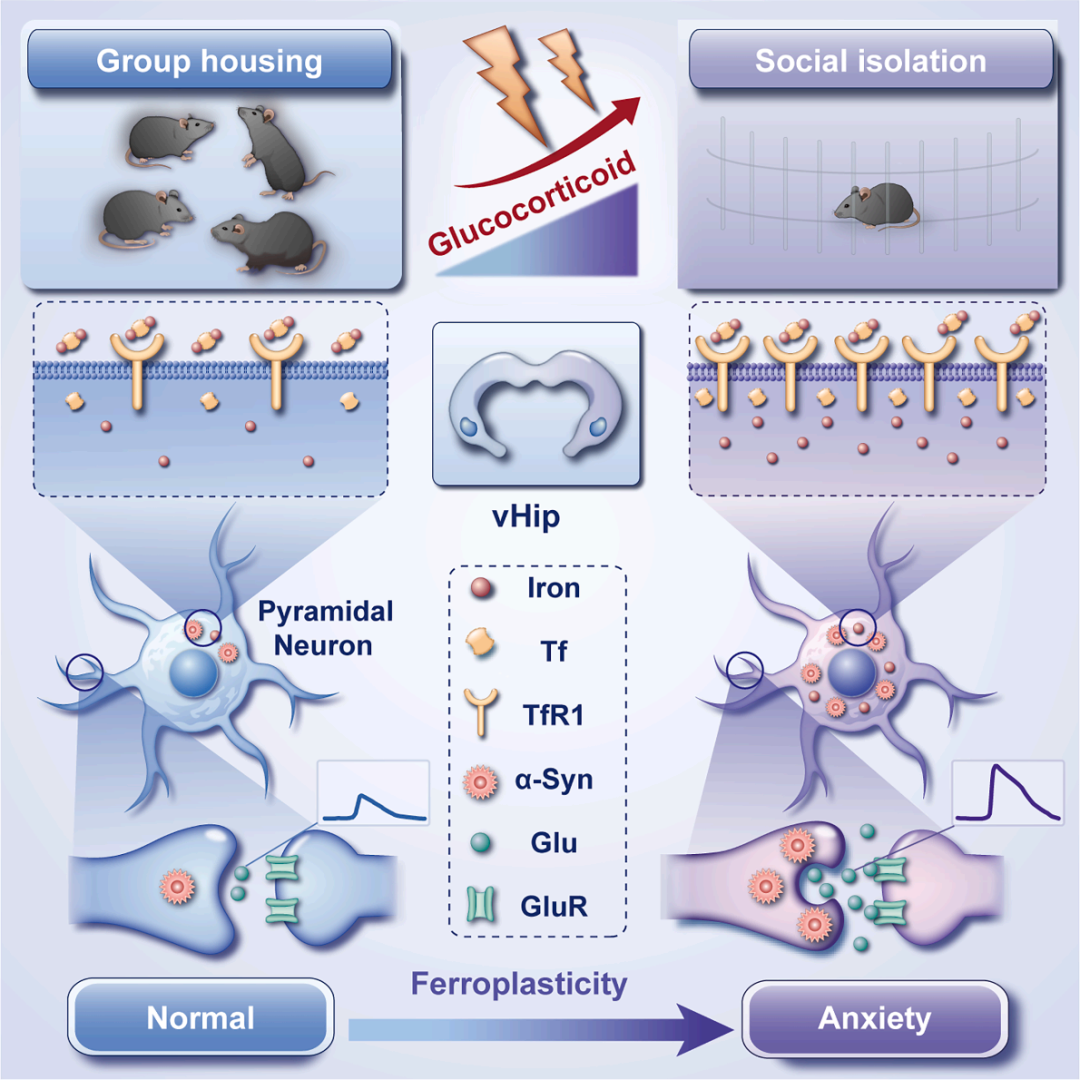
浙江大学王福俤教授/闵军霞教授、华南理工大学王卓副教授、南方医科大学邱平明教授/吕田明教授团队在《Cell Metabolism》发表的研究“Ferroplasticity drives social isolation-induced anxiety via a ventral hippocampal iron-α-synuclein axis”中提出“铁可塑性(Ferroplasticity)”这一新型突触重塑概念,并揭示了一条协调的GC驱动级联反应:SI通过升高GC激活腹侧海马(vHip)GC受体(GR),进而触发转铁蛋白受体1(TfR1)依赖性铁沉积,最终诱导α-Syn过表达。该金属生物学级联反应可增强突触前谷氨酸释放,导致vHip神经元过度兴奋,直接驱动焦虑样行为。在转化研究层面,经鼻递送铁螯合剂去铁胺(DFO)或α-Syn靶向反义寡核苷酸(ASOs)可正常化vHip神经活动并缓解焦虑。该研究不仅填补了社会应激诱导焦虑的分子机制空白,建立了脑铁代谢与情感障碍的直接关联,还开发了非侵入性经鼻给药策略,为焦虑障碍的临床治疗提供了可靠靶点与可行路径,具有重要的基础研究价值与转化潜力。
1、SI通过vHip神经元GR信号启动焦虑级联反应
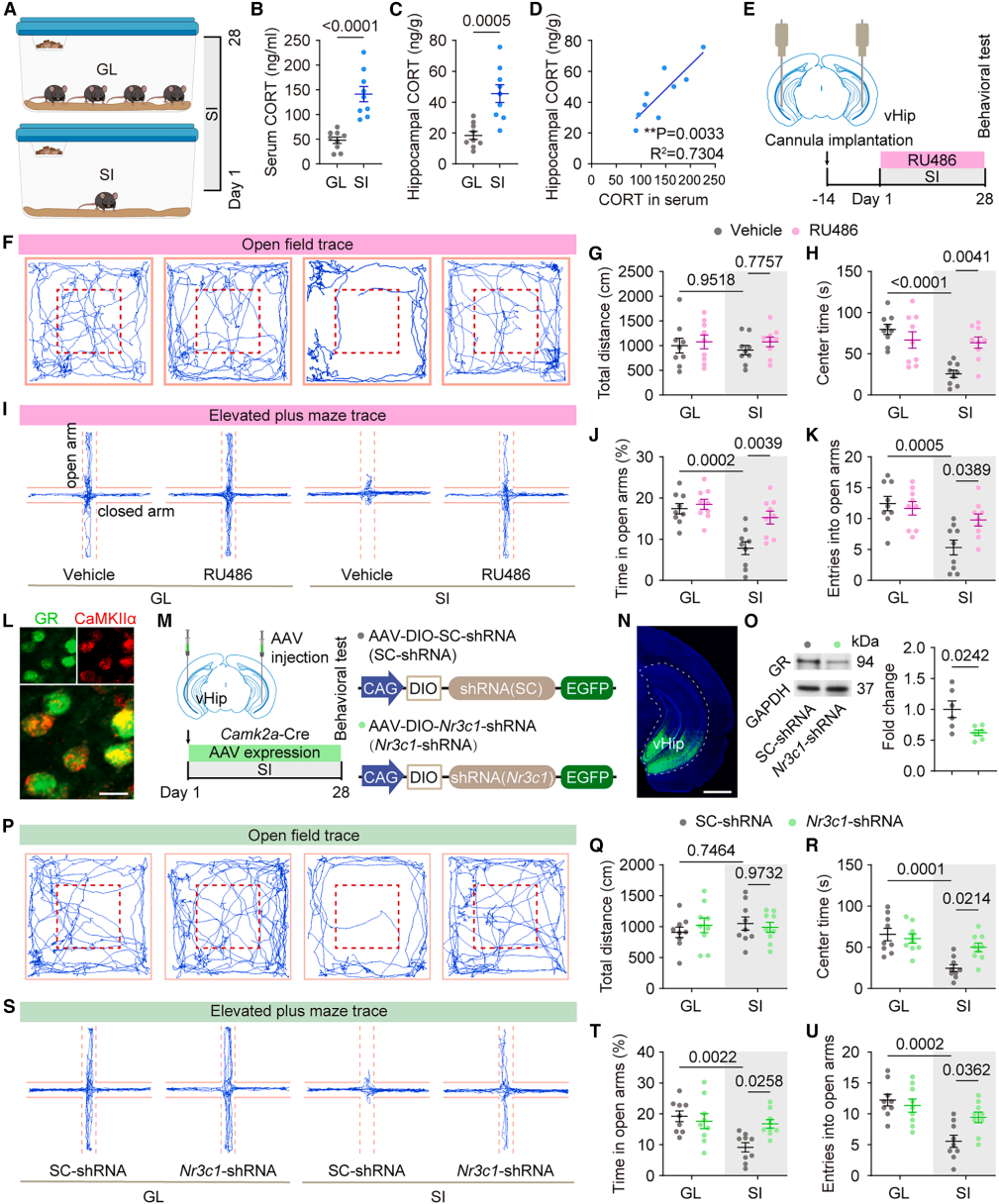
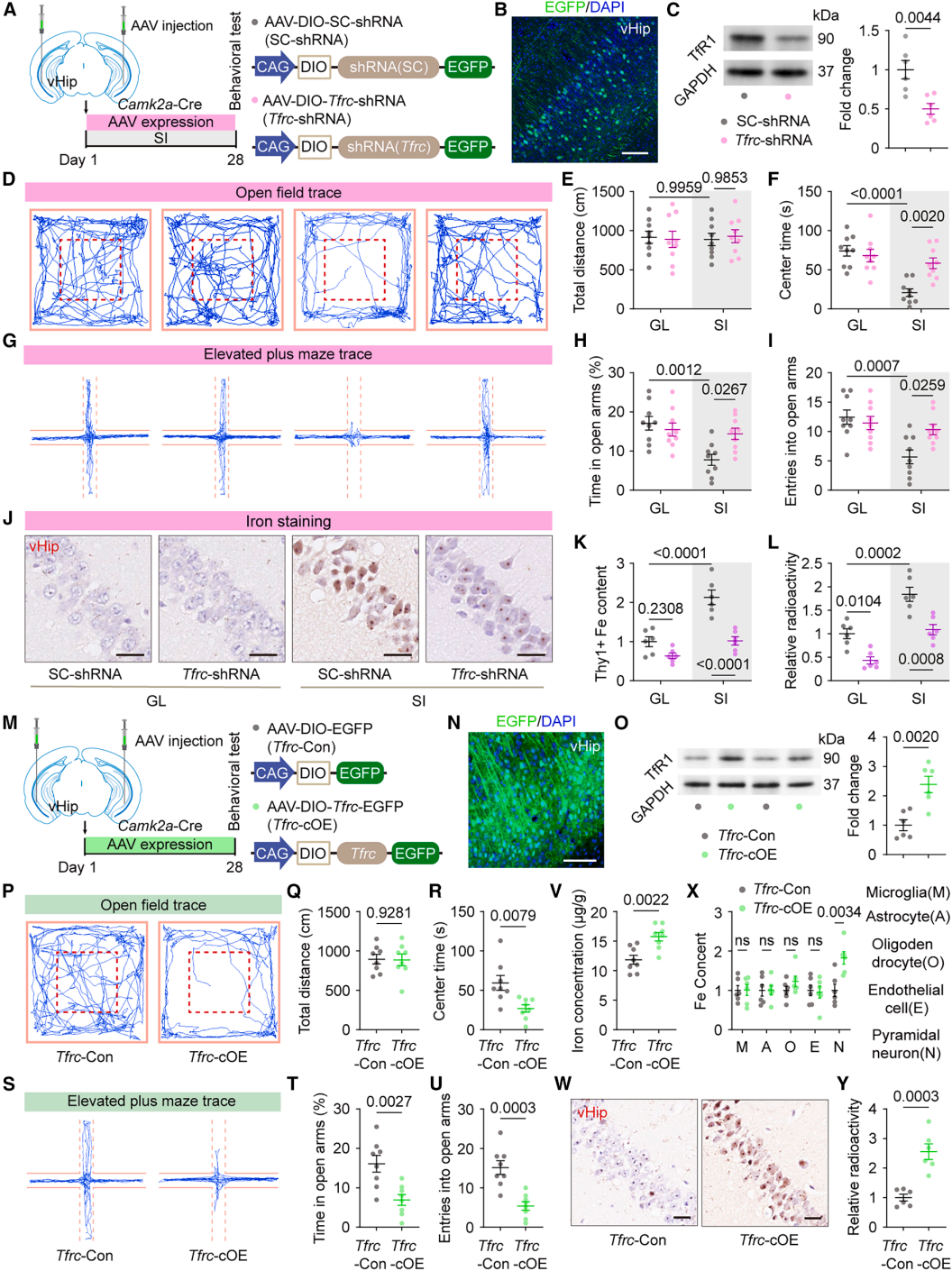
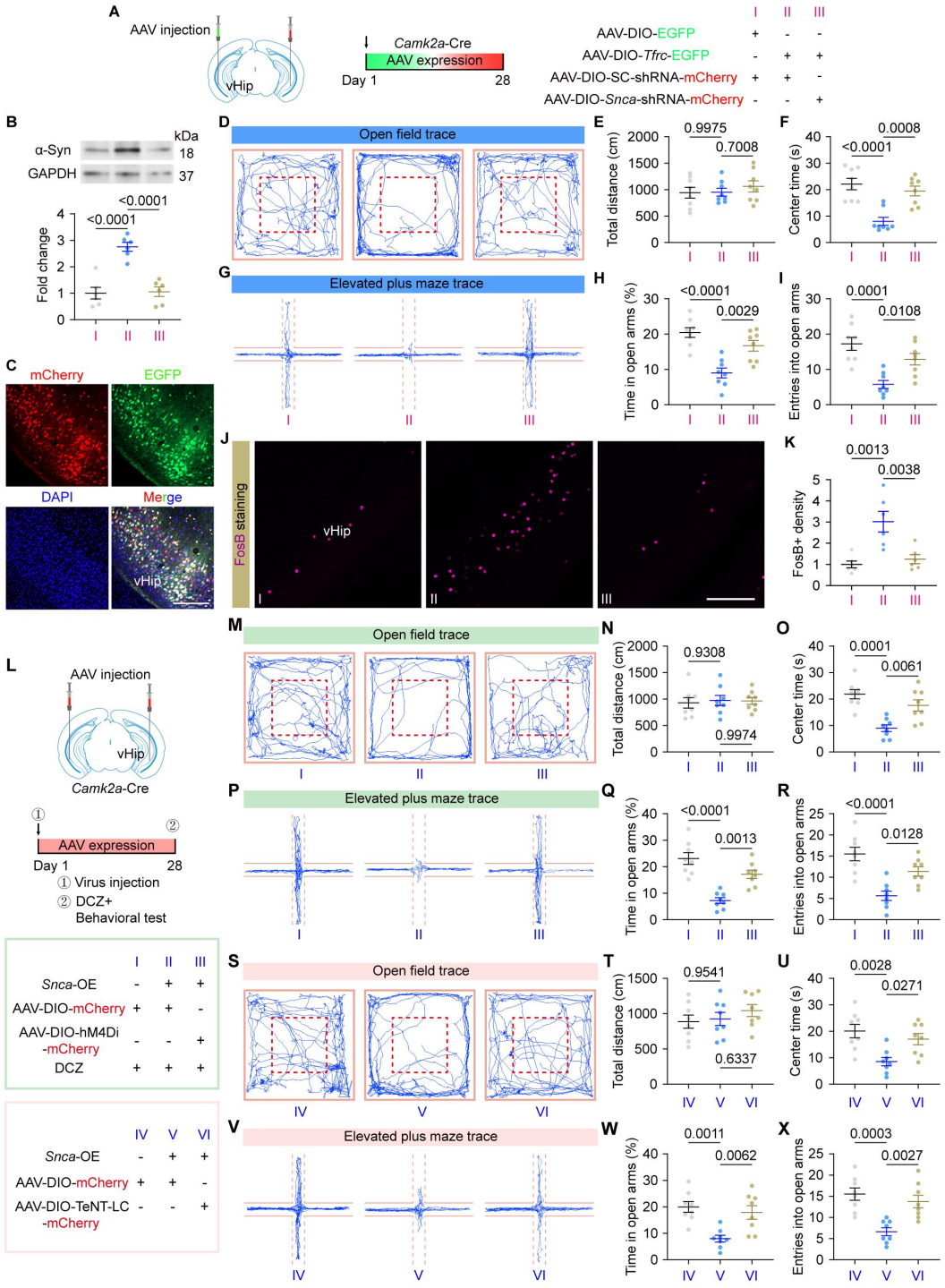
为明确SI诱导焦虑的上游分子开关,研究者建立4周SI小鼠模型,以群居(GL)小鼠为对照展开探索。行为学检测显示,隔离小鼠在旷场实验中中心区域停留时间显著缩短,在高架十字迷宫中开臂探索时间明显减少,表现出典型的焦虑样表型。同时,隔离小鼠血清和海马体中的皮质酮(CORT,小鼠体内主要的GC)水平均显著升高,两者呈强正相关,且海马体CORT水平与焦虑严重程度呈正相关。
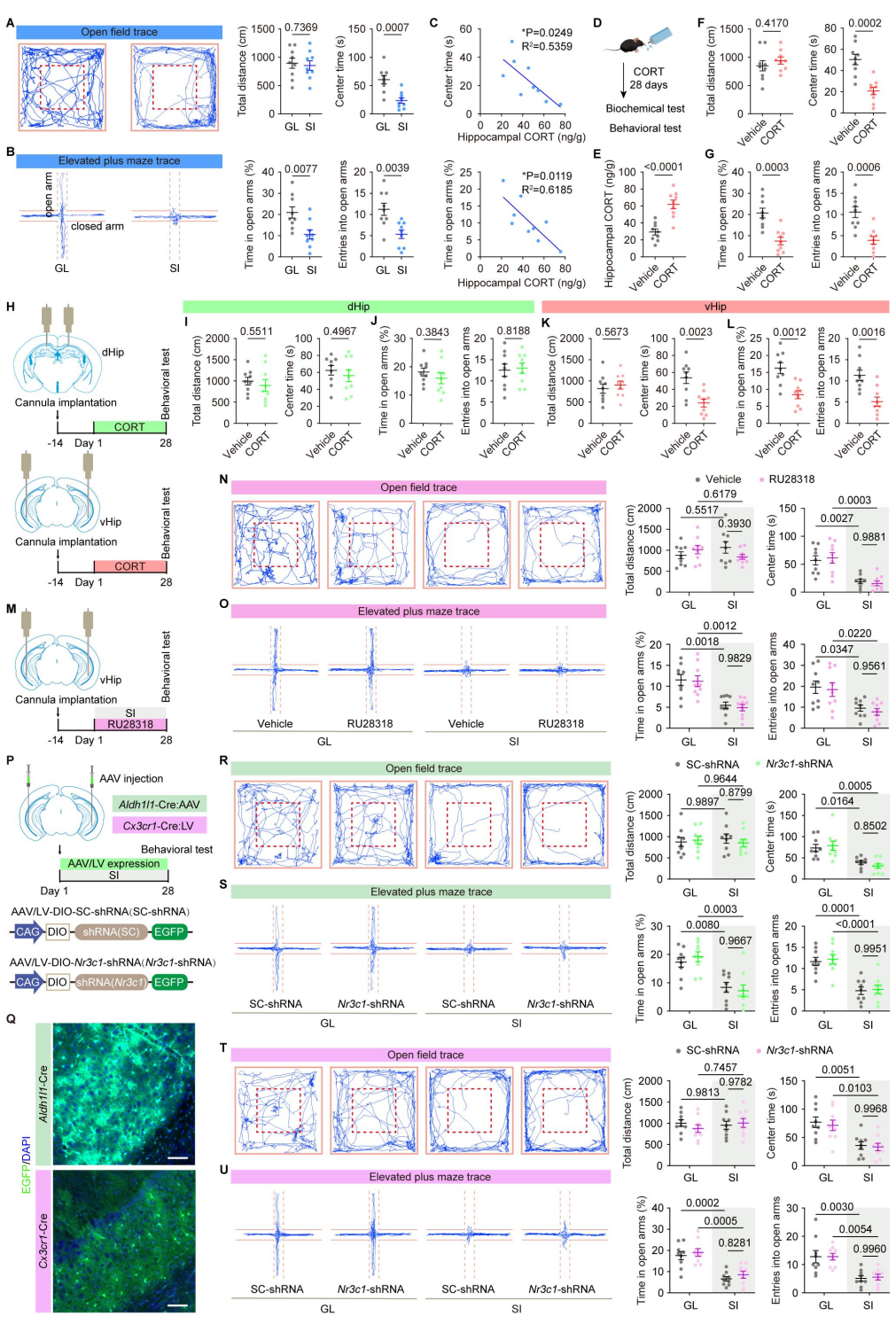
为验证脑区与受体特异性,研究者通过脑立体定位技术向vHip或背侧海马(dHip)输注外源性CORT,结果显示仅vHip输注可重现焦虑样行为;且vHip局部输注GR拮抗剂RU486能显著缓解SI诱导的焦虑,盐皮质激素受体(MR)拮抗剂则无此效应。免疫荧光显示GR在锥体神经元中表达,这支持将锥体神经元作为候选细胞底物进行后续研究。此外,仅锥体细胞靶向敲低GR编码基因Nr3c1可挽救焦虑,星形胶质细胞或小胶质细胞敲低无明显作用。这些结果证实,vHip神经元中的GR是SI诱导焦虑的关键介质。
图1. SI通过vHip神经元GR信号驱动焦虑样行为
2、GR-TfR1轴驱动SI诱导的vHip神经元铁过载
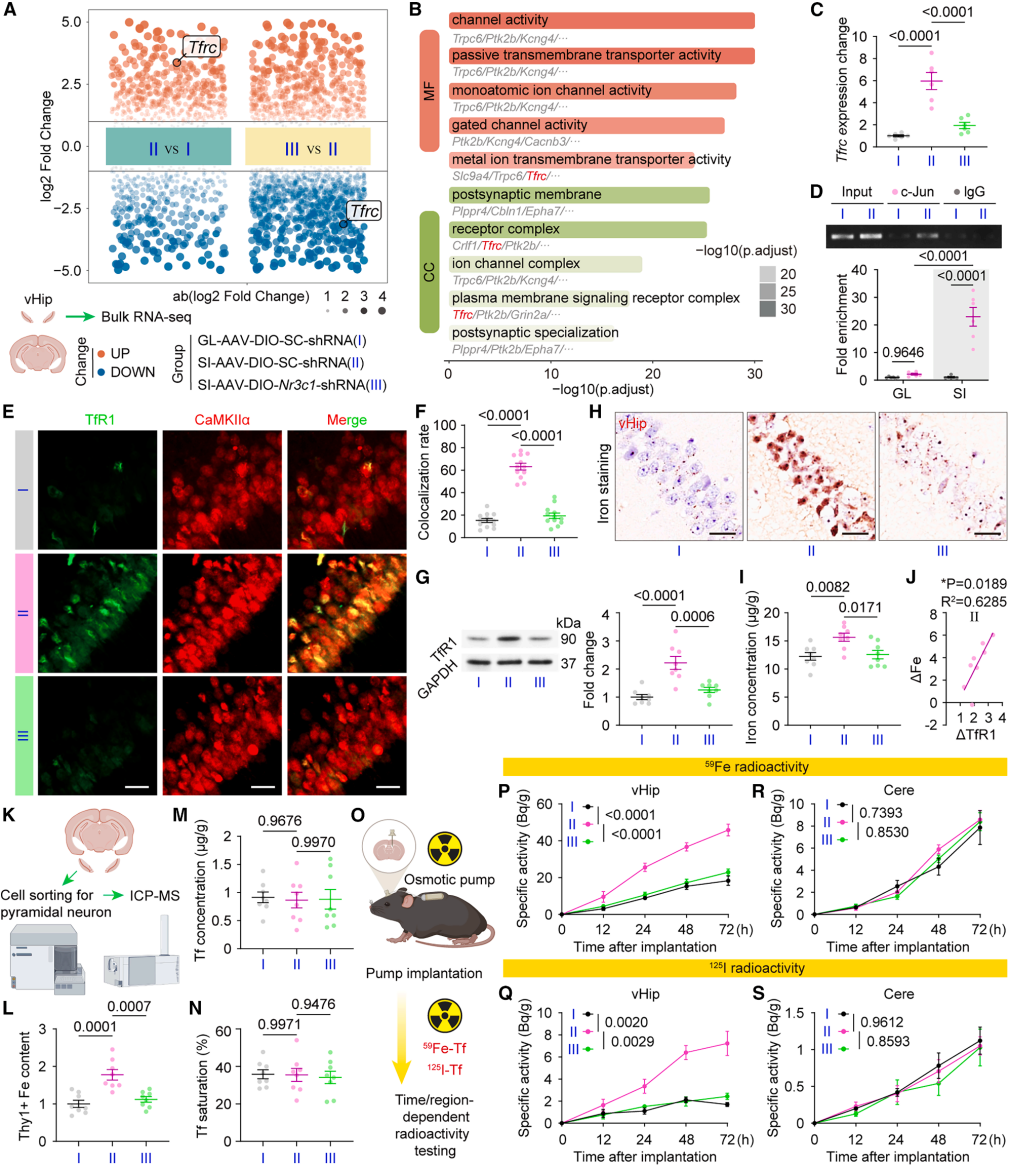
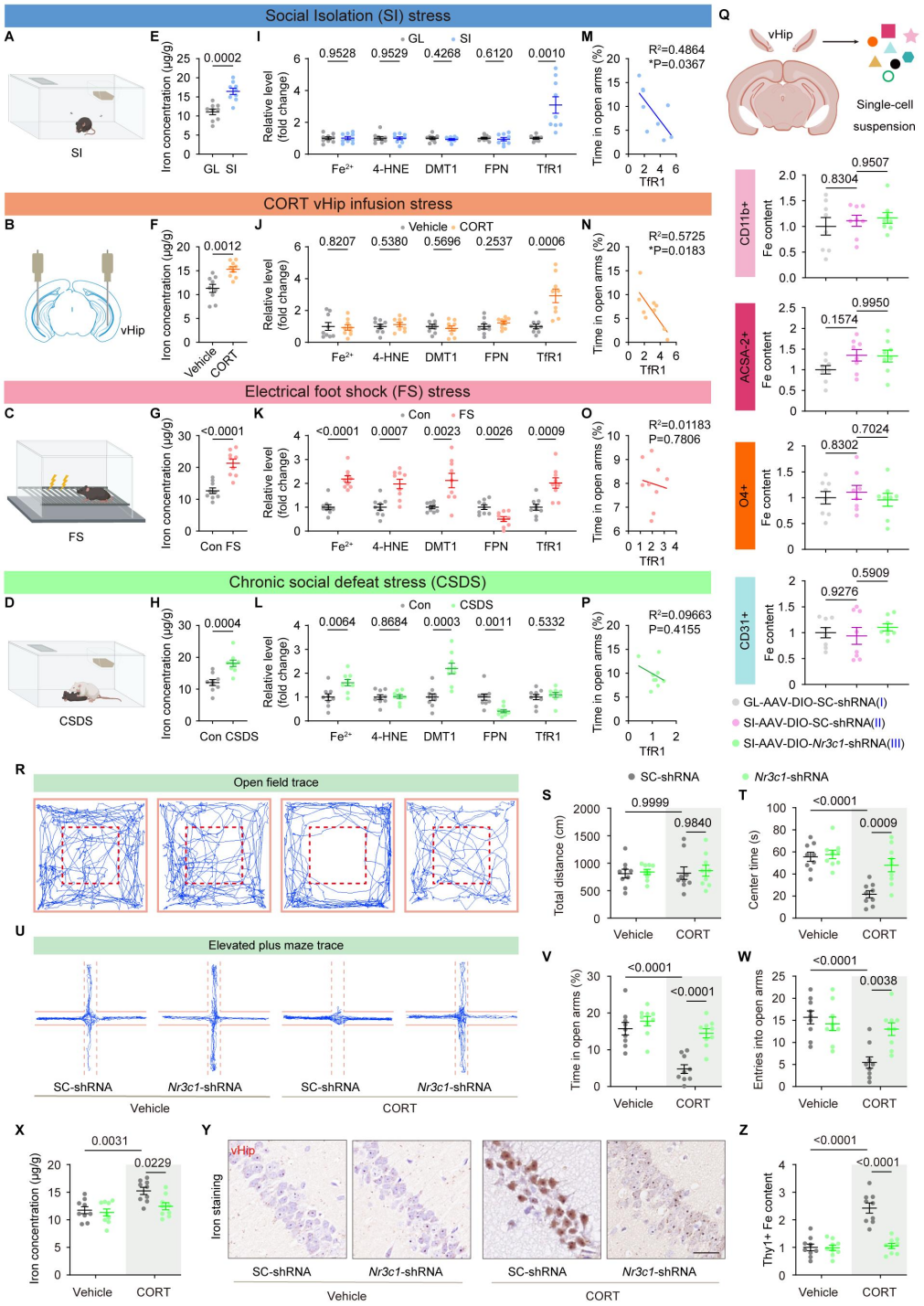
为鉴定GR下游的分子机制,研究者对锥体神经元特异性Nr3c1敲低隔离小鼠的vHip进行了RNA测序。结果显示,TfR1的编码基因Tfrc呈现GR依赖性上调。由于Tfrc近端启动子缺乏典型的GC反应元件(GRE),研究者通过染色质免疫沉淀(ChIP)实验发现,SI增强了转录因子c-Jun与Tfrc启动子的结合,而编码c-Jun的Jun mRNA本身也呈GR依赖升高。免疫荧光与蛋白质印迹(WB)检测进一步证实,SI小鼠vHip的TfR1蛋白水平显著升高,普鲁士蓝染色和生化分析显示铁含量同步增加,且两者呈正相关,而Nr3c1敲低可完全逆转上述变化。流式细胞术结合定量电感耦合等离子体质谱法(ICP-MS)分析进一步明确,铁沉积特异性发生于vHip神经元且呈GR依赖性,其他神经胶质细胞和内皮细胞未受影响;⁵⁹Fe-Tf/¹²⁵I-Tf放射性示踪实验显示,SI小鼠vHip的铁摄取量显著增加,Nr3c1敲低可有效抑制该效应。这些数据表明,SI激活vHip神经元GR信号后,通过c-Jun介导的转录调控上调TfR1表达,增强神经元铁摄取功能,最终导致特异性铁过载,GR-TfR1轴是连接SI与vHip神经元铁沉积的关键分子通路。
图2. SI通过GR依赖的TfR1上调驱动vHip神经元铁过载
图3. 应激诱导的vHip细胞特异性铁变化及神经元GR的治疗性靶向
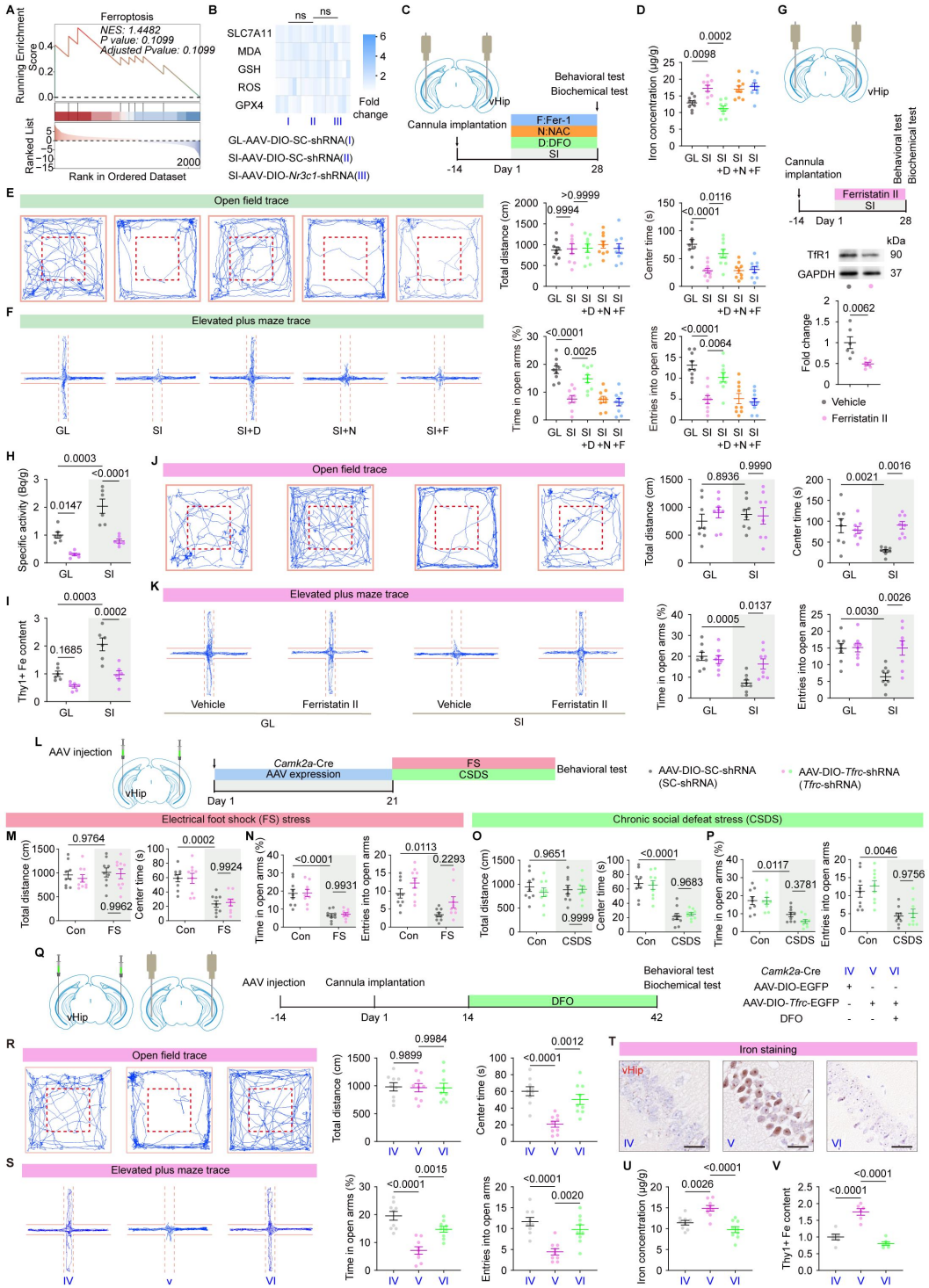
3、vHip锥体神经元TfR1通过铁依赖性、非铁死亡机制驱动SI诱导的焦虑
为确立TfR1的因果作用,研究者对vHip锥体神经元进行了Tfrc敲低与过表达。首先排除铁死亡参与:对vHip转录组和关键生化标志物的分析显示,SI小鼠中无铁死亡激活的证据,铁死亡抑制剂(Fer-1、NAC)不能缓解焦虑,而铁螯合剂DFO可预防焦虑,证明SI诱导焦虑的机制为铁依赖性但非铁死亡。此外,神经元特异性Tfrc敲低显著减轻隔离诱导的焦虑,并减少vHip铁沉积及铁摄取。值得注意的是,该干预对足底电击或社会挫败诱导的焦虑无效,提示机制对SI具有特异性。相反,vHip锥体神经元中Tfrc的过表达足以诱导焦虑,增加铁沉积与铁摄取;而同时vHip输注DFO可阻断上述效应,证明TfR1的致焦虑作用严格依赖于其介导的铁沉积。这些结果表明,vHip锥体神经元TfR1为SI诱导焦虑的必要且充分的上游驱动分子。
图4. vHip锥体细胞特异性Tfrc基因调控双向调节SI诱导的铁沉积与焦虑样行为
图5. vHip中TfR1介导的铁稳态失调通过非铁死亡机制促进SI诱导的焦虑
4、SI通过vHip铁-α-Syn轴驱动焦虑
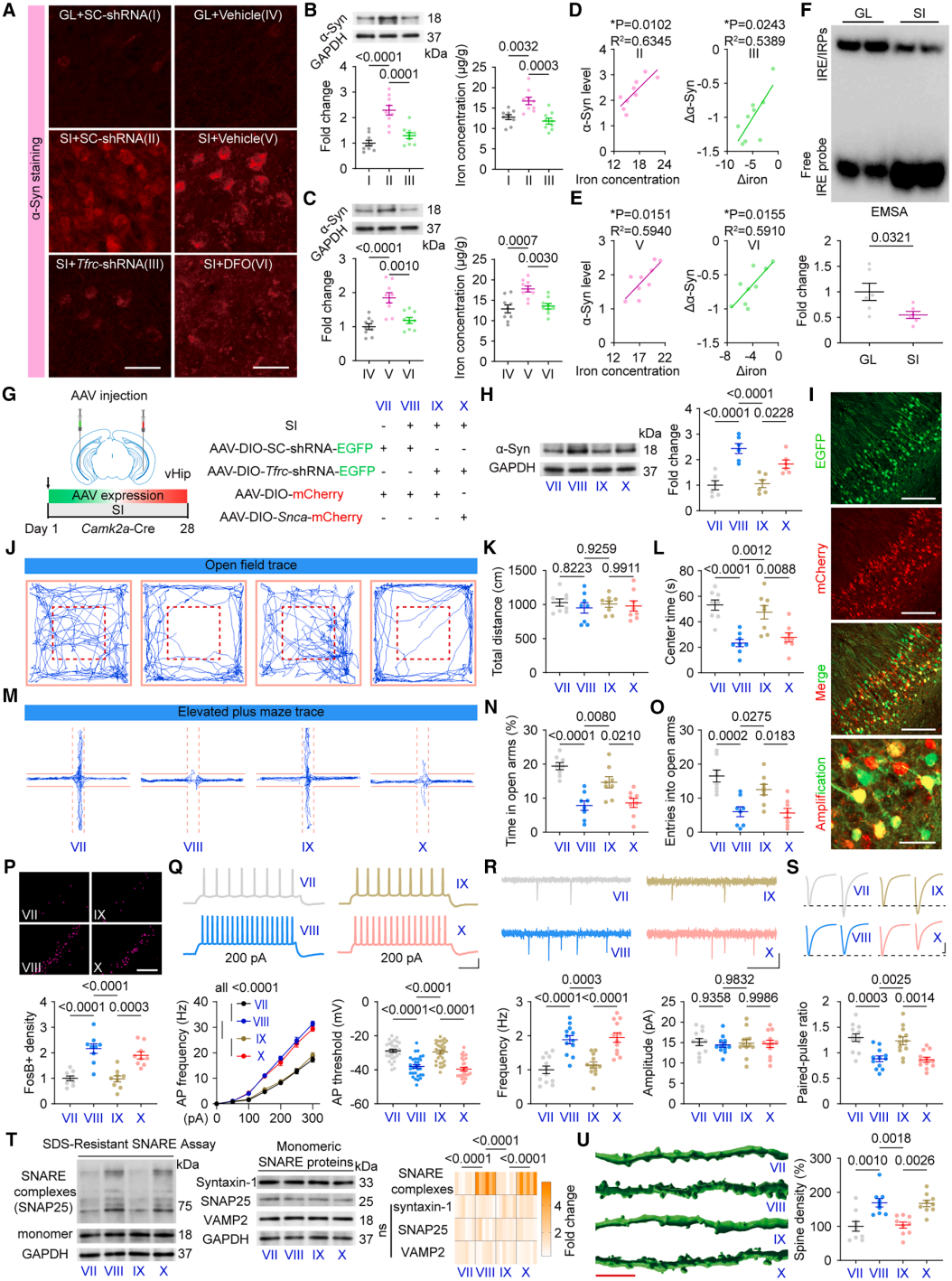
为探究铁过载下游效应物,研究者关注到α-Syn。既往研究表明,α-Syn与铁代谢存在双向调控关系,且编码α-Syn的Snca mRNA的5'非翻译区含有一个铁反应元件(IRE)。免疫荧光与WB显示,SI显著上调vHip中α-Syn的表达,该效应可被Tfrc敲低或铁螯合剂DFO干预逆转,且vHip铁含量与α-Syn水平呈强正相关。另外,RNA电泳迁移率变动分析(EMSA)证实,SI通过减弱铁调节蛋白(IRPs)与Snca IRE的结合,解除翻译抑制以上调α-Syn。
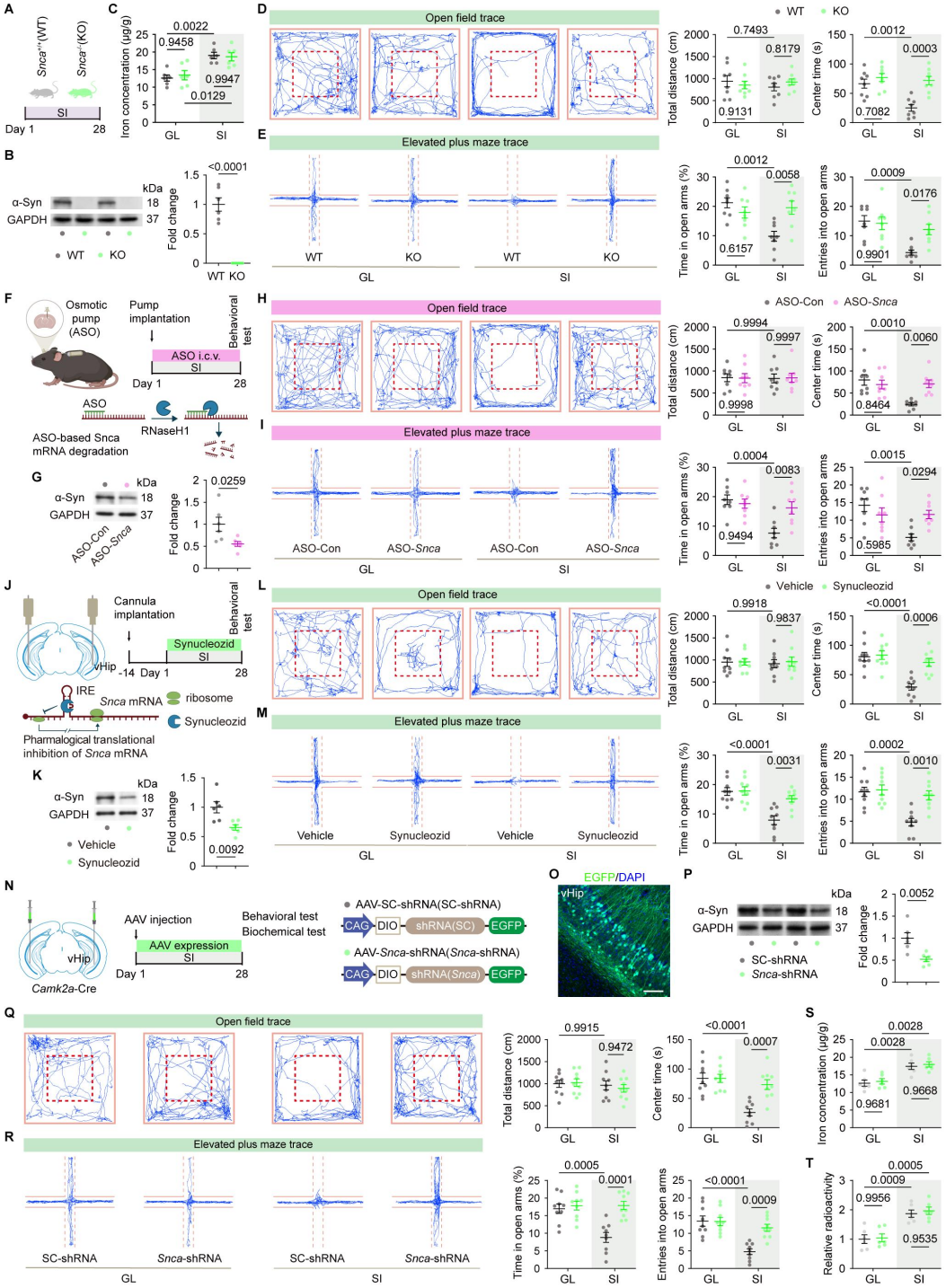
功能验证显示,Snca敲除小鼠、Snca靶向ASO干预,或vHip锥体神经元特异性Snca敲低,均能阻断SI诱导的焦虑。最后,双病毒双向策略实验进一步确立了线性因果关系:vHip锥体神经元Tfrc敲低的抗焦虑效应可被α-Syn过表达逆转,而Tfrc过表达诱导的焦虑能通过Snca敲低挽救,证实α-Syn是TfR1-铁轴下游不可或缺的效应分子。
图6. TfR1-α-Syn轴驱动SI诱导的焦虑和vHip铁可塑性
图7. 多层面靶向α-Syn可缓解SI诱导的焦虑
图8. 从关联到因果:靶向vHip TfR1-α-Syn轴及其下游神经元兴奋性可挽救焦虑表型
5、TfR1-α-Syn轴通过功能性和结构性突触重塑介导铁可塑性
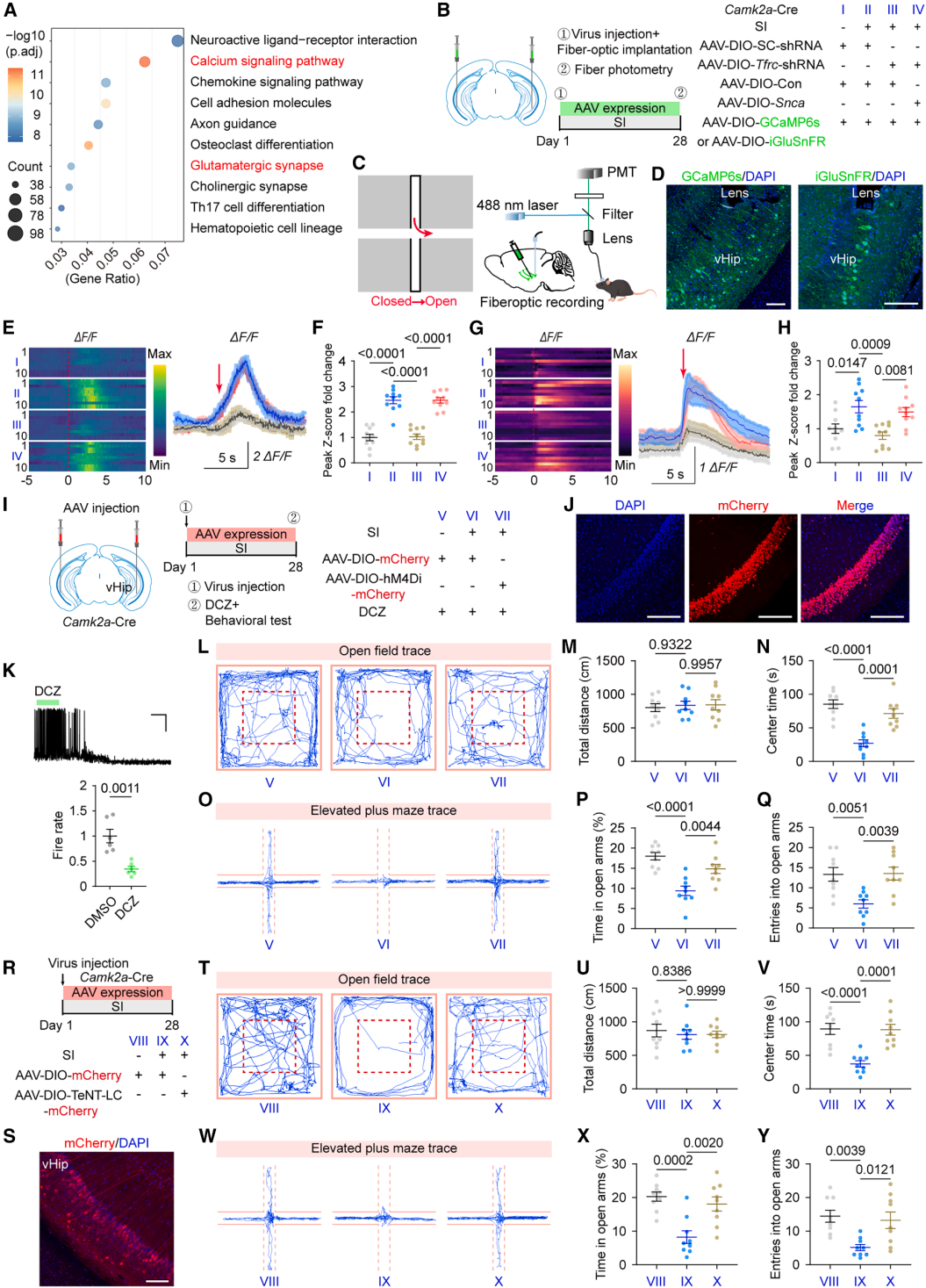
为阐明α-Syn对神经元功能的调控机制,研究者对vHip锥体神经元开展了电生理与结构分析。FosB(神经元激活标志物)免疫染色显示,SI显著增加vHip激活神经元的密度,该效应可被Tfrc敲低逆转,而被α-Syn过表达恢复。全细胞膜片钳记录表明,SI可增强vHip神经元内在兴奋性(放电频率升高、动作电位阈值降低),并提升微小兴奋性突触后电流(mEPSC)频率,提示突触传递增强;这些过度兴奋可通过TfR1干预恢复,α-Syn过表达则会使其重现。配对脉冲比率(PPR)分析进一步证实,α-Syn过表达能在TfR1敲低基础上再次增强谷氨酸释放,驱动突触前功能重塑。
分子层面,SI可升高SNARE复合物(介导突触囊泡融合)水平(不改变其单体总蛋白量),表明α-Syn通过促进该复合物组装增强突触传递。结构层面,SI可增加vHip锥体神经元树突棘密度,同样被Tfrc敲低逆转、α-Syn过表达恢复。综上,这些发现确立了“铁可塑性”——一种由TfR1-α-Syn轴调控的新型铁驱动突触重塑,是vHip突触结构/功能及神经元兴奋性的关键决定因素。(见图6-8)
6、TfR1-α-Syn轴通过诱导vHip过度兴奋与谷氨酸能过度胞吐驱动SI性焦虑
为确立神经元过度兴奋与焦虑行为之间的因果关系,研究者采用了多种功能性干预策略。首先,研究者实时监测了小鼠在高架十字迷宫开臂探索时vHip神经元的钙活动和谷氨酸释放。结果显示,SI小鼠在开臂探索期间表现出显著的钙瞬变增强和谷氨酸释放激增,这些效应被Tfrc敲低消除,并被α-Syn过表达恢复。接下来的化学遗传学抑制实验表明,无论是SI小鼠还是α-Syn过表达小鼠,vHip锥体神经元活动的抑制均显著改善了焦虑样行为(见图8)。表明TfR1-α-Syn轴激活驱动的焦虑样行为关键依赖于vHip神经元过度兴奋。
为直接验证增强的谷氨酸释放(而非一般的过度兴奋)是否为关键病理机制,研究者使用破伤风毒素轻链(TeNT-LC)特异性阻断vHip锥体细胞中突触囊泡胞吐作用。TeNT-LC可通过切割突触小泡蛋白2(VAMP2)选择性抑制突触前释放,而不影响神经元整体兴奋性。结果显示,该操控有效挽救了SI和α-Syn过表达诱导的焦虑表型(见图8)。以上结果确立了一个清晰的因果链条:TfR1-α-Syn轴的激活导致vHip神经元过度兴奋与谷氨酸能过度胞吐,从而驱动焦虑样行为。
图9. TfR1-α-Syn轴驱动的vHip谷氨酸能过度活跃是SI诱导焦虑的必需条件
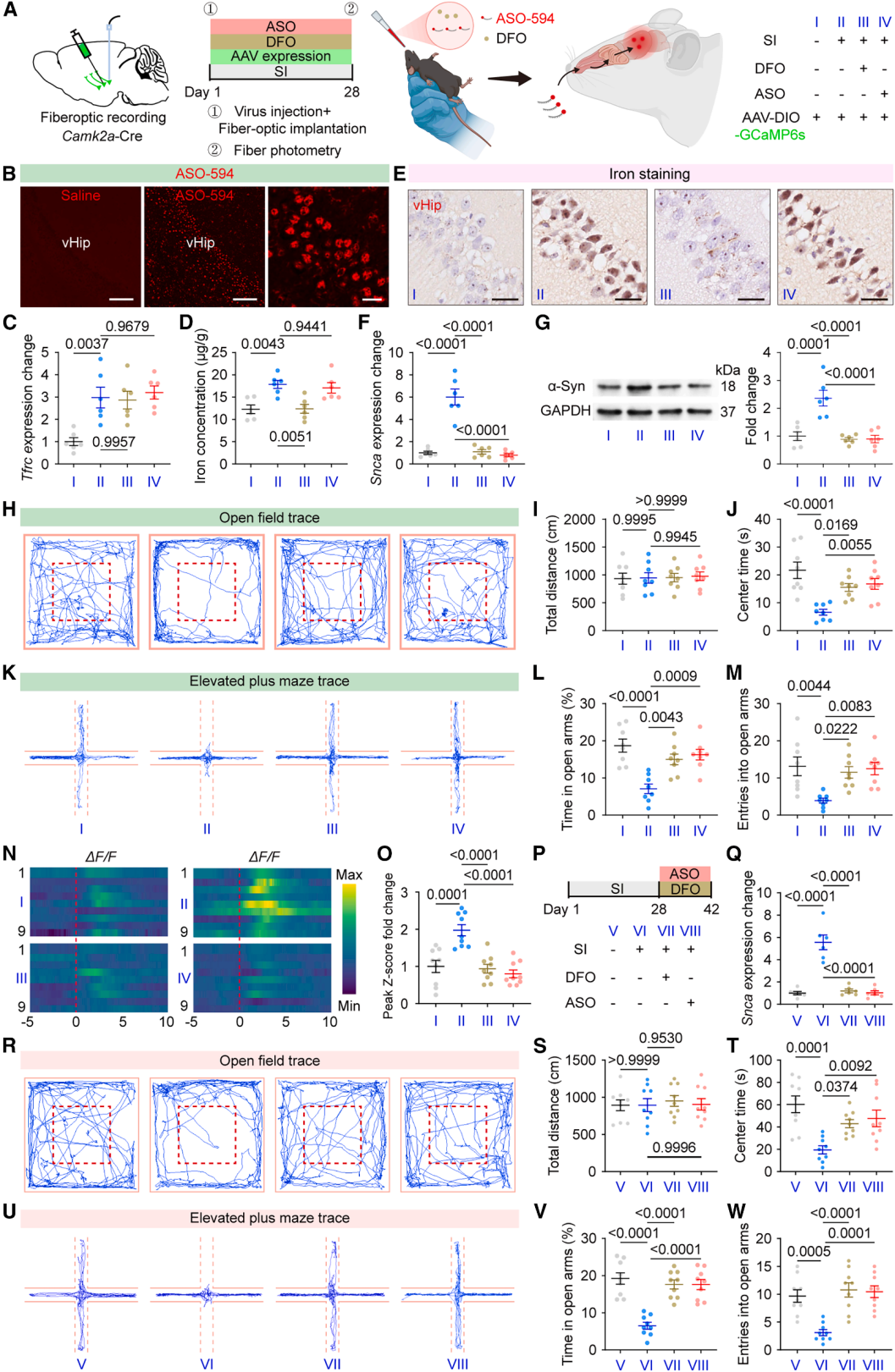
7、经鼻靶向铁-α-Syn轴的临床转化潜力与机制特异性
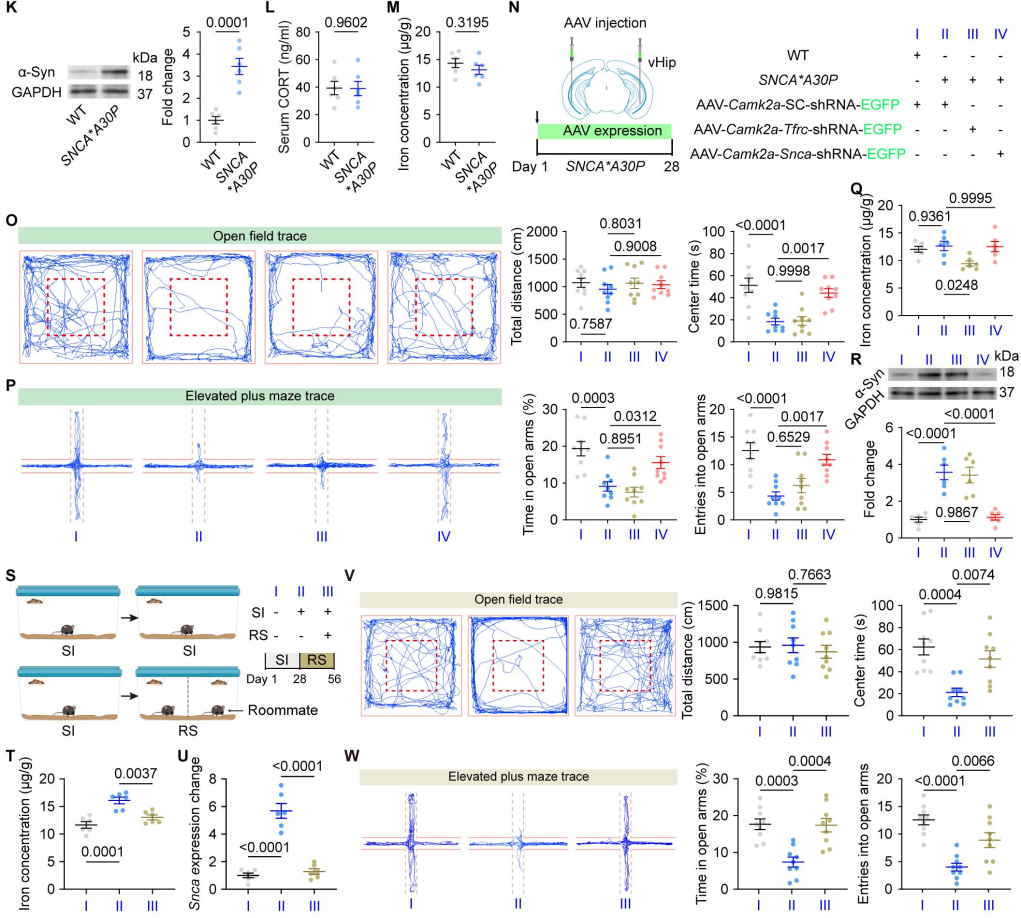
基于上述机制发现,研究者最后评估了靶向该通路的治疗潜力。采用非侵入性鼻给药方式,向隔离小鼠递送铁螯合剂DFO或靶向α-Syn的ASO。在预防性范式中,两种干预均在隔离期间给药,结果显示:DFO显著降低了vHip铁含量,DFO与ASO均下调了Snca的mRNA和蛋白水平;两者均有效预防了焦虑样行为的出现,并正常化了vHip的钙活动。在治疗性范式中,研究者待4周隔离完成、焦虑表型完全建立后,再进行2周鼻内给药。结果显示,DFO与ASO的延迟治疗同样有效逆转了Snca过表达和焦虑样行为,证实靶向铁-α-Syn轴即使在病理已确立的情况下仍具有疾病修饰效应。值得注意的是,将隔离小鼠重新放回社会环境中(重新社会化)4周,同样能使vHip铁水平和Snca表达恢复正常,并挽救了焦虑行为,证明应激诱导的“铁可塑性”级联反应具有经验依赖的可逆性。
为探究该机制的疾病特异性,研究者对SNCA*A30P转基因PD模型小鼠进行了检测。这些小鼠表现出焦虑样行为和vHip α-Syn过表达,但vHip铁水平和GC水平未升高。在A30P小鼠中,vHip Snca敲低可使α-Syn表达正常化并缓解焦虑,而Tfrc敲低则无此效应,表明该模型中的焦虑由α-Syn直接驱动,且独立于上游TfR1-铁通路。这些结果定义了明确的机制分离:SI诱导的焦虑依赖于完整的GR-TfR1-铁-α-Syn级联反应,而该遗传性PD模型中的焦虑则由α-Syn直接驱动,独立于上游铁失调,为不同病因焦虑的精准治疗提供了理论依据。
图10. 经鼻靶向铁-α-Syn轴可预防和逆转SI诱导的焦虑
图11. SI性焦虑的机制解离与可逆性
总结
该研究首次揭示了SI诱导焦虑的完整通路:SI通过升高GC,激活vHip锥体细胞GR信号,上调TfR1并诱导神经元铁沉积;铁过载通过解除Snca mRNA翻译抑制上调α-Syn,介导“铁可塑性”,最终导致vHip谷氨酸能神经元过度活跃,驱动SI性焦虑。该研究的核心突破在于提出“铁可塑性”概念,建立了脑铁代谢与情感障碍的直接关联,并开发了非侵入性经鼻给药策略。不仅填补了社会应激诱导焦虑的分子机制空白,还为焦虑障碍的治疗提供了新靶点与转化路径。
研究局限性包括:缺乏人类临床样本验证、未探索胶质细胞在铁循环中的作用、未关注性别差异对通路的影响等。未来方向需聚焦于临床转化(如开展人类海马体铁成像与生物标志物检测),拓展铁可塑性的调控网络,并优化经鼻给药系统以提升脑靶向效率。
总结图
浙江大学王福俤教授、闵军霞教授、华南理工大学王卓副教授、南方医科大学邱平明教授、吕田明教授为共同通讯作者。华南理工大学王卓副教授、研究生杨思凡、南方医科大学黄添容为共同第一作者。本研究获国家自然科学基金、广东省基础与应用基础研究基金等项目资助。
本文使用的病毒产品均来自枢密科技,列表如下:
扫码添加客服
更多产品及详情欢迎咨询!


市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK