2026-03-02 阅读量:213
胆汁淤积以胆汁酸(BAs)在肝脏及体循环中蓄积为特征,可导致肝损伤。其病因复杂多样,包括胆管梗阻所致的梗阻性胆汁淤积(OC)、原发性胆汁性胆管炎(PBC)、原发性硬化性胆管炎(PSC)等。肝脏中蓄积的BAs可启动炎症反应并促进肝细胞死亡,这一过程部分由趋化因子产生与炎性细胞浸润所介导。结合型BAs可在小鼠肝细胞中诱导CC趋化因子配体2(Ccl2)和CXC趋化因子配体2(Cxcl2)的表达,进而招募中性粒细胞并加重胆管结扎(BDL)胆汁淤积小鼠的肝细胞坏死;而Ccl2敲除则可显著减轻胆汁淤积性肝损伤。这些趋化因子还可招募单核细胞,在肝纤维化、代谢功能障碍相关脂肪性肝病(MASLD)等疾病中促进炎症反应。
单核细胞是骨髓来源的一类单个核细胞。人外周血单核细胞分为三个亚群:经典型CD14⁺CD16⁻单核细胞、中间型CD14⁺CD16⁺单核细胞以及非经典型CD14ˡᵒʷCD16⁺单核细胞。小鼠单核细胞亚群则根据Ly6C与CD43表达分为:经典型Ly6C⁺CD43ˡᵒʷ单核细胞、中间型Ly6C⁺CD43⁺单核细胞及非经典型Ly6CˡᵒʷCD43⁺单核细胞。中间型单核细胞具有独特的表面分子特征与特定生物学功能,可通过高水平分泌促炎细胞因子(包括肿瘤坏死因子-α(TNF-α)、白细胞介素-1β(IL-1β)和白细胞介素-6(IL-6))参与炎症性肠病、视神经脊髓炎谱系疾病等炎症性疾病的发病过程。然而,在胆汁淤积中,CD14⁺CD16⁺单核细胞的作用以及BAs是否通过诱导肝脏趋化因子的表达来招募该细胞亚群,目前仍不明确。
肝细胞死亡(包括细胞焦亡、细胞凋亡等)是驱动胆汁淤积性肝损伤发生发展的重要过程。有趣的是,程序性坏死近年来被证实为肝细胞死亡的一种新机制。从机制上看,多种细胞应激均可启动程序性坏死信号,包括TNF-α、Fas相关凋亡配体(FASL)或TNF相关凋亡诱导配体(TRAIL)等死亡受体配体激活的信号通路。一旦被激活,受体相互作用丝氨酸/苏氨酸蛋白激酶3(RIPK3)与RIPK1结合形成坏死小体复合物,最终激活混合谱系激酶结构域样蛋白(MLKL),并在细胞膜上形成孔道,进而导致细胞死亡。近期研究证实,程序性坏死通常由TNF-α与FASL启动。既往研究发现,OC患者存在肝细胞程序性坏死且肝脏TNF-α水平升高。然而,胆汁淤积如何诱导肝细胞发生程序性坏死仍不清楚。
近期,陆军军医大学第一附属医院(西南医院)消化内科柴进教授团队在JHEP|Reports期刊(IF=7.5)发表了题为“Conjugated bile acid-driven CD14⁺CD16⁺monocyte infiltration promotes cholestatic liver injury by enhancing hepatocyte necroptosis”的研究论文。本研究通过单细胞RNA测序(scRNA-seq)与多重免疫荧光(mIF)技术,观察到OC与PBC患者胆汁淤积肝脏中CD14⁺CD16⁺单核细胞浸润增加。且CD14⁺CD16⁺单核细胞数量与肝损伤严重程度呈正相关,具体表现为与丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)水平正相关。输注人CD14⁺CD16⁺单核细胞(即人中间型单核细胞)可加重1%石胆酸(LCA)饲喂小鼠的胆汁淤积性肝损伤;同样地,输注小鼠中间型单核细胞亦可加重小鼠胆汁淤积性肝损伤。机制研究表明,CD14⁺CD16⁺单核细胞浸润可使肝脏中TNF-α和FASL水平升高,激活RIPK1-RIPK3-MLKL信号轴,从而促进肝细胞程序性坏死。此外,BAs应激的肝细胞可通过c-Jun氨基末端激酶(JNK)/c-Jun信号通路介导CCL2和CCL3表达上调,从而趋化CD14⁺CD16⁺单核细胞向肝脏浸润。综上所述,本研究首次证实浸润的CD14⁺CD16⁺单核细胞可促进肝细胞程序性坏死,加重胆汁淤积性肝损伤。因此,靶向调控该类单核细胞的趋化作用,有望成为胆汁淤积性肝损伤的潜在治疗策略。

1.OC患者与健康对照肝脏非实质细胞(NPCs)的单细胞转录组分析
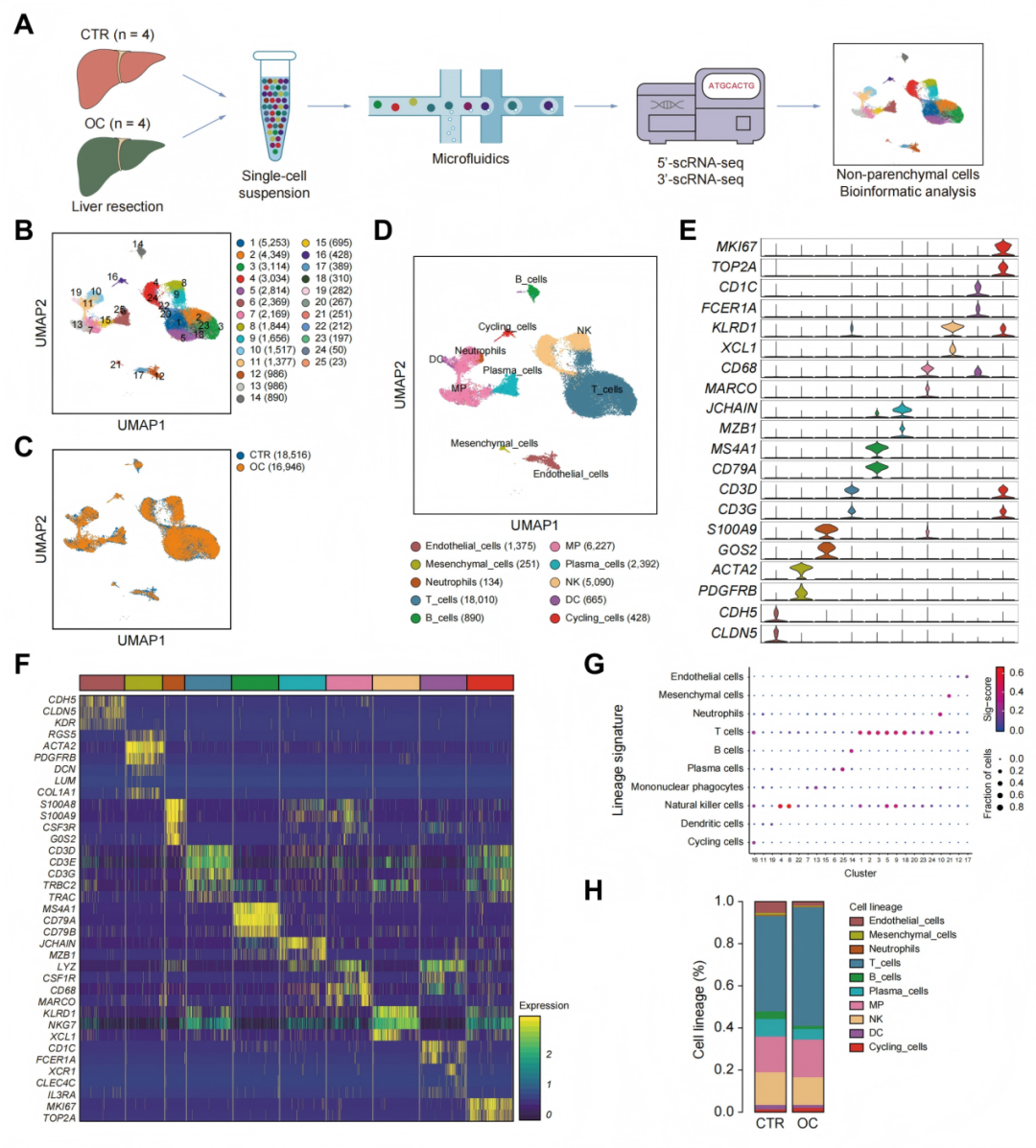
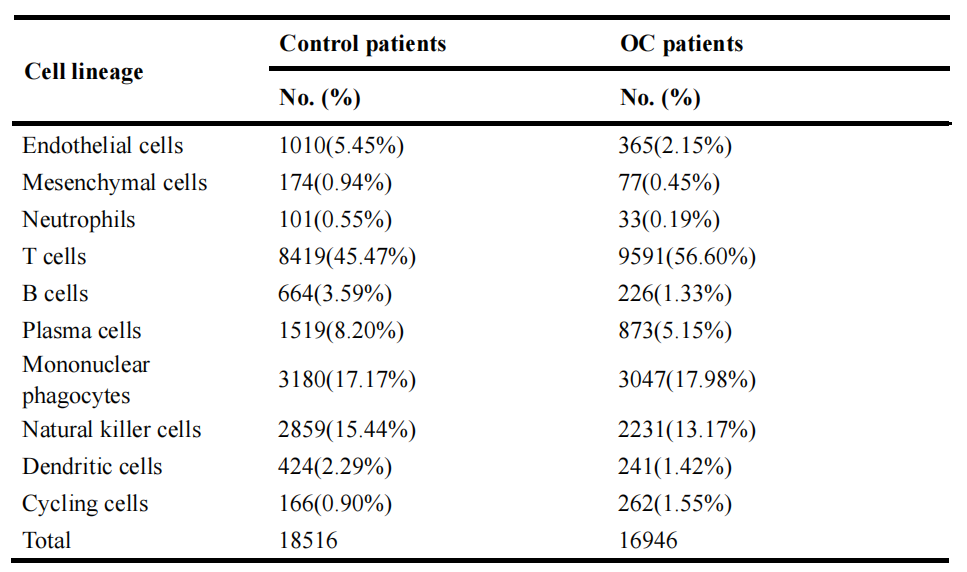
研究人员对OC患者及对照人群肝组织进行了5′/3′-scRNA-seq分析(每组n=4)。5′-scRNA-seq在对照组与OC患者肝脏中分别鉴定出18516个和16946个肝脏NPCs。均匀流形逼近与投影(UMAP)分析显示,这些样本共分为25个NPCs亚群,涵盖10种细胞谱系,各细胞谱系均具有特征性基因标志物。值得关注的是,这些细胞谱系的构成在对照组与OC肝脏之间存在显著差异。3′-scRNA-seq数据证实了相似的细胞组成变化。研究者还分析了两组中各肝脏细胞亚群的差异表达基因(DEG)。
图1.对OC患者与对照人群的肝脏NPCs进行单细胞转录组分析
表1.经5′-scRNA-seq鉴定的肝脏中不同类型NPCs的分布
2.胆汁淤积患者肝脏CD14⁺CD16⁺单核细胞数量与肝损伤严重程度呈正相关
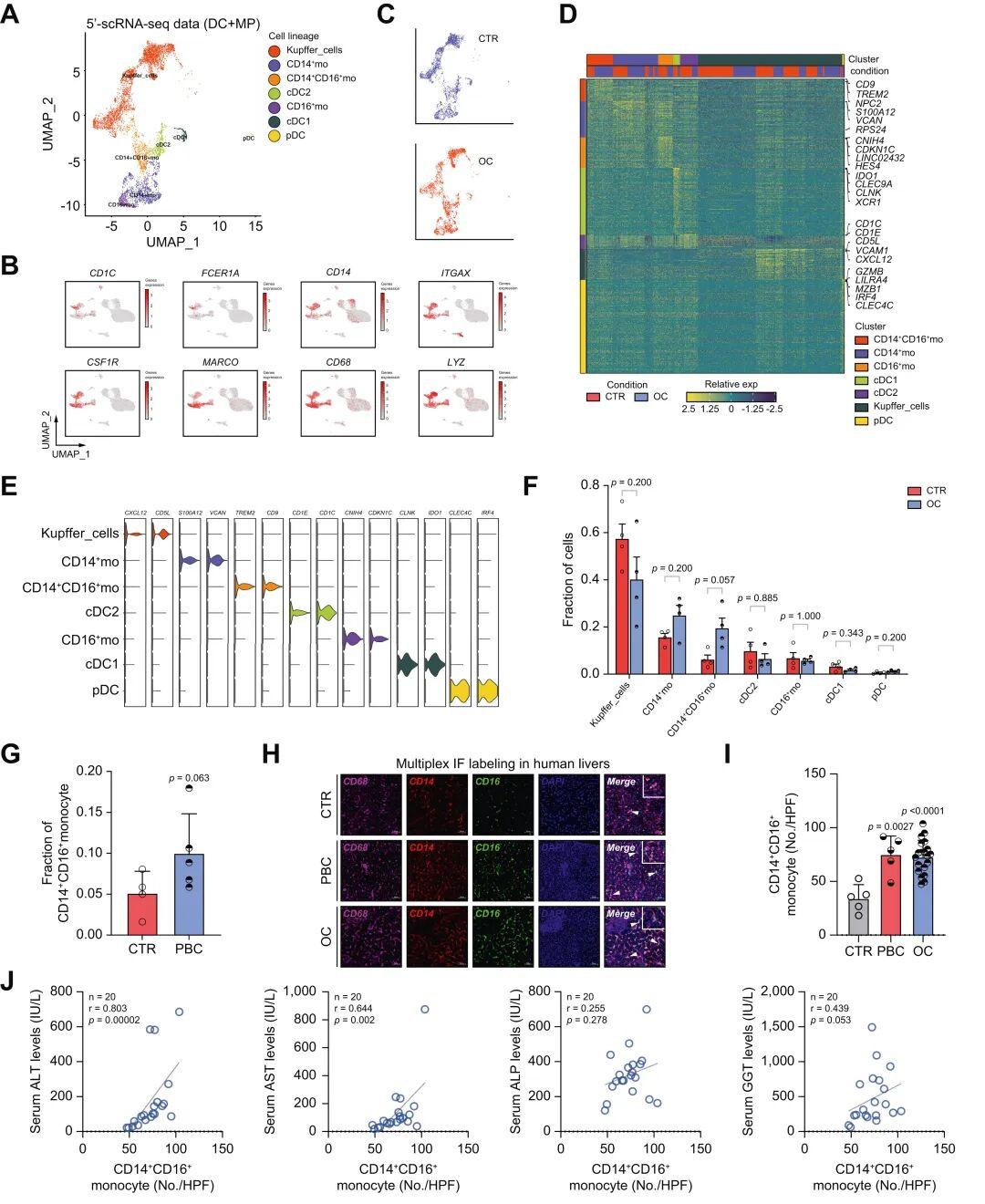
为进一步探究NPCs在胆汁淤积中的潜在病理生理作用,作者进行了深入的亚群分析。尽管T细胞和B细胞在主要细胞谱系水平上呈现一定变化,但其亚群构成未观察到显著改变。值得注意的是,单核吞噬细胞系统的各亚群比例发生了显著重构。scRNA-seq数据分析显示,依据独特的分化状态与功能,单核吞噬细胞系统可分为7个细胞簇。这些细胞簇呈现出独特的基因表达谱与生物标志物。在这7个细胞簇中,单核细胞分为3个亚群:CD14⁺单核细胞(人经典型单核细胞)、CD16⁺单核细胞(人非经典型单核细胞)以及CD14⁺CD16⁺单核细胞(人中间型单核细胞)。与对照人群相比,OC患者肝脏中CD14⁺CD16⁺单核细胞比例显著升高。同样,PBC患者肝脏中也观察到CD14⁺CD16⁺单核细胞比例升高。
为验证CD14⁺CD16⁺单核细胞的特异性,研究人员通过基因本体(GO)分析了DEG及相关通路。结果显示,CD14⁺CD16⁺单核细胞具有区别于其他单核细胞亚群的独特DEG谱,提示单核吞噬细胞系统内部存在机制各异的转录调控模式。
为验证上述结果,对人肝组织进行了多重免疫荧光(mIF)染色。结果显示,与对照组相比,OC或PBC患者肝脏中浸润的CD14⁺CD16⁺单核细胞数量显著增多。有趣的是,肝脏CD14⁺CD16⁺单核细胞数量与血清丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)水平呈显著正相关,提示CD14⁺CD16⁺单核细胞可加重胆汁淤积状态下的肝损伤。
图2.胆汁淤积患者肝脏中CD14⁺CD16⁺单核细胞浸润数量增多,且与肝损伤程度呈正相关
表2.经5′-scRNA-seq鉴定的单核吞噬细胞亚群的分布

3.在石胆酸(LCA)饮食诱导的胆汁淤积小鼠模型中,CD14⁺CD16⁺单核细胞浸润显著加重胆汁淤积性肝损伤
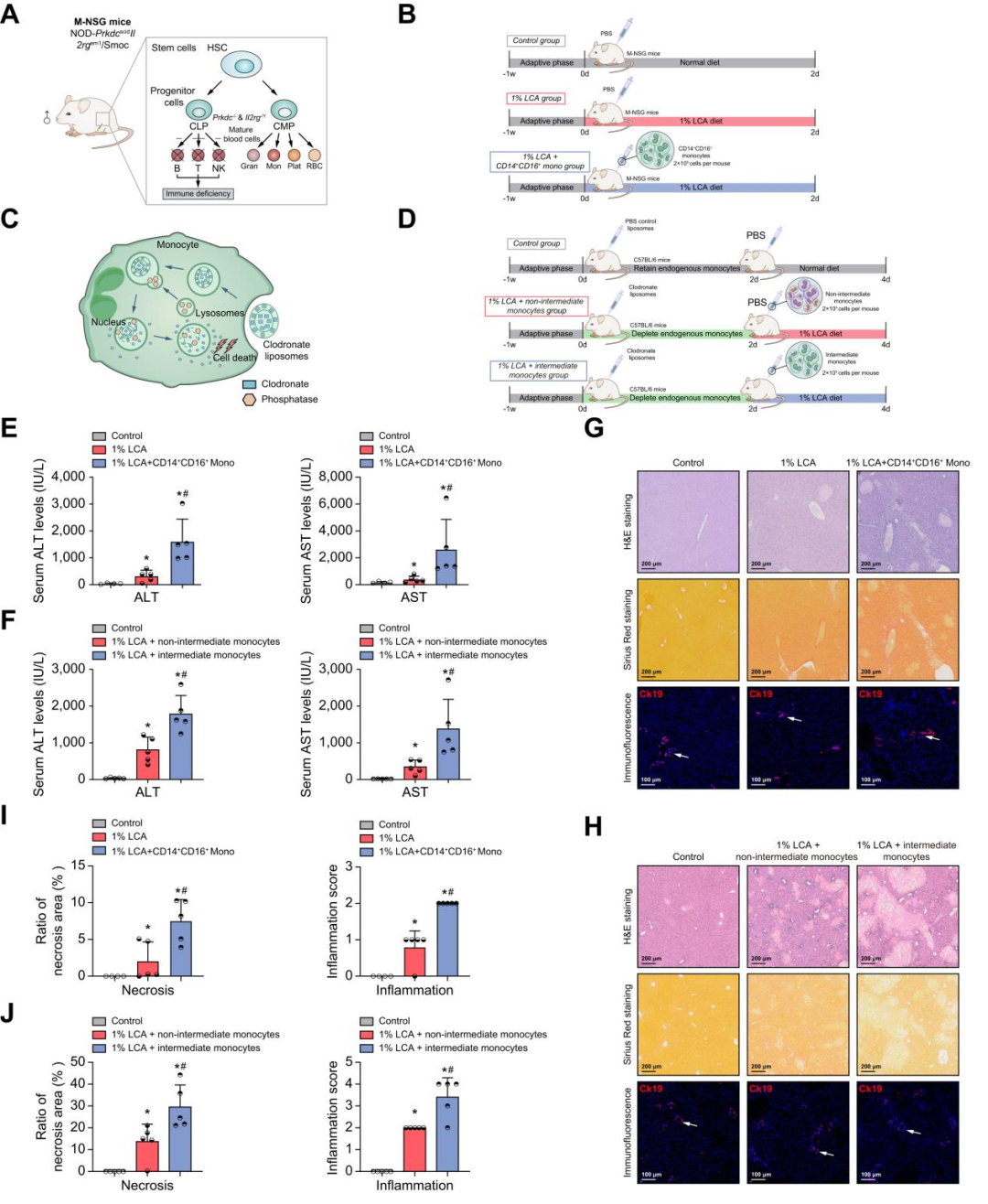
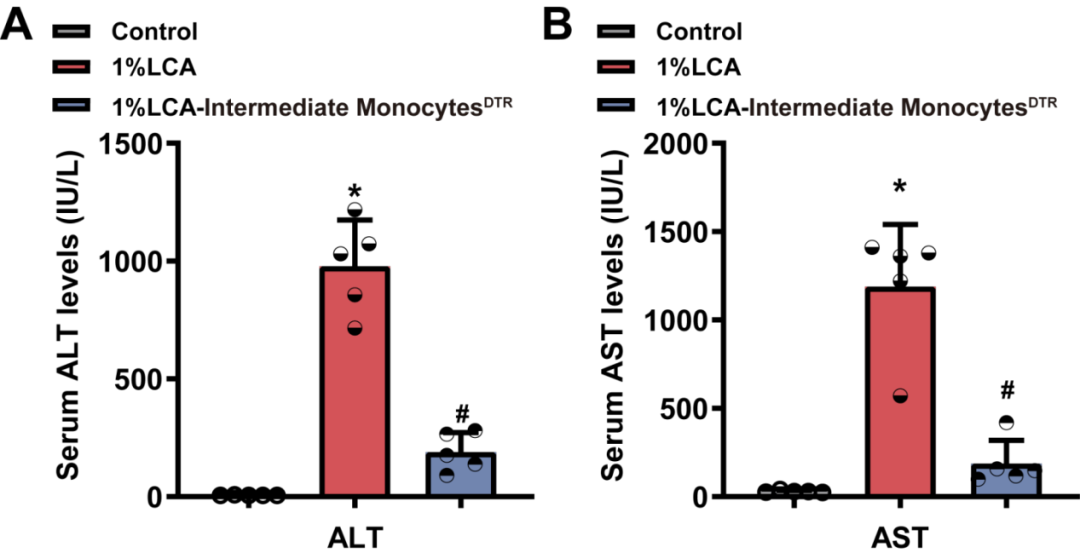
为进一步探究浸润的中间型单核细胞在胆汁淤积中的功能作用,本研究构建了两种动物模型。在第一种模型中,纯化人外周血CD14⁺CD16⁺单核细胞并将其注射入免疫缺陷型NOD-PrkdcscidIl2rgeml/Smoc(商品名M-NSG)小鼠(完全缺失成熟T、B、NK细胞,几乎无适应性免疫与NK杀伤功能),随后给予1% LCA饮食以诱导胆汁淤积。在第二种模型中,使用氯膦酸盐脂质体清除C57BL/6小鼠内源性单核吞噬细胞。注射氯膦酸盐脂质体两天后,从小鼠骨髓中分离原代小鼠中间型单核细胞及非中间型单核细胞,随后分别向两组小鼠回输中间型单核细胞或非中间型单核细胞。与未回输细胞的小鼠相比,人CD14⁺CD16⁺单核细胞回输可显著升高胆汁淤积M-NSG小鼠的血清ALT与AST水平。同样,与回输非中间型单核细胞组相比,回输中间型单核细胞的小鼠血清ALT和AST水平更高。
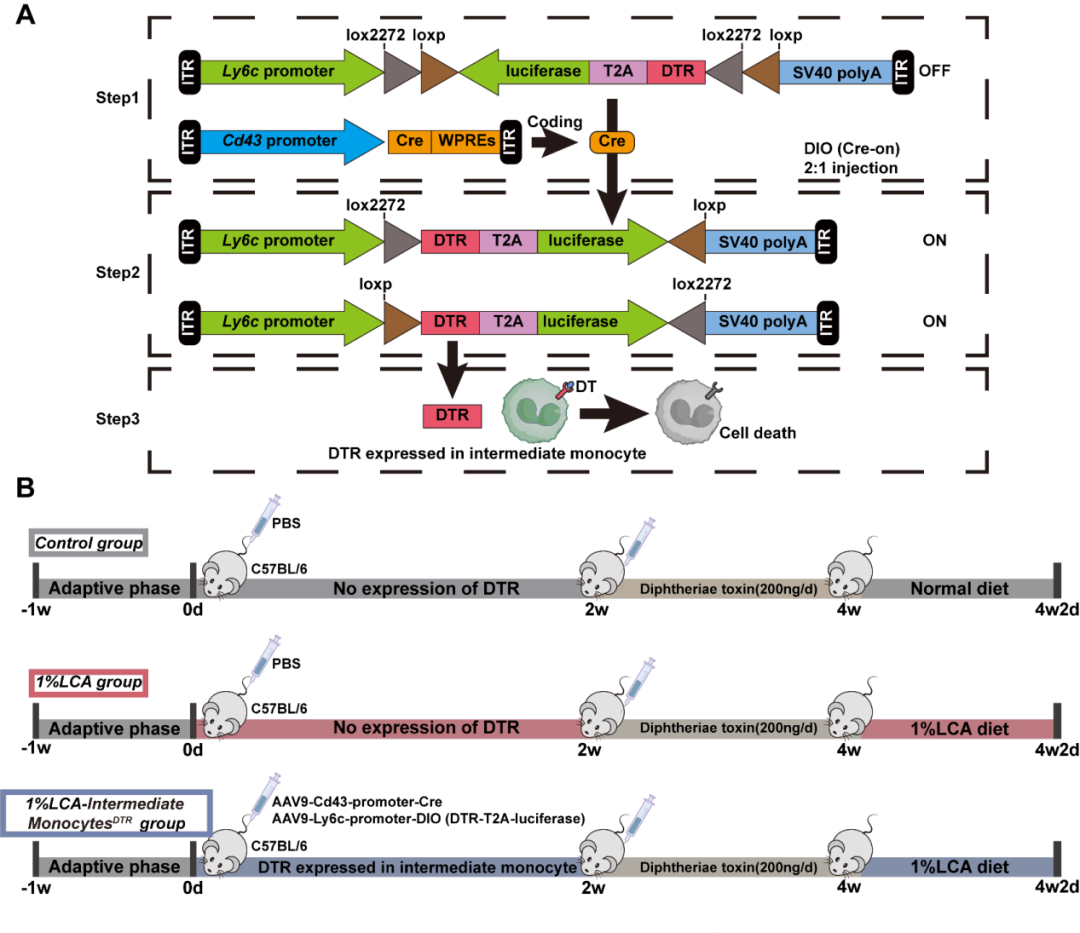
研究人员还构建了中间型单核细胞特异性白喉毒素受体(DTR)敲除系统,通过向C57BL/6小鼠尾静脉注射AAV9-Cd43-promoter-Cre与AAV9-Ly6c-promoter-DIO(DTR-T2A-luciferase)实现。结果发现,腹腔注射DT清除中间型单核细胞可减轻LCA诱导的肝损伤。此外,组织学结果证实,回输人源或小鼠源中间型单核细胞的胆汁淤积小鼠,经HE染色检测显示,其肝脏坏死面积比例与炎症评分均显著升高。但天狼星红(Sirius Red)染色评估的肝纤维化评分、角蛋白17(CK17)IF染色观察的胆管增殖均无显著性差异。综上所述,这些结果为中间型单核细胞浸润可显著加重胆汁淤积性肝损伤提供了可靠证据。
图3.输注人源或小鼠源中间型单核细胞可加重1% LCA诱导的胆汁淤积性小鼠模型的肝损伤
图4.清除中间型单核细胞的实验方案
图5.清除中间型单核细胞可显著缓解LCA诱导的小鼠胆汁淤积性肝损伤
4.在LCA诱导的胆汁淤积小鼠及胆汁淤积患者中,肝细胞程序性坏死显著增加,并与CD14⁺CD16⁺单核细胞数量呈正相关
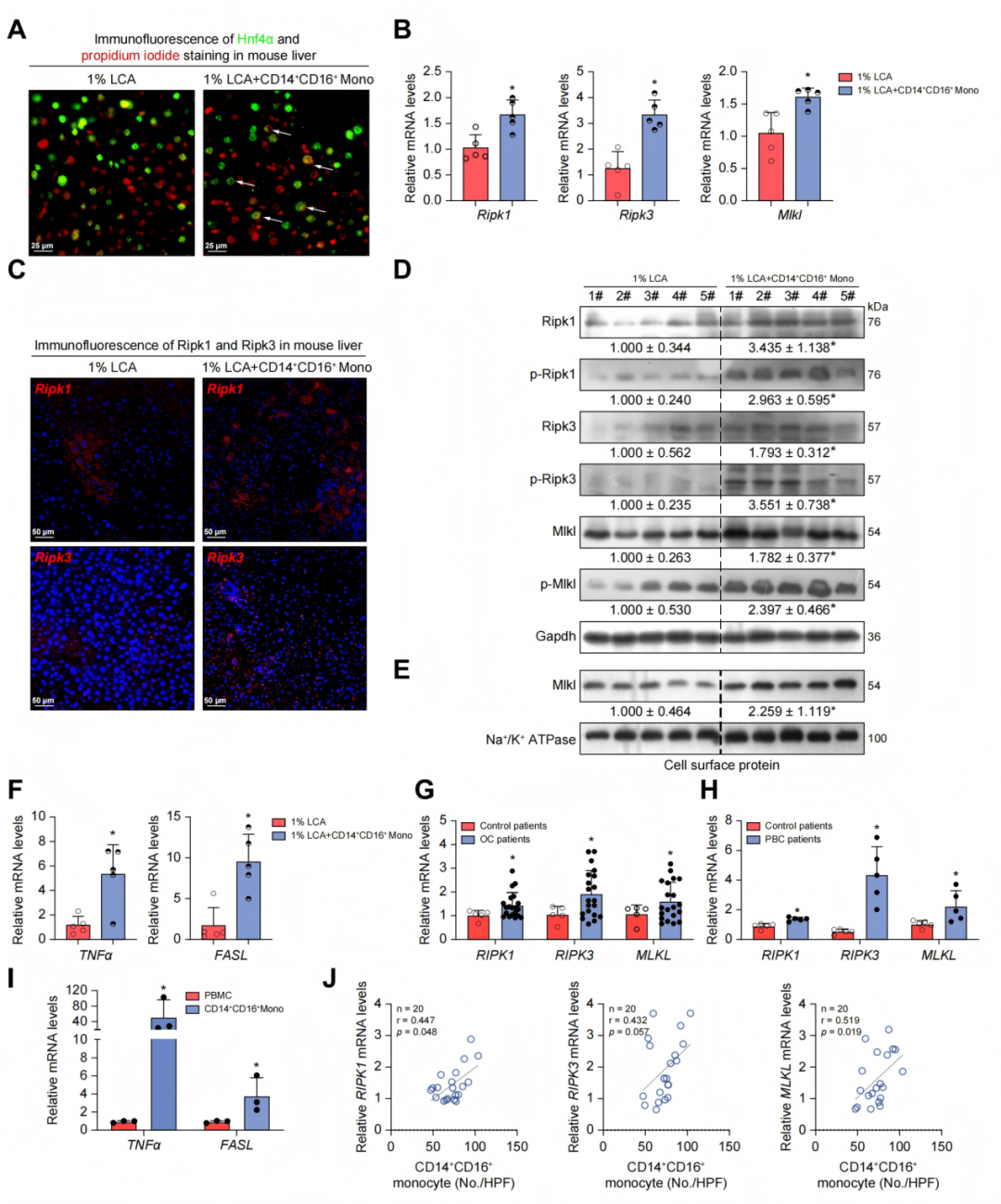
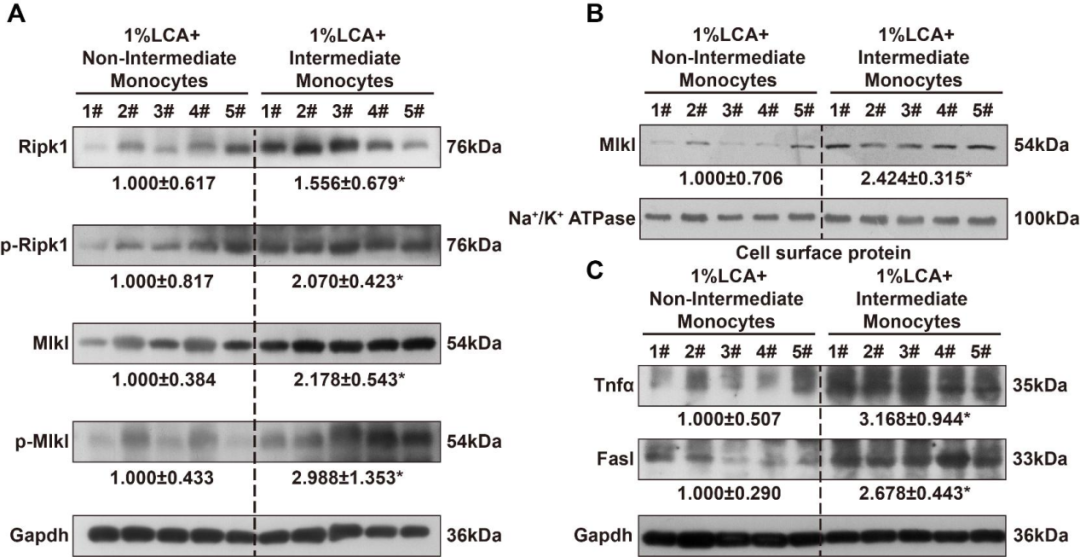
血清ALT和AST显著升高提示肝细胞大量死亡。通过肝细胞特异性核标志物肝细胞核因子4α(HNF4α)IF染色与碘化丙啶(PI)核复染进行双重标记检测,研究人员观察到:给予LCA喂养但未输注中间型单核细胞的M-NSG小鼠,其HNF4α阳性细胞核形态大多保持完整(呈圆形或椭圆形,荧光强度均匀),反映胆汁淤积应激下的基础细胞死亡水平。相比之下,输注CD14⁺CD16⁺单核细胞并给予LCA喂养的小鼠,其HNF4α阳性细胞核形态出现明显异常,表现为染色质浓缩、核碎裂及核轮廓不规则。于是,为探究CD14⁺CD16⁺单核细胞如何加重肝细胞特异性死亡,研究人员检测了不同类型的细胞死亡:以半胱天冬氨酸蛋白酶3(Caspase-3)和Bax指示细胞凋亡,焦孔素D(GSDMD)指示细胞焦亡,RIPK1、RIPK3和MLKL指示程序性坏死。结果显示,在输注或不输注人CD14⁺CD16⁺单核细胞的胆汁淤积小鼠中,凋亡相关分子(Caspase-3、Bax)及焦亡相关分子(Gsdmd)的表达水平均无显著变化。与之相反,在LCA诱导的胆汁淤积M-NSG小鼠中,输注人CD14⁺CD16⁺单核细胞可显著升高肝脏Ripk1、Ripk3和Mlkl(程序性坏死)的mRNA相对水平。IF结果证实,在输注人CD14⁺CD16⁺单核细胞的小鼠肝脏中,RIPK1和RIPK3蛋白表达上调。此外,蛋白质免疫印迹结果显示,在LCA诱导的胆汁淤积M-NSG小鼠中,输注人CD14⁺CD16⁺单核细胞可显著升高肝脏中RIPK1、RIPK3和MLKL的磷酸化水平及总蛋白水平,且程序性坏死的负向调控因子Caspase-8表达降低。此外,这些小鼠中MLKL膜转位增加,证实程序性坏死通路被激活。在接受小鼠中间型单核细胞或非中间型单核细胞移植的模型中,蛋白质免疫印迹结果同样证实程序性坏死信号轴被激活。同样,在OC或PBC患者中,程序性坏死标志物RIPK1、RIPK3、MLKL的mRNA水平亦显著升高,提示人胆汁淤积状态下肝脏程序性坏死被激活。此外,输注小鼠中间型单核细胞还可促进LCA诱导胆汁淤积小鼠的T细胞浸润。通过T细胞标志物(CD3、CD4及CD8)IF染色,观察到输注中间型单核细胞的模型中T细胞数量增加。
鉴于TNF-α和FASL是细胞程序性坏死的重要诱导因子,研究者也检测了其肝脏水平。实时荧光定量PCR(RT-qPCR)结果显示,与对照组小鼠相比,输注人CD14⁺CD16⁺单核细胞的LCA诱导M-NSG小鼠中Tnf和Fasl的mRNA转录水平显著升高。在注射小鼠中间型单核细胞的LCA诱导胆汁淤积小鼠模型中也观察到相似结果。
为明确肝细胞程序性坏死是否由BAs直接细胞毒性引起,使用结合型BAs,包括牛磺胆酸(TCA)、牛磺鹅脱氧胆酸(TCDCA)和牛磺脱氧胆酸(TDCA),处理原代肝细胞。然而,BAs处理并未显著改变Ripk1、Ripk3或Mlkl的蛋白水平。
有趣的是,RT-qPCR分析显示,与其余外周血单个核细胞(PBMC)相比,人CD14⁺CD16⁺单核细胞中程序性坏死诱导因子(TNF和FASL)的mRNA表达水平更高。此外,在人胆汁淤积肝脏中,CD14⁺CD16⁺单核细胞数量与RIPK1或MLKL的mRNA转录水平呈正相关。综上所述,这些结果表明:CD14⁺CD16⁺单核细胞在肝脏内聚集,可通过促进TNF-α和FASL分泌,进而诱导胆汁淤积肝脏发生肝细胞程序性坏死。
图6.输注人源CD14⁺CD16⁺单核细胞可加重LCA诱导的小鼠肝脏程序性坏死
图7.输注小鼠中间型单核细胞可加重LCA诱导的小鼠肝脏程序性坏死
5.结合型BAs可诱导趋化因子CCL2和CCL3生成,进而在胆汁淤积过程中招募CD14⁺CD16⁺单核细胞向肝脏浸润
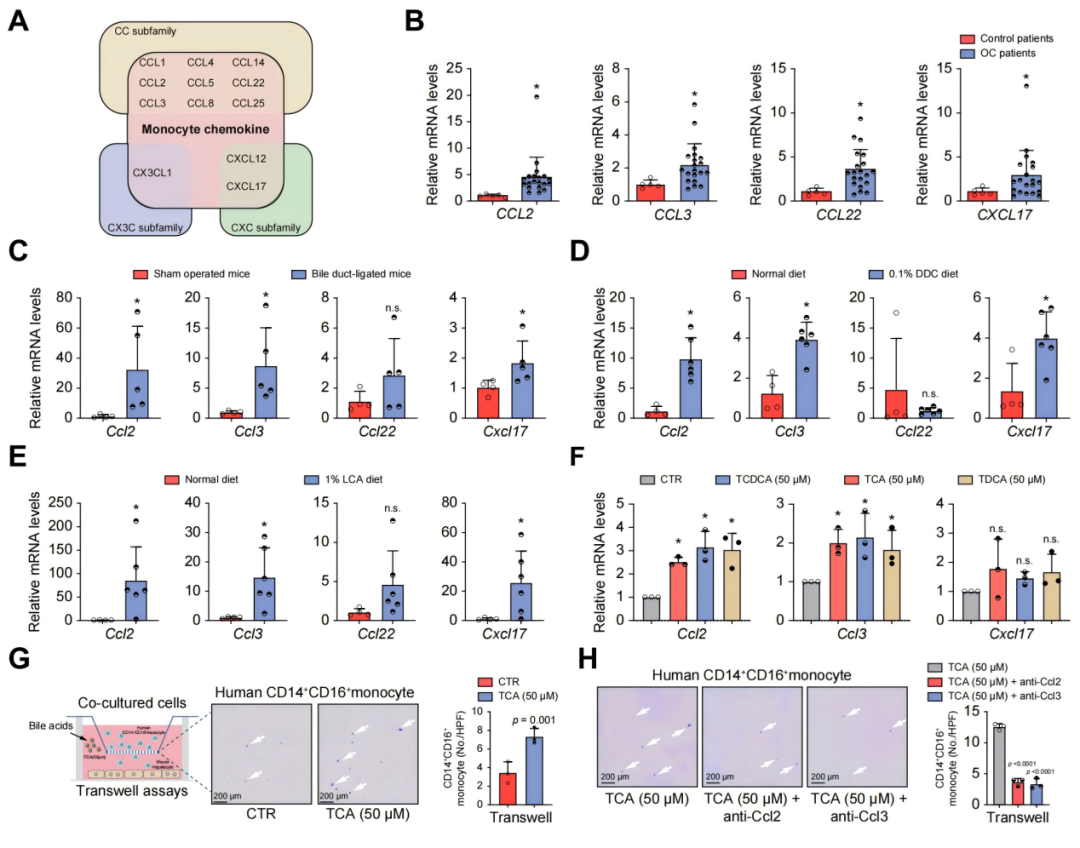
趋化因子通过其受体调控炎性细胞迁移。目前已知有49种趋化因子参与调控这一生物学过程,其中12种可介导单核细胞趋化作用。为鉴定胆汁淤积中调控CD14⁺CD16⁺单核细胞迁移的关键趋化因子,研究人员检测了上述12种趋化因子在OC患者肝脏中的表达水平。RT-qPCR结果显示,与对照组相比,OC患者肝脏中CCL2、CCL3、CCL22和CXCL17的mRNA转录水平显著升高;CCL4、CCL5、CCL8及CCL25的mRNA转录水平无明显变化;而CCL1、CCL14、CXCL12及CX3C趋化因子配体1(CX3CL1)的mRNA转录水平显著降低。同样,在多种胆汁淤积小鼠模型(包括BDL模型、0.1% 3,5-二乙氧羰基-1,4-二氢可力丁(DDC)饮食诱导模型及1% LCA诱导模型)的肝脏中,Ccl2、Ccl3和Cxcl17的mRNA转录水平亦显著升高,而Ccl22的mRNA转录水平未见明显变化。此外,RT-qPCR分析显示,结合型BAs(TCA、TCDCA和TDCA)处理小鼠原代肝细胞,可显著上调Ccl2和Ccl3的表达,但对Cxcl17表达无显著影响。
随后,采用Transwell共培养体系,验证结合型BAs是否通过诱导肝细胞表达CCL2和CCL3来招募CD14⁺CD16⁺单核细胞。结果显示,TCA处理可显著增加穿过Transwell膜、向小鼠原代肝细胞迁移的CD14⁺CD16⁺单核细胞数量。然而,在加入CCL2或CCL3中和抗体后,这种趋化增强效应可被显著阻断。综上所述,上述结果表明:结合型BAs可诱导肝细胞表达CCL2和CCL3,进而招募CD14⁺CD16⁺单核细胞向肝脏浸润。
图8.BAs可诱导肝细胞表达CCL2和CCL3,进而招募CD14⁺CD16⁺单核细胞向肝脏迁移并在肝脏内聚集
6.结合型BAs通过JNK/MAPK信号通路增强c-Jun与CCL2和CCL3启动子的结合活性,进而在胆汁淤积中诱导其表达
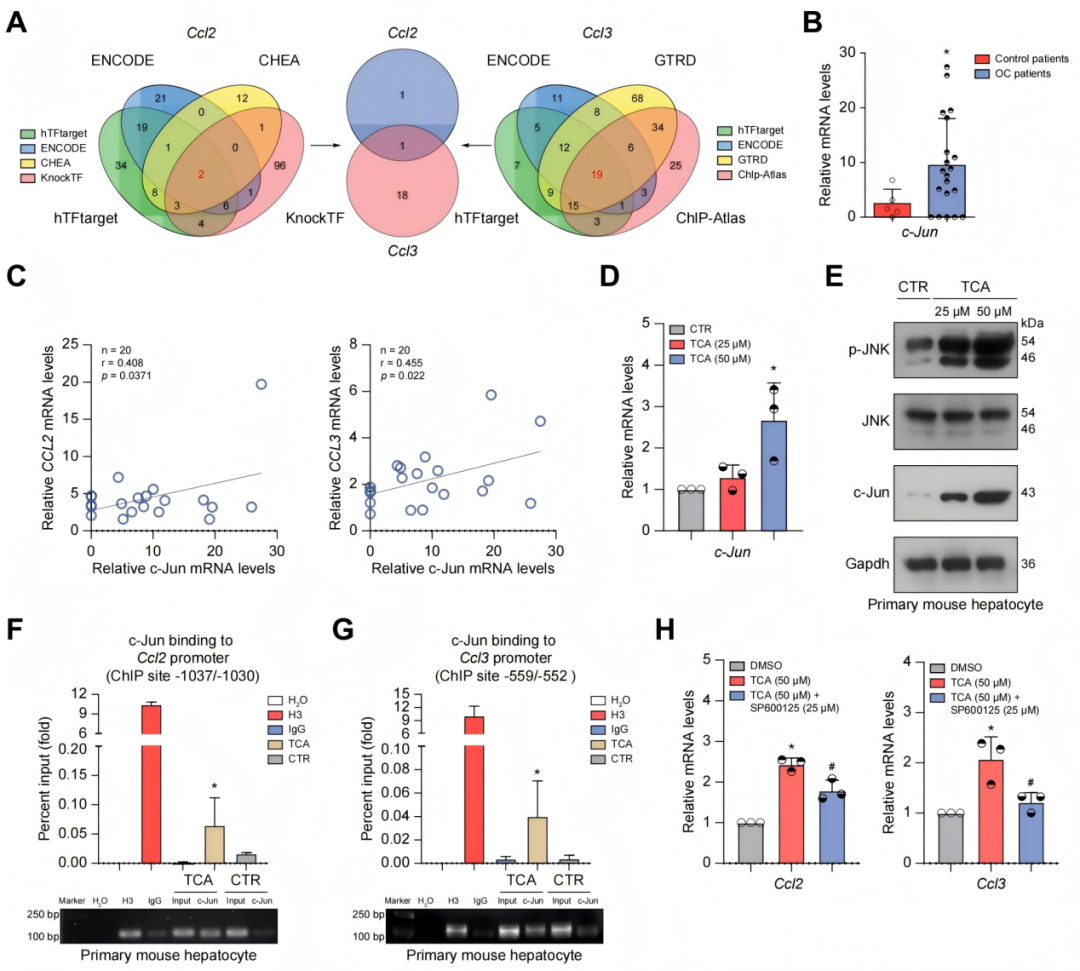
为阐明胆汁淤积状态下结合型BAs诱导CCL2和CCL3表达的分子机制,本研究通过生物信息学分析(hTFtarget、ENCODE、CHEA、KnockTF、GTRD及ChIP-Atlas数据库)预测了CCL2和CCL3启动子区域潜在的转录因子结合位点。RT-qPCR结果显示,OC患者肝脏中JUN mRNA水平升高,并与CCL2和CCL3表达呈正相关,提示c-Jun可上调上述趋化因子的表达。有趣的是,在小鼠原代肝细胞中,TCA可呈剂量依赖性上调Jun的mRNA与蛋白表达水平,并提高c-Jun氨基末端激酶(JNK)的磷酸化水平。此外,染色质免疫共沉淀(ChIP)实验证实,TCA能显著增强c-Jun与Ccl2或Ccl3启动子的结合能力;而在JNK特异性抑制剂SP600125处理后,上述增强效应明显减弱。综上,上述结果表明:在胆汁淤积过程中,结合型BAs通过上调肝细胞中c-Jun的表达与活性,进而诱导CCL2和CCL3的表达。
图9.在胆汁淤积的病理过程中,c-Jun调控肝细胞内CCL2和CCL3的表达
总结
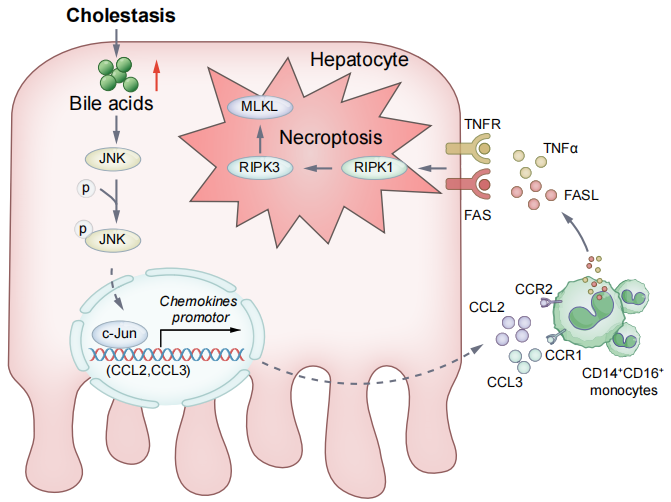
本研究证实,结合型BAs通过增强c-Jun与CCL2和CCL3启动子的结合活性,诱导肝细胞表达CCL2和CCL3,进而促进CD14⁺CD16⁺单核细胞向肝脏浸润,并通过加剧肝细胞程序性坏死加重胆汁淤积性肝损伤。因此,阻断CD14⁺CD16⁺单核细胞的肝脏浸润,有望成为治疗胆汁淤积性肝损伤的有效策略。
机制模式图
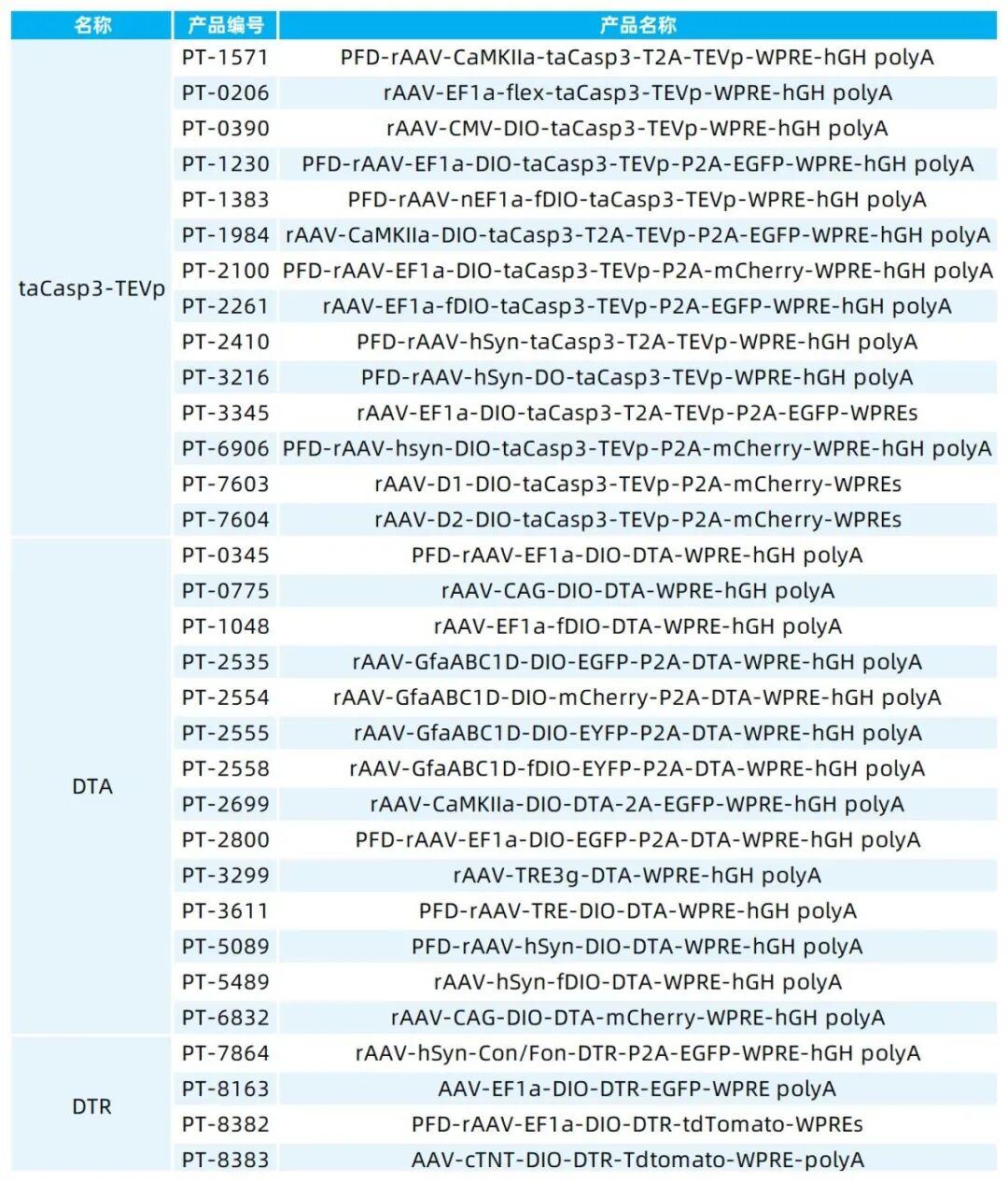
本文使用的病毒产品均来自枢密科技,列表如下:

我司提供多种诱导凋亡病毒,部分产品列表如下:
扫码添加客服
更多产品及详情欢迎咨询!


市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK