2026-02-25 阅读量:253
摄食作为维持生命活动的核心本能行为,受到昼夜节律的严格调控。摄食昼夜节律紊乱往往导致非适宜时段摄食和能量代谢失衡,进而增加代谢性疾病的患病风险。因此,作为生物体能量代谢调控的重要环节,摄食昼夜节律的神经机制研究对于理解代谢性疾病的发生机制具有重要意义。然而,目前我们对摄食昼夜节律调控的细胞和神经环路机制仍知之甚少。以往的研究主要关注传统摄食中枢(如下丘脑)在摄食昼夜节律调控中的作用,而对其他脑区的参与机制认识有限。
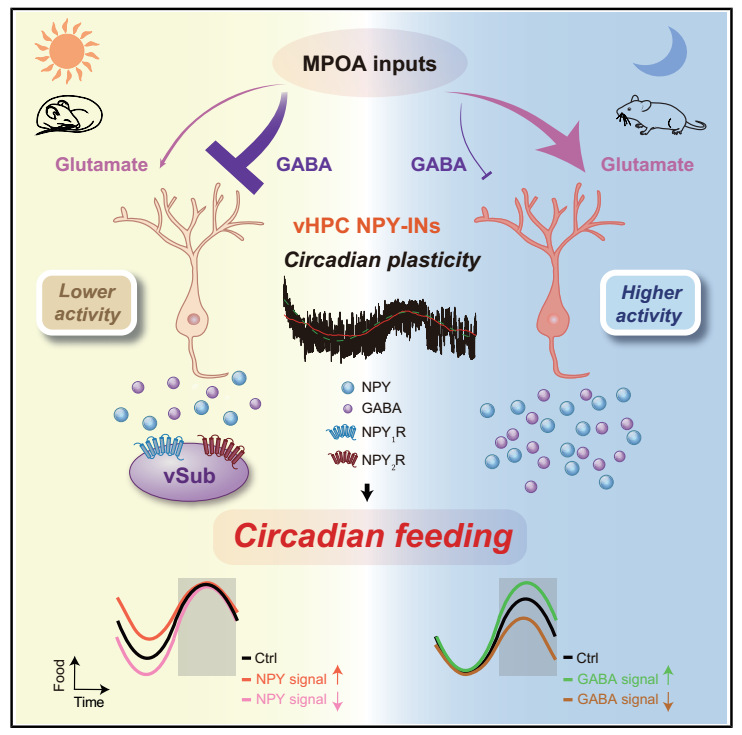
2026年2月19日,上海交通大学徐天乐教授团队联合北卡罗来纳大学教堂山分校(UNC)宋娟教授团队,在Neuron期刊(IF=15)在线发表了题为“Ventral hippocampal NPY interneurons regulate circadian feeding in mice”的合作研究论文。在这项工作中,研究人员通过构建昼夜节律紊乱小鼠模型,结合化学遗传、钙成像、脑片电生理、脑区埋管给药和功能性磁共振成像(fMRI)等方法,揭示了腹侧海马表达神经肽Y的中间神经元(vHPC NPY-INs)在调控摄食昼夜节律中的关键作用,阐明了vHPC NPY信号和γ-氨基丁酸(GABA)信号分别介导调节白天和夜间摄食的特异性功能,并解析了内侧视前区(MPOA)到vHPC NPY-INs神经环路的结构与功能特征,明确了vHPC NPY-INs通过下游脑区腹侧海马下托(vSub)的神经肽Y1受体(NPY1R)和神经肽Y2受体(NPY2R)实现对摄食昼夜节律的调控。这些发现不仅拓展了对摄食节律神经机制的理解,也为揭示昼夜节律紊乱相关的代谢性疾病的发病机制提供了新的理论依据。
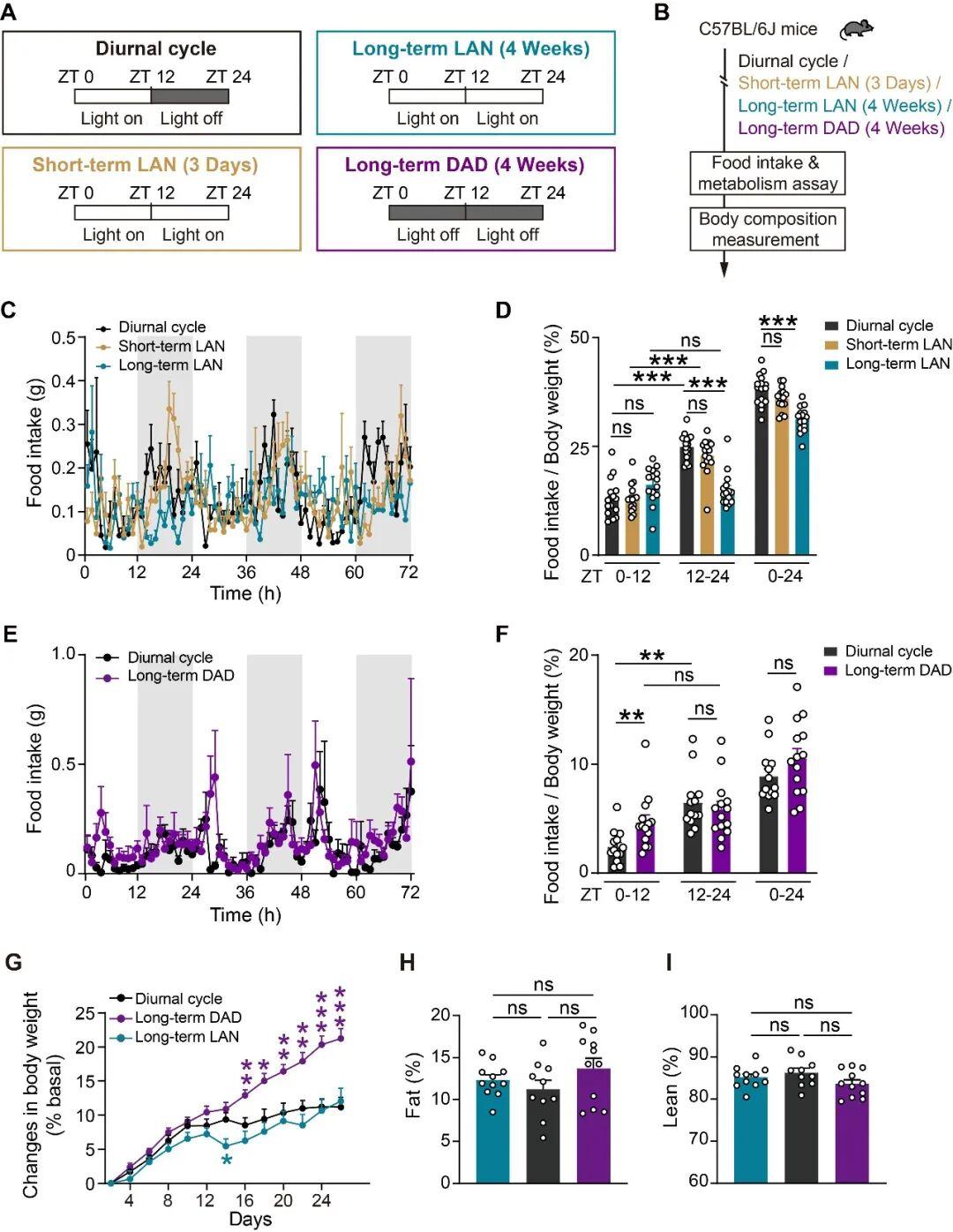
首先,通过对小鼠进行长期夜间光照处理(light at night,LAN)和长期日间光照剥夺(dark at day,DAD)处理,作者构建了两种昼夜节律紊乱的小鼠模型,而后对造模小鼠和对照小鼠的摄食量和能量代谢指标进行检测,结果显示:与正常昼夜节律下的对照组小鼠相比,经历长期DAD处理小鼠的白天摄食量显著增加,而经历长期LAN处理小鼠的夜间摄食量显著减少。同时,其他代谢和运动相关指标的昼夜节律性也表现出明显失衡(图1)。
图1:长期光照紊乱改变小鼠食物摄入的昼夜节律
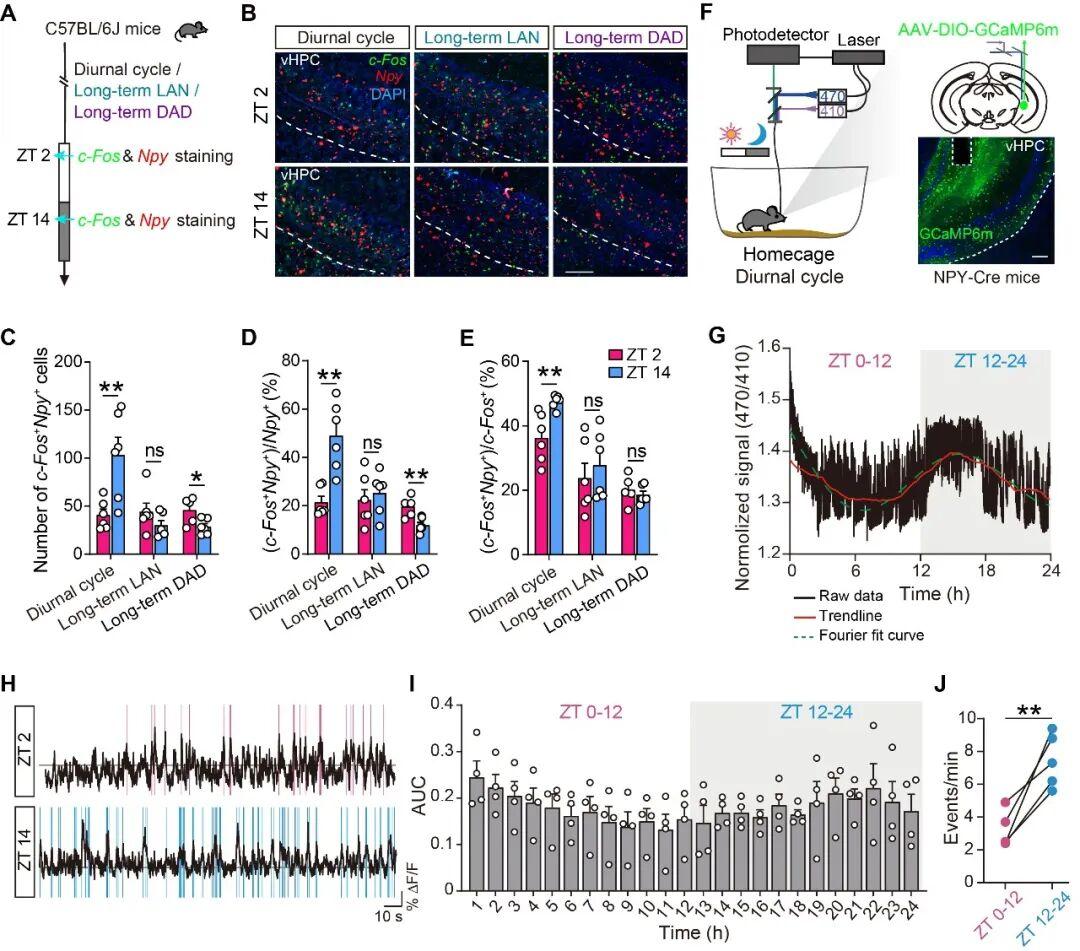
接着,通过实时在体钙离子(Ca2+)信号记录和离体脑片免疫荧光c-Fos染色,作者发现小鼠vHPC NPY-INs的活动呈现昼夜节律性,即白天活性较低,夜间活性较高。这一神经元层面的昼夜节律性与小鼠的摄食节律同步,即在正常昼夜节律下,小鼠白天摄食较少,夜间摄食较多。而昼夜节律紊乱模型小鼠vHPC NPY-INs的昼夜活性节律则被破坏(图2)。
图2:昼夜节律紊乱破坏vHPC NPY-INs活动的昼夜节律
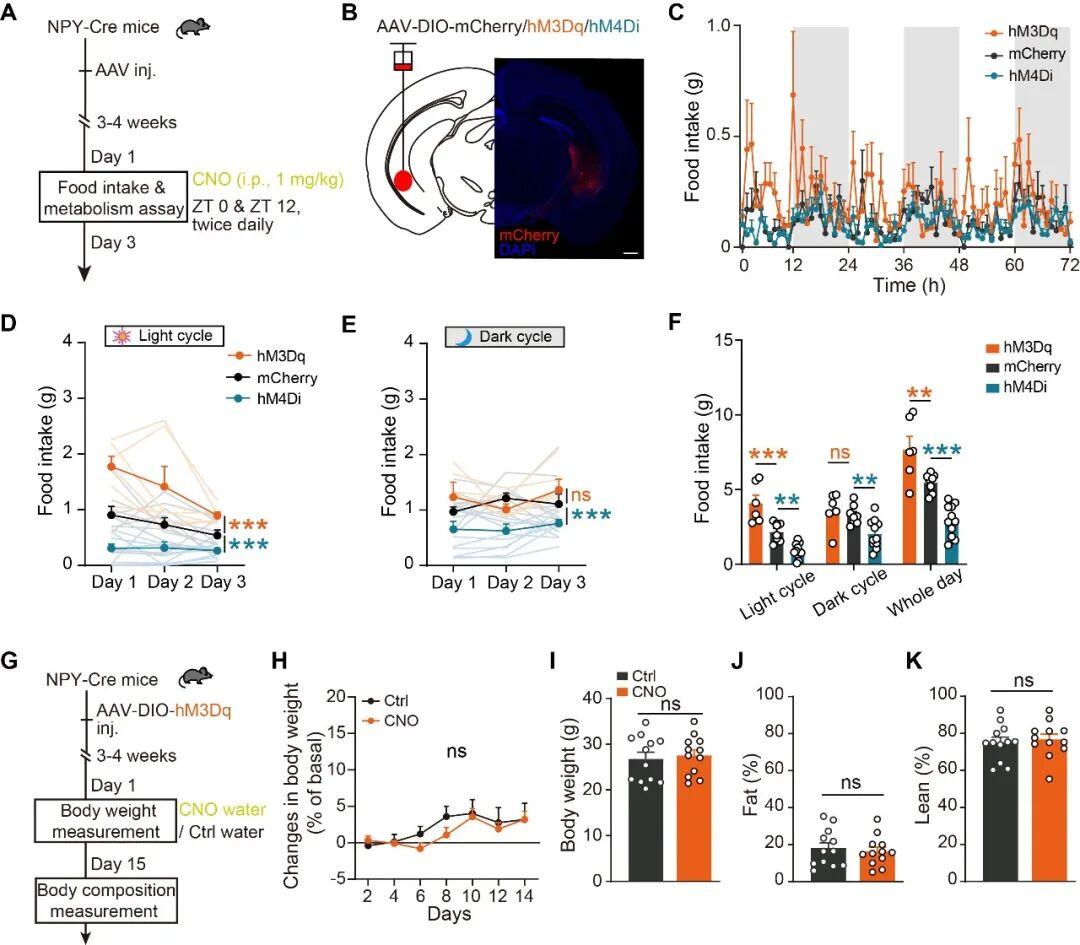
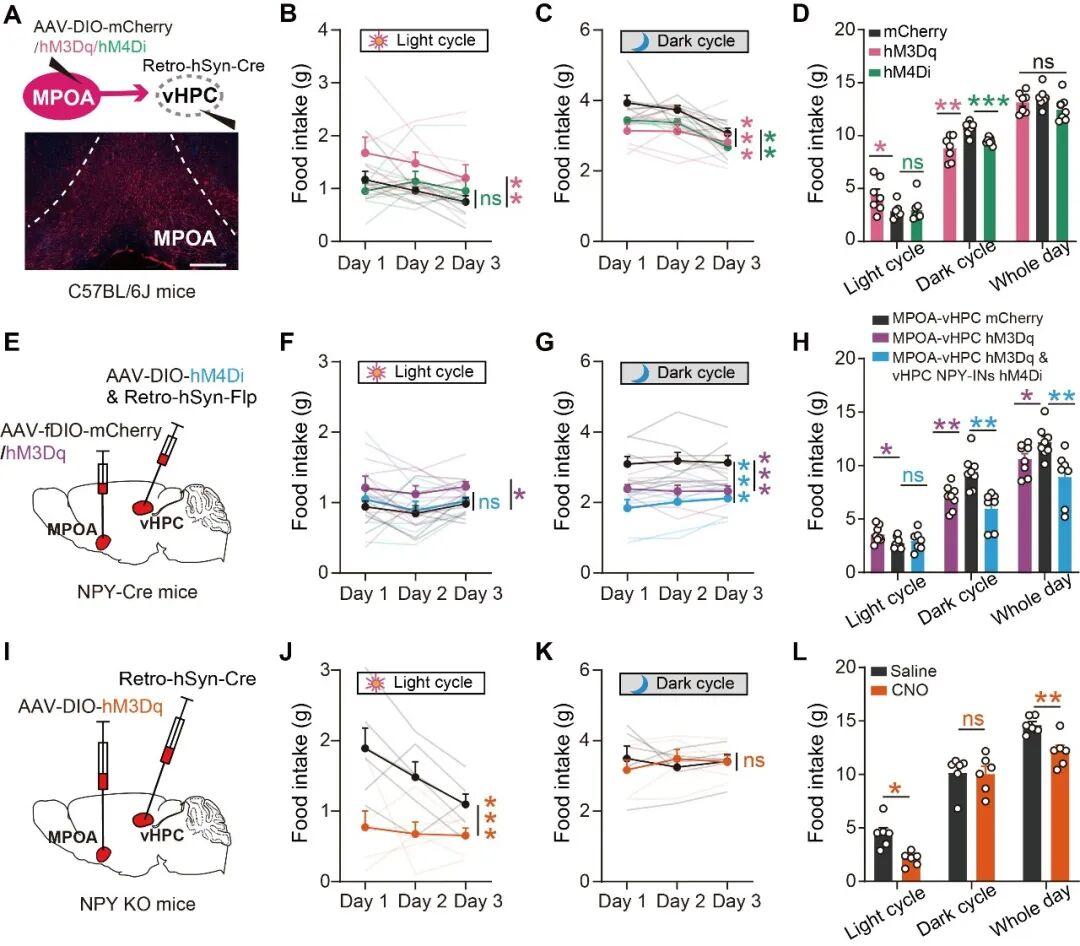
进而,通过化学遗传学激活或抑制vHPC NPY-INs,作者发现vHPC NPY-INs对小鼠的摄食调控是充分且必要的,并且呈现出对白天摄食量更强的干扰作用(图3)。
图3:vHPC NPY-INs对小鼠昼夜周期内的摄食量发挥充分且必要的调控作用
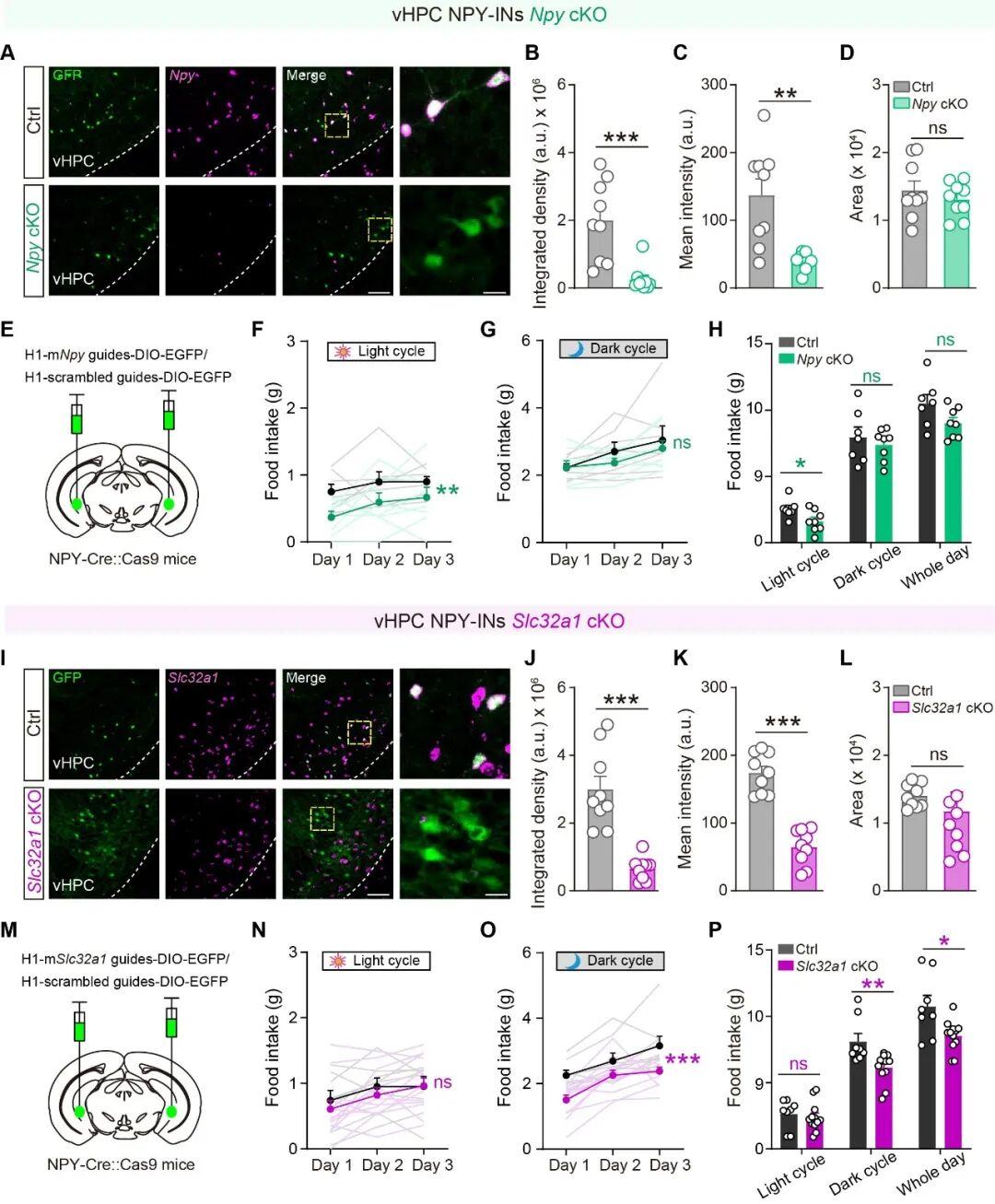
以往研究表明,vHPC NPY-INs可以共释放NPY和GABA,为了进一步探讨vHPC NPY-INs释放的NPY或GABA对摄食昼夜节律调控的作用,作者利用CRISPR基因编辑技术,分别敲减vHPC NPY-INs中的Npy或Slc32a1(编码囊泡GABA转运体VGAT),并检测其对摄食昼夜节律的影响。结果表明,vHPC NPY-INs释放的NPY信号介导白天摄食量的调控,而GABA信号则介导夜间摄食量的调控(图4)。
图4:vHPC NPY-INs分别利用NPY和GABA调节不同昼夜时相的摄食量
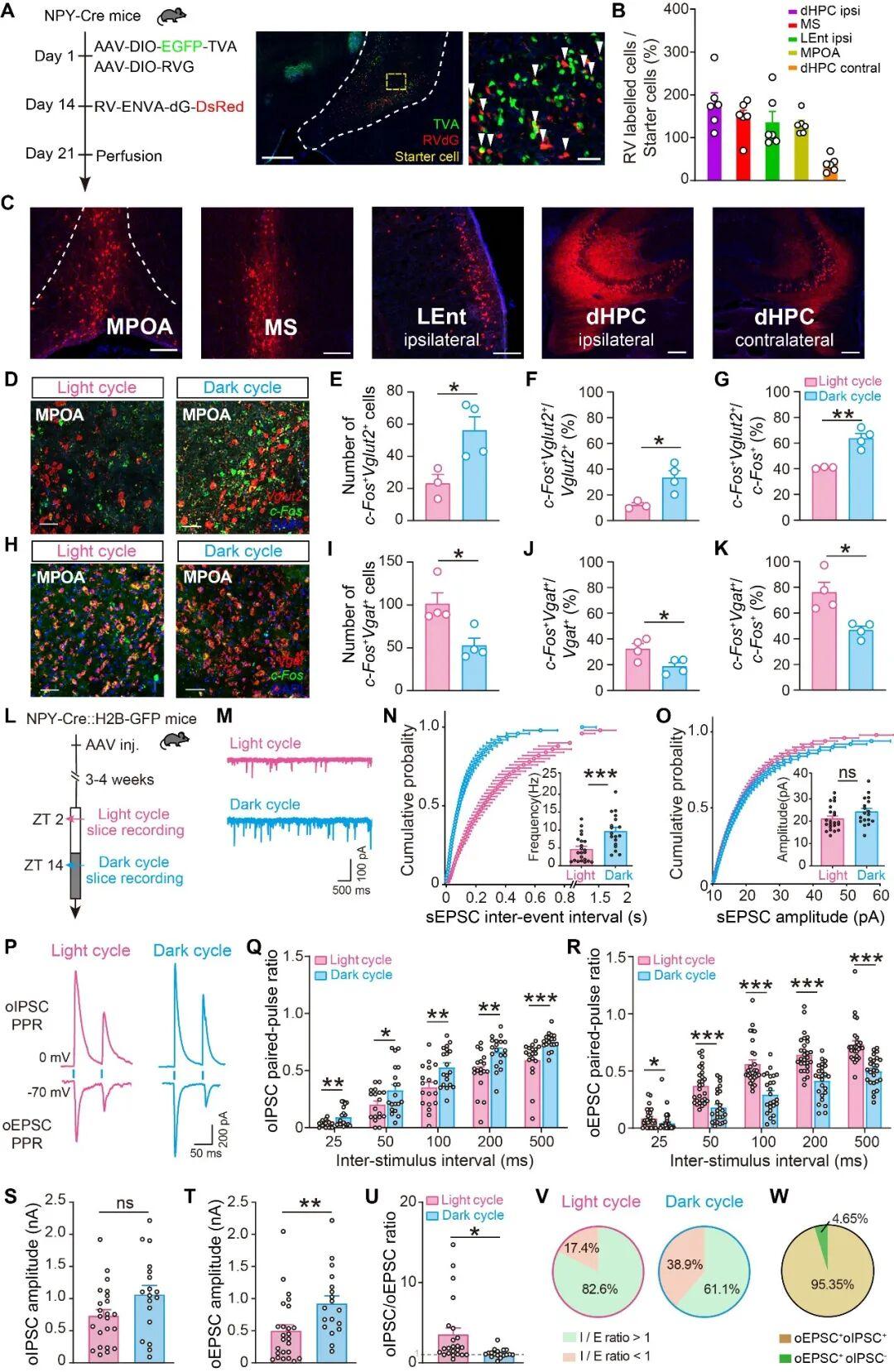
进一步地,作者解析了vHPC NPY-INs参与调控摄食昼夜节律的上、下游神经环路机制。具体而言,通过基于伪狂犬病毒(RV)的逆行跨单突触示踪技术,鉴定出vHPC NPY-INs的多个解剖学上游脑区。随后通过化学遗传学干预验证,确定了MPOA是vHPC NPY-INs调控摄食昼夜节律的功能性上游脑区。
为了解析MPOA脑区作为功能性上游调控vHPC NPY-INs的突触可塑性机制,作者进行了白天和夜间的脑片电生理记录,结果显示:vHPC NPY-INs同时接收来自MPOA的谷氨酸能和GABA能单突触输入。此外,作者通过RNAscope原位杂交技术结合c-Fos染色发现,MPOA的GABA能神经元和谷氨酸能神经元在白天和夜间的活性模式相反,即GABA能神经元白天活性较高,夜间活性较低,而谷氨酸能神经元则与之相反。这一现象在离体脑片的电生理记录中也得到了验证,即来自MPOA的抑制性输入在白天较强,夜间较弱;兴奋性输入则在白天较弱,夜间较强,由此共同决定了vHPC NPY-INs的昼夜节律性(图5-6)。
图5:MPOA昼夜兴奋性和抑制性输入介导vHPC NPY-INs的昼夜节律可塑性
图6:vHPC NPY-INs调节摄食昼夜节律的功能性上游为MPOA
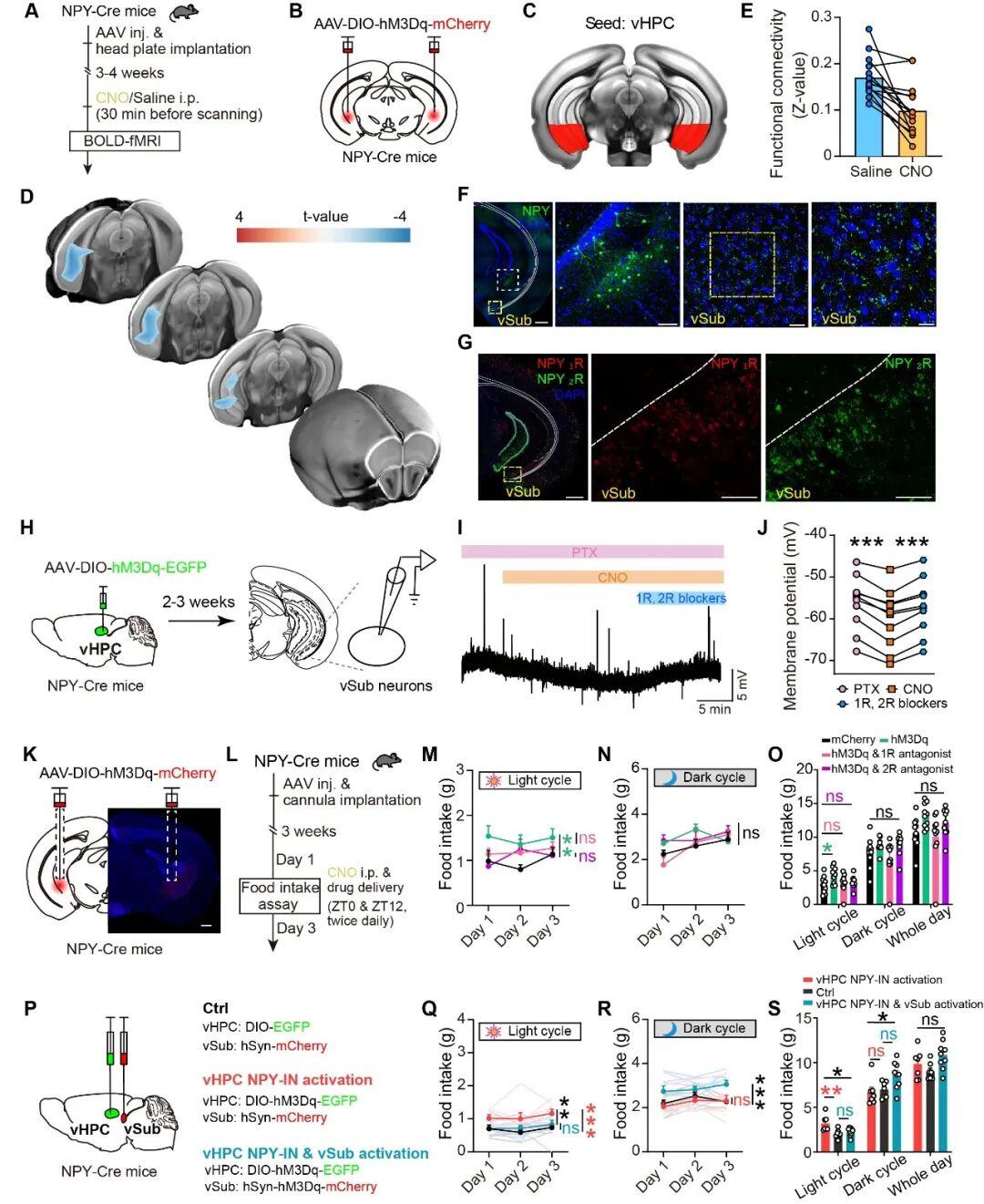
为了在小鼠清醒状态下从全脑范围内筛选vHPC NPY-INs激活后引起的脑区活性变化,作者运用fMRI技术,初步证实了vSub为vHPC NPY-INs的潜在下游脑区。进而,通过小鼠脑区埋管给药实验,揭示了vHPC NPY-INs通过调控vSub的NPY1R和NPY2R来调节小鼠的摄食昼夜节律(图7)。
图7:vHPC NPY‑INs通过vSub中的NPY1R和NPY2R信号调控光照周期摄食
结论
该研究表明,小鼠的vHPC NPY-INs活性表现出与摄食节律相关的昼夜节律变化:白天摄食量较少,vHPC NPY-INs活性较低;夜间摄食量较多,vHPC NPY-INs活性较高。这种昼夜不同的神经元活动状态可被LAN和DAD处理诱导的昼夜节律紊乱所破坏。此外,这群vHPC NPY-INs对小鼠昼夜周期摄食量的调控具备充分必要性,进而影响摄食昼夜节律。其中,该类神经元释放的NPY信号参与调控小鼠白天摄食量,而GABA信号参与调节小鼠夜间摄食量。膜片钳记录及c-Fos染色的结果表明,其功能性上游脑区MPOA神经元,通过向vHPC NPY-INs传递兴奋性与抑制性投射的昼夜可塑性变化,调节vHPC NPY-INs的昼夜活性及递质释放,进而通过下游脑区vSub的NPY1R和NPY2R实现对小鼠昼夜摄食量的调节。
创新点:该研究首次揭示了非经典摄食脑区vHPC中的NPY阳性中间神经元参与调控小鼠摄食的昼夜节律。并解析了其上下游环路及其突触可塑性和分子机制,为昼夜节律失调相关摄食和代谢疾病的治疗提供了潜在的理论依据。
总结图
上海交通大学医学院博士研究生焦志涵、博士后吴延娇、博士研究生边鑫为论文的共同第一作者。上海交通大学医学院徐天乐教授和宋兴磊博士、美国UNC宋娟教授为论文的共同通讯作者。上海交通大学医学院松江研究院李亚东研究员提供了合作支持。该研究得到了国家自然科学基金委、科技创新2030-脑科学与类脑研究重大项目、上海市教委创新团队项目等项目的支持。
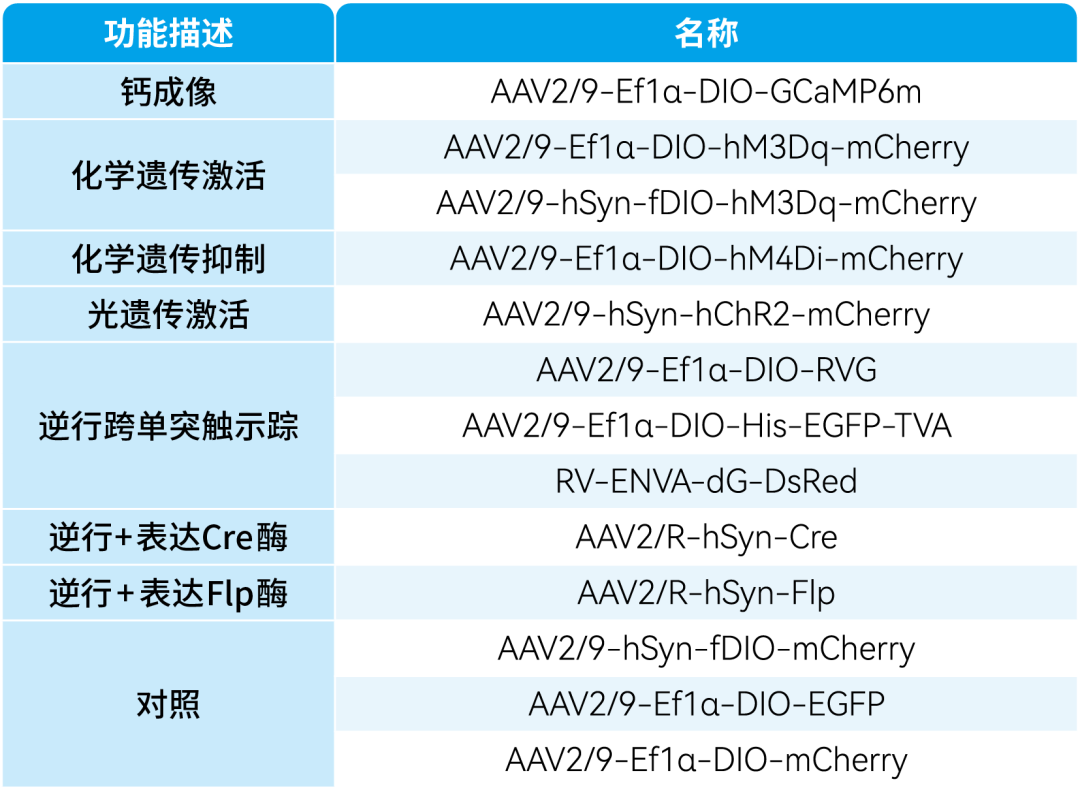
本文使用的来自枢密科技的病毒产品,列表如下:
扫码添加客服
更多产品及详情欢迎咨询!


市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK