2025-11-26 阅读量:492
成年神经发生在维持脑内稳态中发挥关键作用,且能对神经源性损伤产生应答。然而,成年哺乳动物脊髓的内在神经发生能力极其有限。脊髓损伤(spinal cord injury,SCI)后神经元再生与功能重建是目前最具挑战性的医学难题之一。直接谱系重编程可将终末分化的体细胞直接转分化为功能性神经元,无需经过iPSC(诱导多能干细胞)中间过程,既缩短了治疗的准备期,也降低了移植手术的风险。直接神经元重编程的新研究进展表明,直接转分化的特异性神经元可用于人类神经系统疾病建模和治疗,尽管已有较多研究报道神经胶质细胞可成功转分化为特定功能神经元,但通过直接神经元重编程产生运动神经元的研究较少,且转分化效率低、转录因子组合复杂。
2025年11月19日,华中科技大学张斌教授与江汉大学舒细记教授课题组在Cell Reports Medicine期刊(IF=10.6)在线发表了题为“Ngn2 and Isl1-mediated astrocyte-to-neuron conversion in vivo promotes functional recovery after spinal cord injury”的研究论文。在这项工作中,研究人员通过建立小鼠SCI模型,结合CRISPRa(CRISPR转录激活)基因编辑技术、神经元示踪及脊髓电生理等方法,明确了CRISPRa介导内源性转录因子神经生成素2(Ngn2)和胰岛因子1(Isl1)的激活可在SCI后再生功能性神经元。这些诱导神经元表达运动神经元和胆碱能神经元的特异性标志物,并与脊髓上行及下行通路形成突触连接。重要的是,星形胶质细胞向神经元的转分化可促进脊髓固有束轴突再生,改善肌肉的神经肌肉接头(NMJ)形态与功能,最终促进SCI后的运动功能恢复。
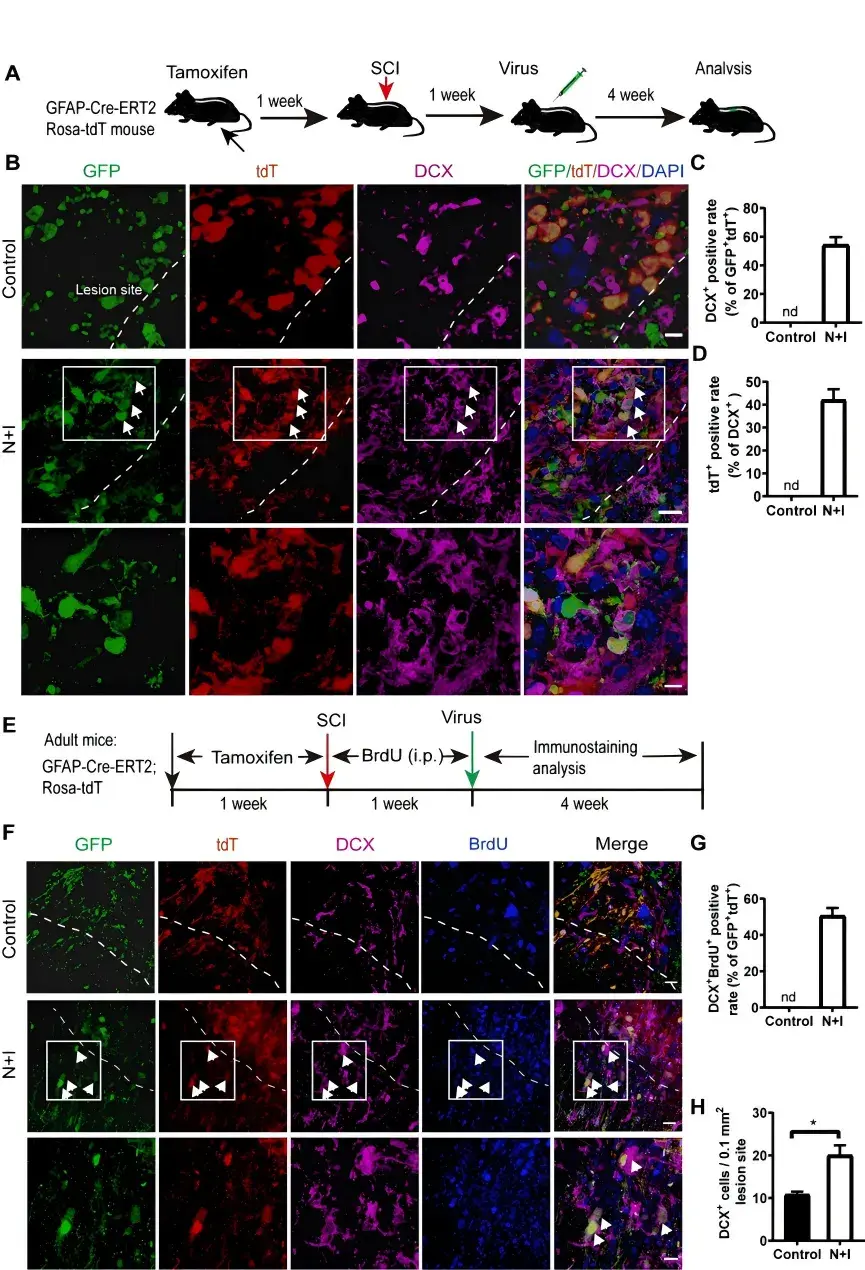
研究团队前期已发现激活Ngn2和Isl1能够诱导星形胶质细胞转分化为运动神经元。由于SCI后局部微环境发生变化,为了明确在病理条件下激活Ngn2和Isl1能否诱导反应性星形胶质细胞向神经元分化,作者通过谱系追踪,分别用星形胶质细胞特异性报告小鼠hGFAP-CreERT2;Ai14 mice,小胶质细胞特异性报告小鼠CX3CR1-Cre;Ai14 mice及NG2特异性报告小鼠Pdgfra-CreERT2;Ai14 mice,在SCI造模后一周注射腺相关病毒(AAV)激活Ngn2和Isl1,检测新生神经元特异性标志物双皮质素(DCX)的表达(图1)。结果显示,AAV感染的星形胶质细胞表达DCX,并且与BrdU(标记新生神经元)共定位,这表明激活Ngn2和Isl1能够诱导SCI模型星形胶质细胞神经发生。
图1.内源性Ngn2和Isl1激活诱导SCI模型星形胶质细胞神经源性重编程。
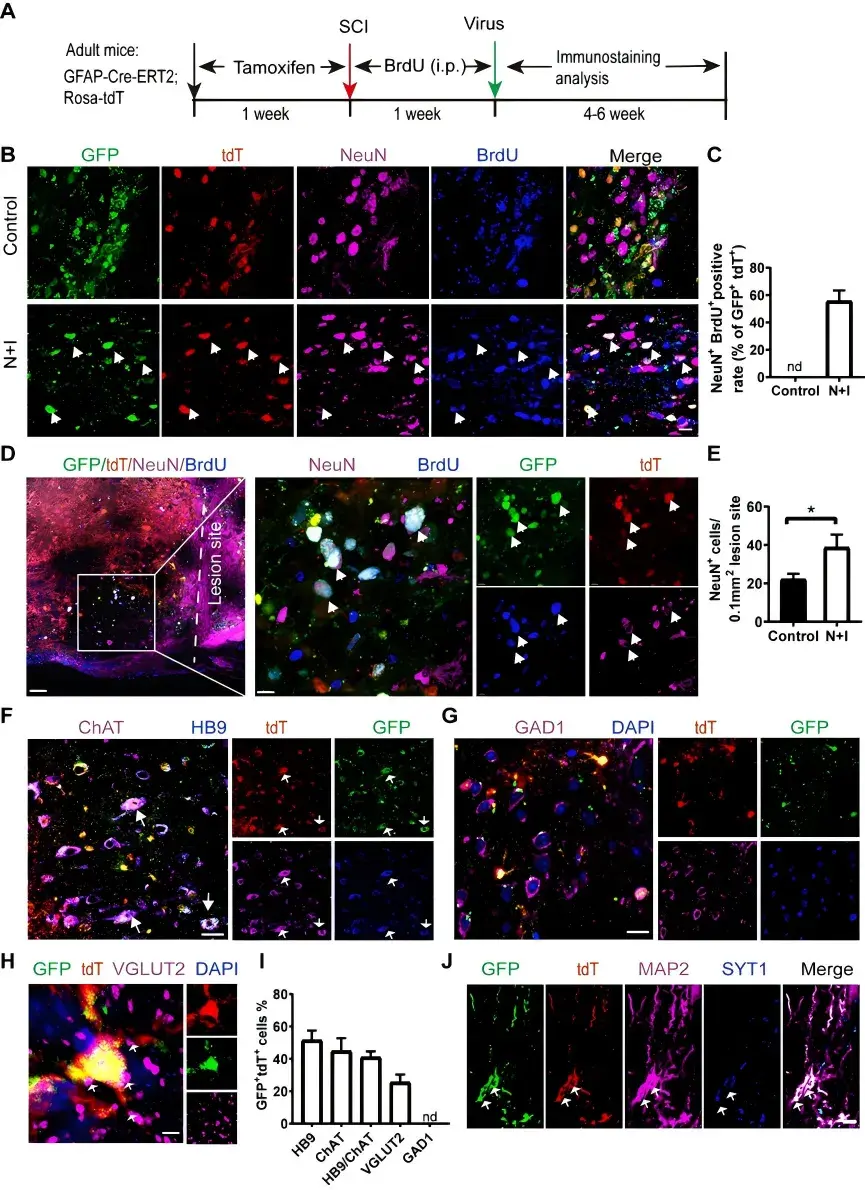
在检测到神经发生后,接下来研究了Ngn2和Isl1诱导病变区域的DCX+细胞是否可以发育成成熟的神经元。结果显示这些诱导的细胞表达NeuN(成熟神经元特异性标志物),并且与BrdU有共定位,表明它们是由星形胶质细胞经过重新编程形成的成熟神经元,而非内源性神经元(图2)。接着检测了诱导的神经元亚型,结果显示,诱导的神经元主要表达运动神经元特异性转录因子HB9(运动神经元身份标志物)及胆碱能神经元标志物ChAT(胆碱乙酰转移酶),并且表达突触前膜标志物突触结合蛋白1(SYT1)(图2)。以上结果表明,Ngn2和Isl1激活诱导SCI模型小鼠反应性星形胶质细胞转化为成熟胆碱能运动神经元。
图2.Ngn2和Isl1诱导反应性星形胶质细胞分化为成熟胆碱能运动神经元。
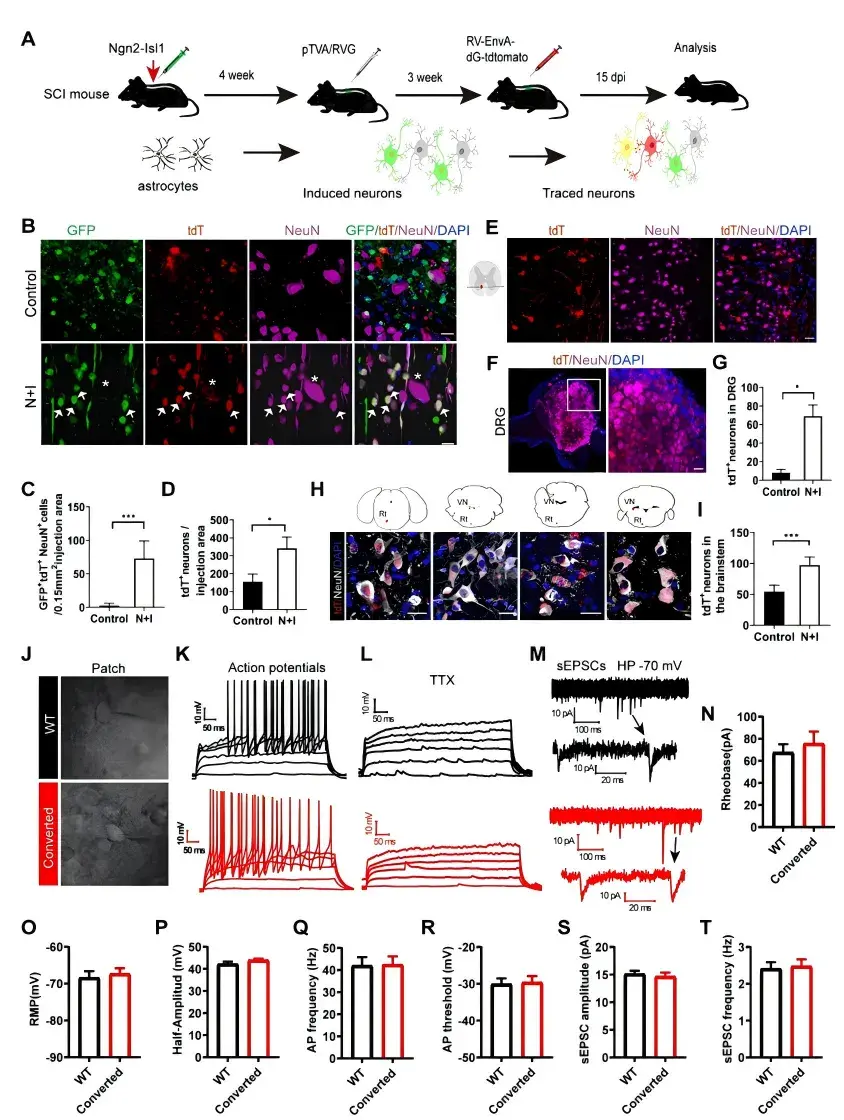
神经元之间的连接是细胞功能的基础。接下来,运用重组狂犬病病毒(RV)逆行跨单突触示踪方法来检测星形胶质细胞转化神经元的单突触连接。结果显示,同侧背根神经节(DRG)中部分神经元被tdTomato(tdT)标记追踪到,表明其与脊髓中诱导的神经元存在单突触连接。对大脑和脑干的连续冠状切片分析显示,在脑干网状核、前庭核,以及大脑运动皮层和小脑中,均可检测到与诱导神经元形成的单突触连接(图3)。以上结果说明,在SCI模型中星形胶质细胞转化的神经元可以与固有脊髓神经元以及运动皮层、脑干、小脑和DRG中的神经元形成单突触连接。
然后,通过全细胞膜片钳记录来评估星形胶质细胞转化神经元的电生理特征,结果进一步证实在SCI模型中星形胶质细胞转化的神经元能够整合到局部突触环路中(图3)。
图3.星形胶质细胞转化的神经元在SCI后形成突触连接。
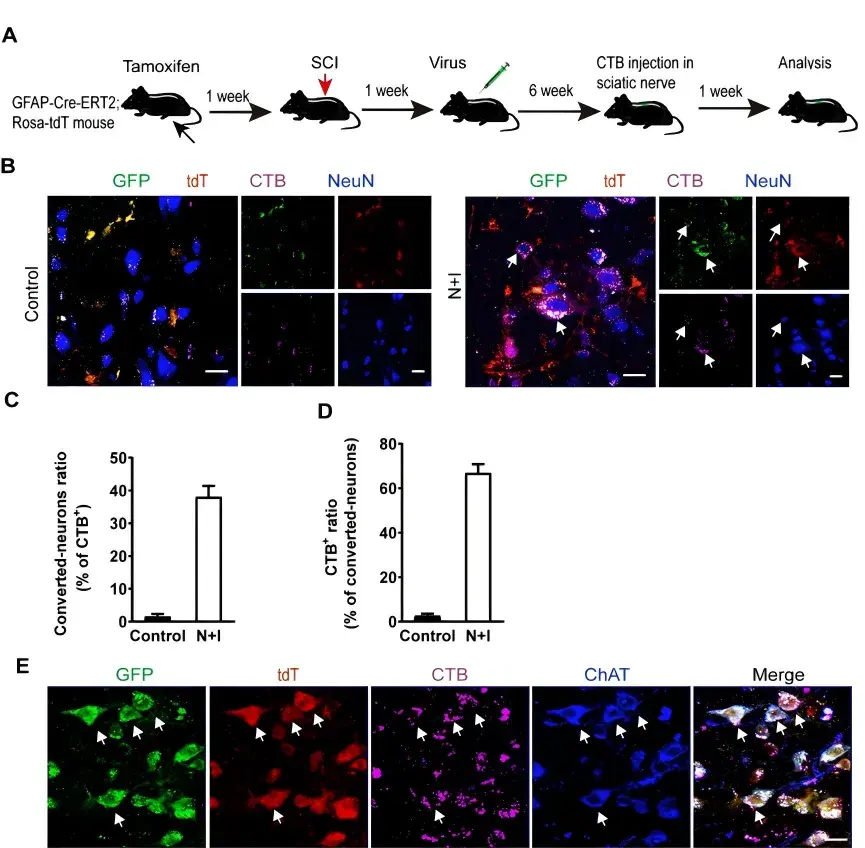
紧接着,作者通过神经元逆行示踪技术检测了这些星形胶质细胞诱导神经元的轴突投射情况,结果显示,诱导的神经元可以投射到坐骨神经(图4)。
图4.诱导的神经元投射到坐骨神经。
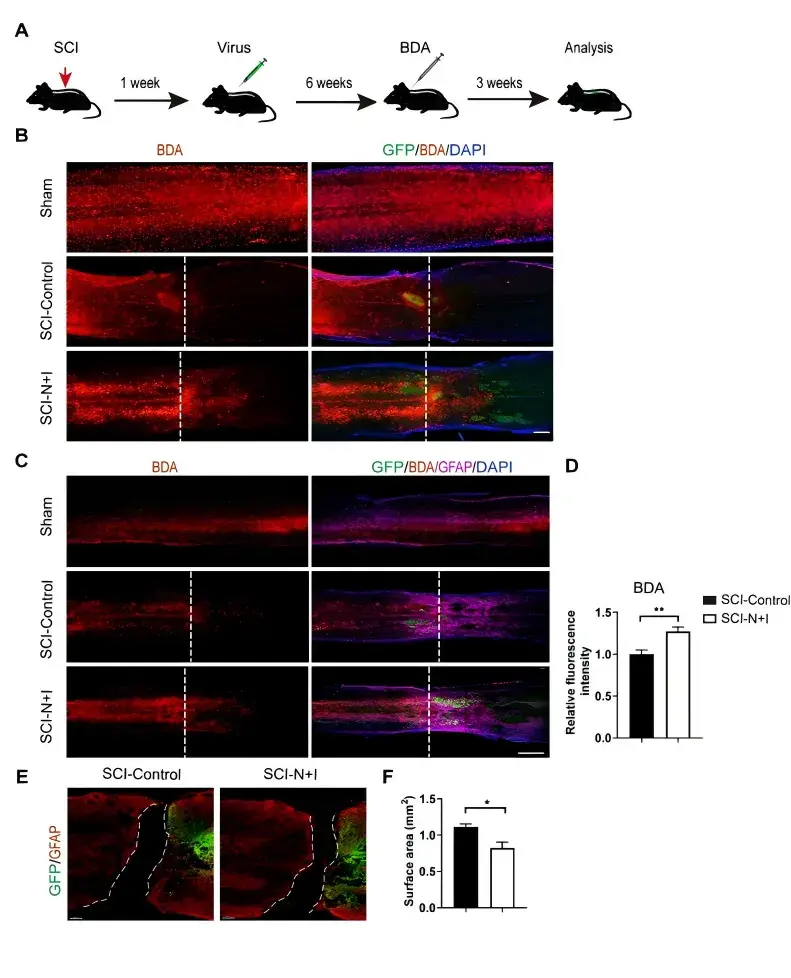
作者通过神经元顺行示踪,发现诱导星形胶质细胞向神经元转化能够有效促进脊髓固有神经元轴突再生(图5)。这提示,Ngn2和Isl1诱导的星形胶质细胞-神经元转化可能改善SCI后的病理微环境,促进脊髓固有轴突再生。
图5.星形胶质细胞-神经元转化促进SCI后脊髓固有轴突再生。
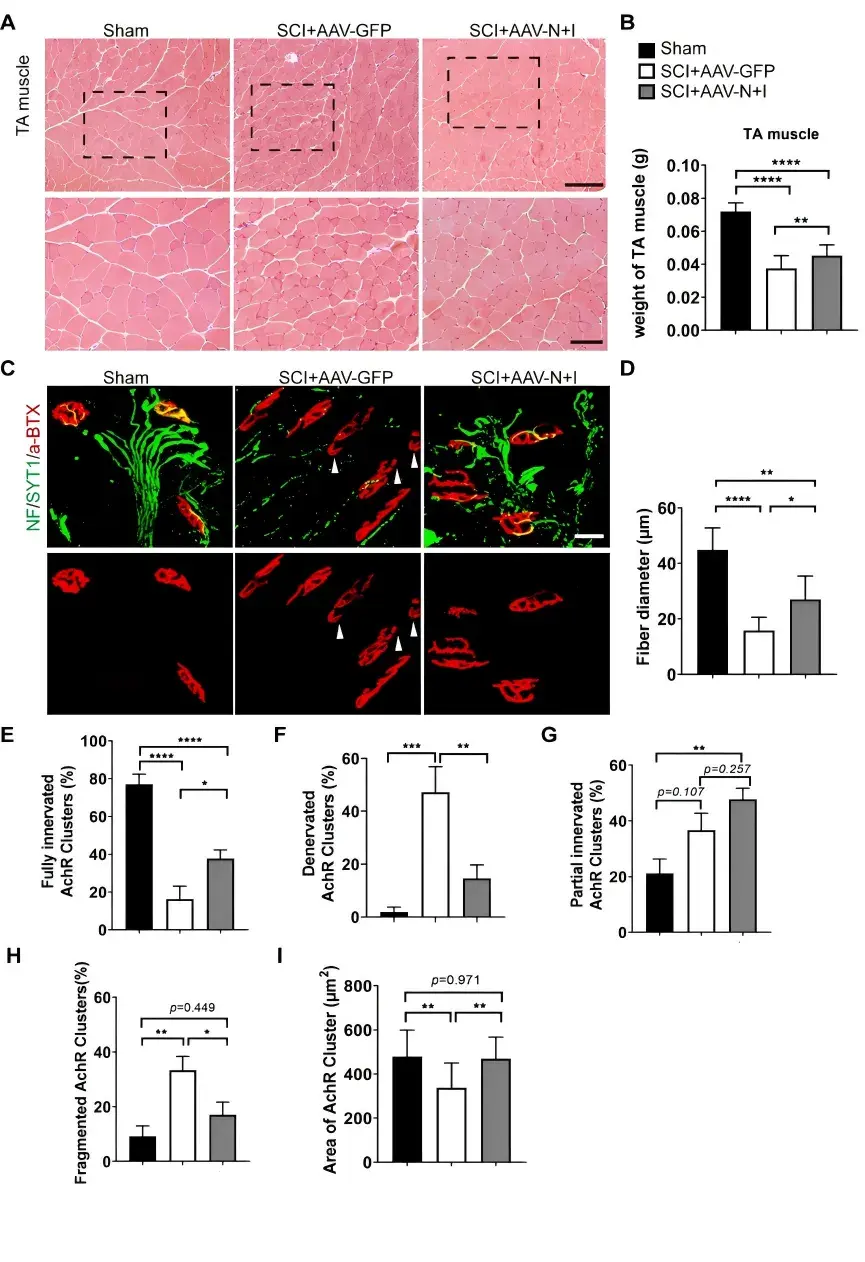
SCI后通常会发生肌肉萎缩,接着作者评估诱导星形胶质细胞向神经元转化是否可改善肌肉萎缩和神经肌肉接头(NMJ)形态和功能。结果显示,星形胶质细胞向神经元的转化能改善SCI小鼠胫前肌(TA)的萎缩程度,并且改善了NMJ形态和功能(图6)。
图6.神经元转化改善SCI小鼠TA的NMJ形态和功能。
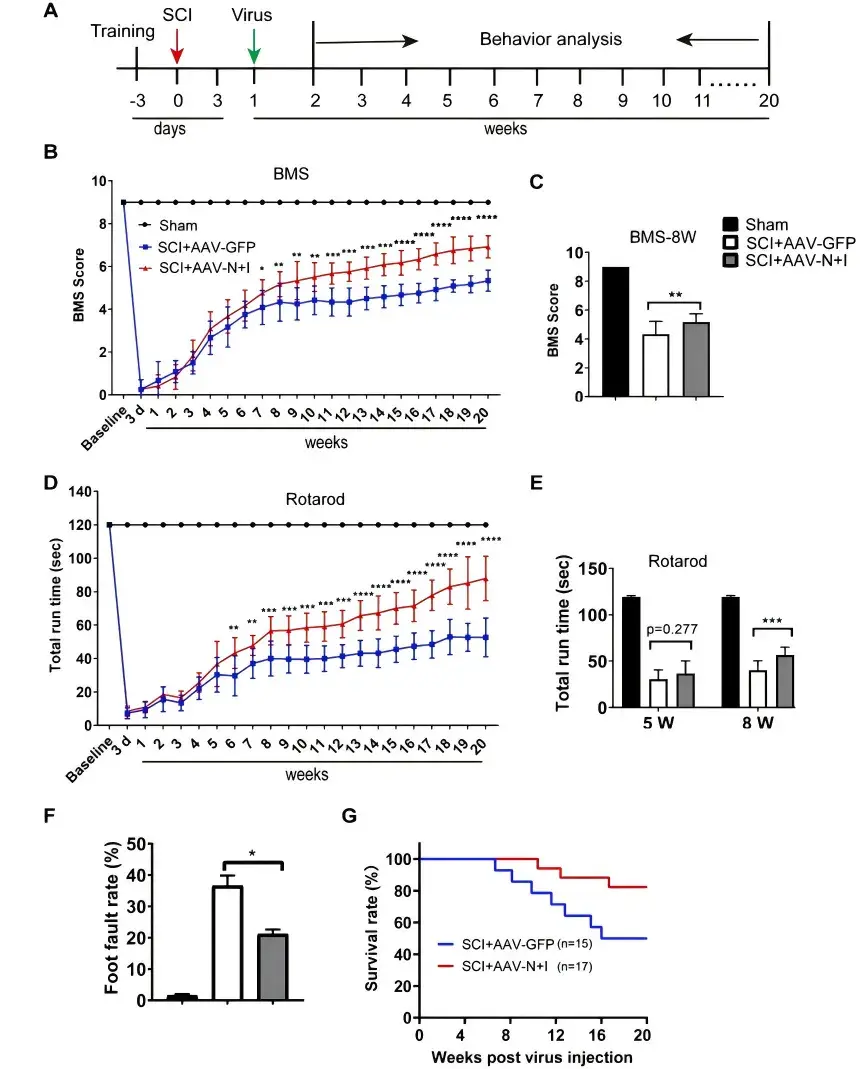
由于作者已经发现,Ngn2和Isl1介导的星形胶质细胞向神经元转化后,在SCI小鼠模型中损伤区域的神经再生水平显著增加,接着作者进一步研究了这种方法是否可以挽救SCI小鼠的运动缺陷。通过行为学检测,结果显示,星形胶质细胞向神经元转化后,小鼠运动功能较对照组显著增强,并且能够显著增加SCI小鼠生存率(图7)。以上结果说明,在体星形胶质细胞向神经元的转化可以改善SCI后的运动功能,延长寿命。
图7.神经元转化促进SCI小鼠运动功能恢复。
结论
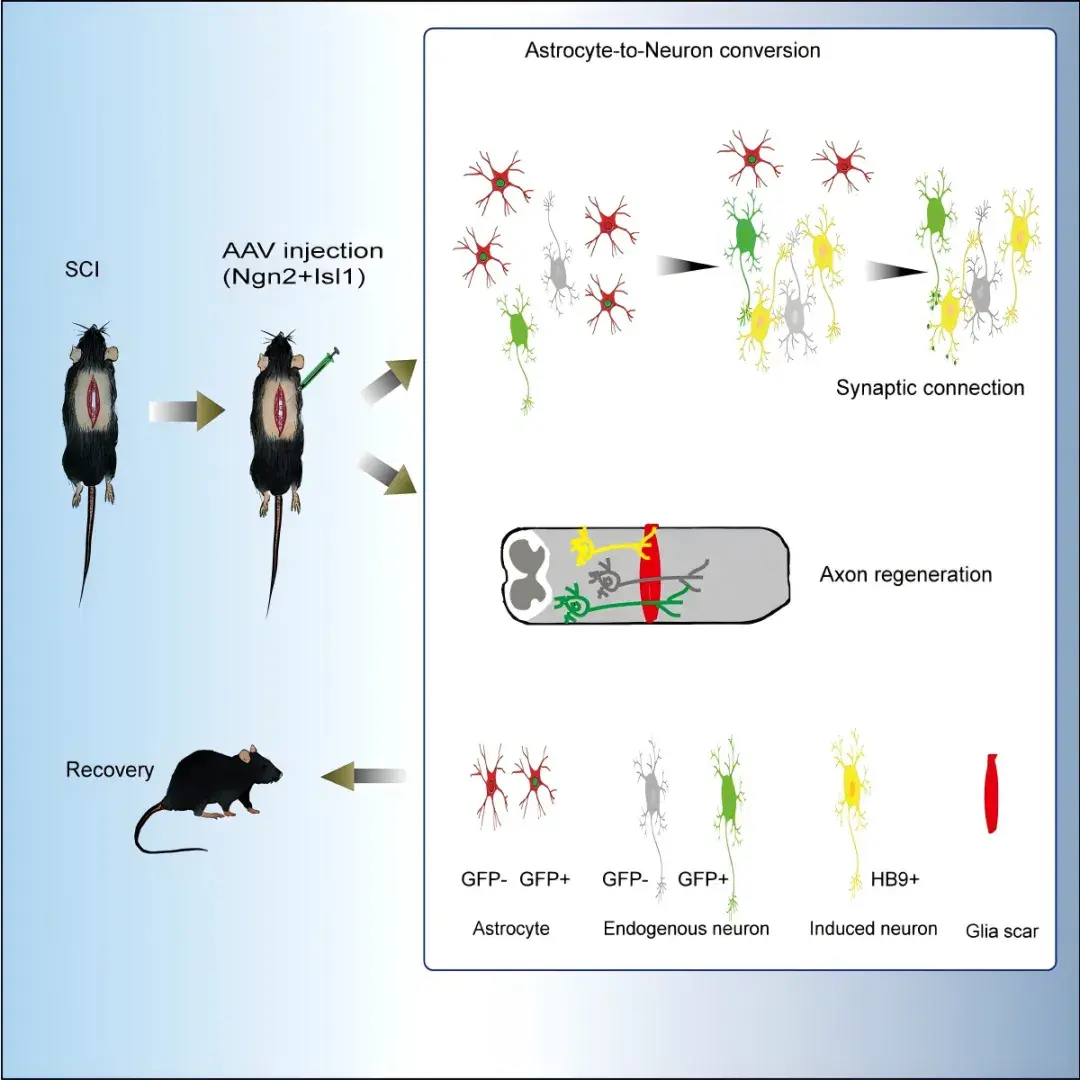
综上,结合基因编辑技术、神经元示踪、谱系追踪和脊髓电生理等技术,探明了激活内源性转录因子Ngn2和Isl1可在SCI后诱导反应性星形胶质细胞转分化为功能性神经元,并与脊髓的上行和下行通路形成突触连接。且星形胶质细胞向神经元的转化促进脊髓固有轴突的再生,改善NMJ的形态和功能,最终促进SCI后的运动功能恢复(图8),该研究一方面有助于解决谱系重编程相关的争议,另一方面作为一项概念验证研究或许能为脊髓修复开辟一条新途径。
图8.神经元转分化促进SCI后功能恢复示意图
江汉大学教师周美玲博士为论文的第一作者,华中科技大学张斌教授和江汉大学舒细记教授为论文的共同通讯作者。本研究得到了国家自然科学基金委和湖北省科技厅的资助。
舒细记教授课题组合照
通讯作者介绍
张斌,华中科技大学生理学系教授,博士生导师。2003-2013年在美国University of Alabama at Birmingham和Medical College of Georgia从事神经肌肉接头(NMJ)形成发育的分子机制,以及NMJ相关的神经疾病的发病机理研究。回国后课题组长期从事神经生物学领域的研究,已在Stem Cell Reports、Clinical and Translational Medicine、Cellular and Molecular Life Science等学术杂志发表多篇论文。研究兴趣与方向包括:运动神经元相关的神经疾病的发病机理和治疗策略;以NMJ为模型研究神经突触形成发育的分子机制;神经胶质细胞生理功能和相关疾病的病理机制。
舒细记,教授,江汉大学医学部常务副部长、认知与情感障碍湖北省重点实验室主任。主持、参与及指导国家自然科学基金项目13项,主持、参与教育部产学合作育人项目、就业育人项目等省部级科研项目10余项,近五年在《Cell》、《Nature Communications》、《Science Advances》等国际顶刊发表系列代表性成果,相关研究被《Cell》、《Nature Reviews Molecular Cell Biology》、《Nature Reviews Neurology》等权威期刊正面评述与广泛引用300余次。舒细记教授团队长期专注于神经退行性疾病的病理机制解析与早期诊断研究。
本文使用的来自枢密科技的病毒产品,列表如下:


了解产品及服务
请扫码添加客服微信:BrainVTA2020

市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK