2025-11-03 阅读量:391
古人云“知足常乐”,《中庸》亦有“过犹不及”之论,这些智慧都指向同一个道理:凡事皆有其度,恰到好处方为上策。在生物体内,这种平衡艺术同样展现得淋漓尽致——当身体缺水时会主动寻找水源,一旦需求得到满足便会自然停止摄取。这一看似平常的生理过程,实则体现了神经系统令人叹为观止的精密调控能力。
传统的饮水调节理论主要关注血液成分监测系统,特别是脑室周围器官(Circumventricular Organs,CVOs)等结构如何感受体液渗透压和血容量的波动,进而引发渴觉或饱水感的“反馈调节模式”。然而,越来越多的研究发现,实际的饮水行为启动和停止时间往往远早于血液指标的实际变化——这表明存在来自消化道和口咽部的“前馈预警系统”。本项研究正是要探索这一预测性调控的核心原理:即在体液平衡尚未真正恢复之前,神经系统如何提前发出停止饮水的信号。
相信每个人都有这样的切身感受:感到口干时,仅仅喝下少量水分就能迅速消除不适感。但从生理反应来看,水分从进入口腔到真正被吸收并影响血液渗透压,通常需要几分钟乃至更长时间。这就产生了一个引人深思的科学问题:在水盐平衡尚未实际恢复的情况下,我们的机体是通过什么方式提前“预测”已经摄入了充足的水分?这种精准的“分寸把握”能力,恰恰展现了生命调控系统的卓越智慧。
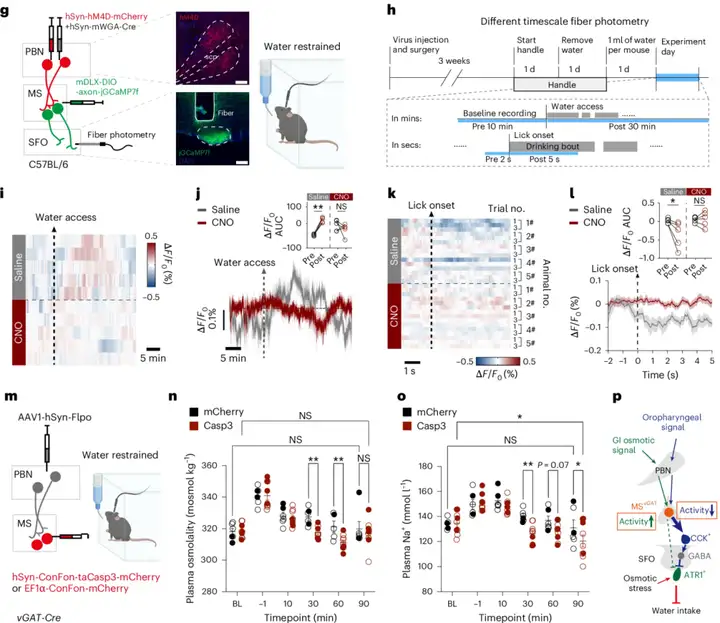
近日,浙江中医药大学陈忠教授团队在《Nature Neuroscience》上发表了文章“A bottom-up septal inhibitory circuit mediates anticipatory control of drinking”。该研究利用光遗传学,双光子记录和spatial-seq(空间转录组测序)等技术揭示了一条从内侧隔核(Medial septum,MS)到穹窿下器官(the subfornical organ,SFO)的抑制性环路,参与小鼠饮水行为的预测性控制。MS的GABA能(MSvGAT)神经元通过臂旁核(Parabrachial nucleus,PBN)的信号输入,整合口腔和胃肠道信号,并进一步防止机体过度水合。它就像一位隐秘的指挥官,在你喝水开始时就已经准备好了“停止”信号。
陈忠教授团队长期致力于研究MS在摄食、认知等生理功能及癫痫等疾病中的作用(Biol Psychiatry. 2020; Curr Biol. 2022; Nat Commun. 2021, 2024; Cell Rep. 2025)[1-3]。在探究组胺H2受体如何在MS中介导摄食行为的神经环路基础时(Curr Biol. 2022)[3],团队意外发现,MSvGAT神经元在小鼠摄水行为过程中会出现与行为相关联的钙信号变化。这一意外发现引发了团队的浓厚兴趣:这是否意味着MS也参与了与摄水相关的某种信号传递?若是如此,MS在摄水行为中的生理意义和功能又是什么?
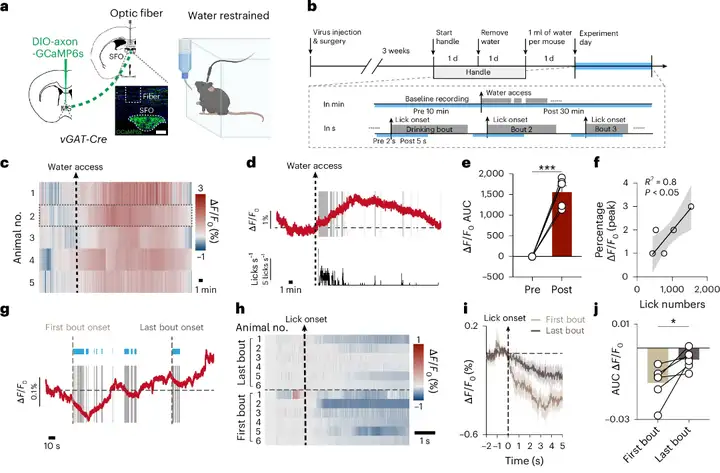
研究首先通过神经示踪技术确认,MS不仅是控制饮水行为关键中枢SFO的重要上游,且其GABA能神经元在水饱足状态下显著活跃。双光子成像进一步揭示,这些神经元在饮水过程中表现出独特的双相活动模式:饮水初始阶段活动迅速下降,随后在持续饮水过程中逐渐增强(图1)。这种活动模式提示MSvGAT神经元同时编码两类信息:舔舐开始时的口腔即时抑制性信号,以及随后逐渐增强的胃肠道感觉信号。
图1 MSvGAT能神经元在饮水过程中呈现双相活动模式
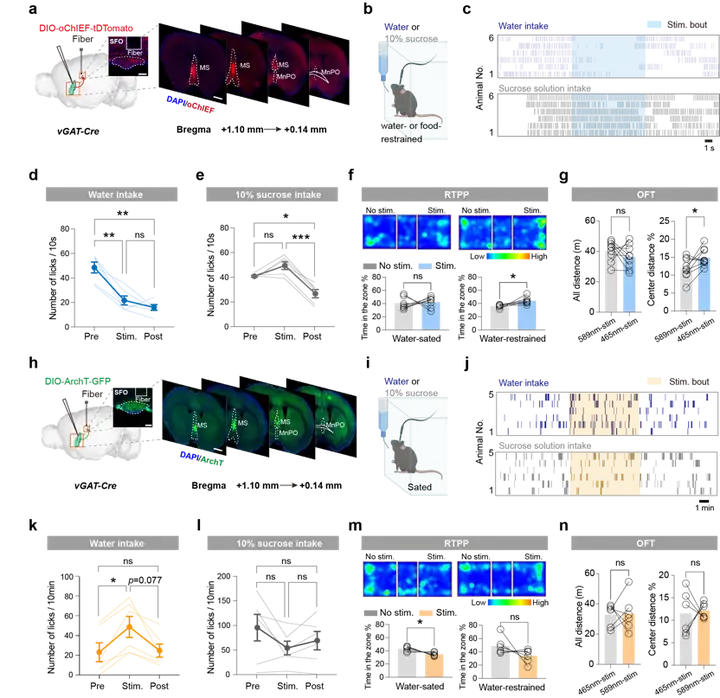
通过神经环路精准操控,研究人员发现激活MS-SFO的GABA能神经环路可立即中断口渴小鼠的饮水行为;相反,抑制该环路可使不口渴的小鼠也发生饮水行为(图2)。这表明该环路对饮水行为具有状态依赖性的双向调控作用:在口渴状态下激活该通路产生即时“止渴”效应;而在水分充足状态下抑制该通路则诱发“假性口渴”效应,延长饮水行为持续的时间。
图2 MSvGAT-SFO环路状态依赖性双向调控摄水行为
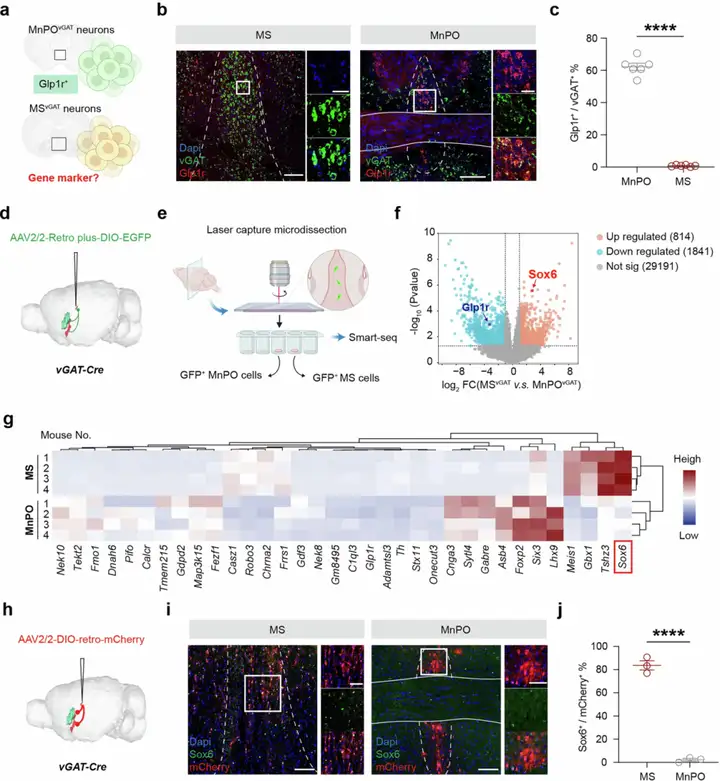
为了探索投射至SFO的MSvGAT神经元的分子特征,研究团队采用spatial-seq技术[4-5],发现这些神经元与毗邻的正中视前核(Median preoptic nucleus,MnPO)的GABA能(MnPOvGAT)神经元在基因表达上存在显著差异。具体而言,MnPOvGAT神经元主要由胰高血糖素样肽1受体(glucagon-like peptide 1 receptor,GLP1r)基因标记[6],而向SFO投射的MSvGAT神经元则选择性表达SRY盒转录因子6(SRY-Box Transcription Factor 6,Sox6)(图3)。Sox6被认为在体液平衡调控中发挥重要作用[7]。
图3 投射至SFO的MSvGAT神经元特异性表达Sox6
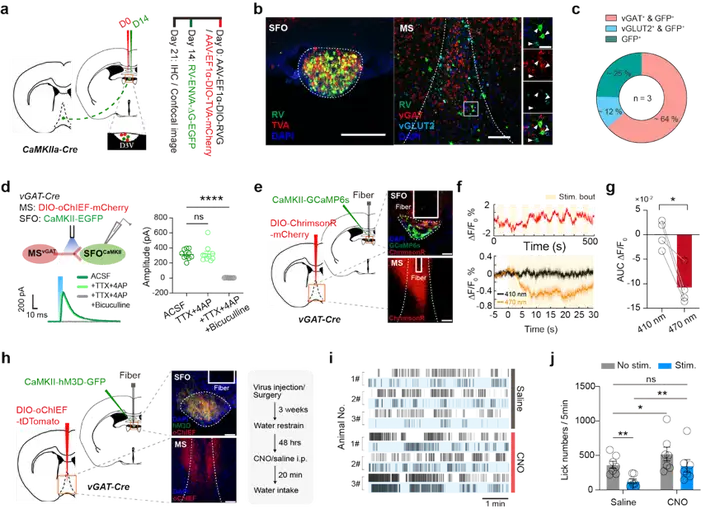
接下来,研究人员界定了MSvGAT神经元的下游SFO功能细胞类型。首先,狂犬病毒(RV)逆行跨单突触示踪与电生理记录证明了SFO的兴奋性CaMKII(SFOCaMKII)神经元是MSvGAT神经元的主要直接下游,二者形成抑制性单突触连接。进一步的功能连接实验表明,激活MSvGAT神经元可以光跟随性地即刻抑制SFOCaMKII神经元钙活动。关键的是,当在脱水状态下激活SFOCaMKII神经元时,可显著逆转光激活MSvGAT-SFO环路所产生的抑制摄水效应,表明SFOCaMKII神经元是这条抑制性环路调控饮水的核心“效应器”(图4)。
图4 SFOCaMKII神经元是MSvGAT神经元的主要下游效应细胞
那么,这些MSvGAT神经元是如何知道我们已经喝够水了呢?研究发现,这些神经元能够同时接收来自PBN输入的口腔和胃肠道信号,并将这些感官信息整合后传递至下游SFO,从而调控饮水行为。PBN作为关键信号的中转站,将口腔和胃肠道的感觉信息传递至MSvGAT神经元,为饮水调控提供了一个更完整的神经网络框架。切断PBN至MS的信号输入后,MSvGAT在饮水过程中的钙活动也被“钝化”,小鼠会过度饮水并发生低钠血症——这就像是没有了“刹车”的车辆,一路狂奔导致事故(图5)。
图5 MSvGAT神经元接收来自PBN的信号输入并预测性调控摄水行为
结论
本研究揭示了一条全新的预测性饮水调控神经环路,阐明了MSvGAT神经元如何通过接收PBN传递的口腔和胃肠道早期信号,提前终止饮水行为,维持机体水平衡。这一发现填补了“大脑如何在血液渗透压真正改变前预测性终止饮水”这一科学问题的重要空白。
尽管研究成果具有重要意义,但仍存在一些局限性。首先,这些发现主要基于小鼠模型,其在人类中的普适性有待验证。其次,MS-SFO环路与其他已知体液平衡调控机制的交互作用尚不清楚。此外,这一环路在病理状态下的功能变化也是未来值得探索的方向。
这项研究不仅深化了我们对饮水行为神经调控机制的理解,还为多种饮水障碍相关疾病(如糖尿病和精神分裂症相关的多饮症)的治疗提供了新的潜在靶点。未来研究可进一步探索这一环路在疾病状态下的功能变化,以及靶向干预该环路以治疗相关疾病的可能性。
Chen Lab部分人员合照(照片提供自Chen Lab)
该研究的第一作者为浙江中医药大学博士后徐玲钰(一排左二),浙江大学硕士研究生孙瑜浩(一排右三)、新加坡国立大学黄陈元博士以及浙江中医药大学郑艳榕研究员(二排右六)为共同第一作者,浙江中医药大学陈忠教授(二排左四)为本研究的通讯作者。本研究也得到了浙江中医药大学汪仪研究员(二排左五)、浙江大学药学院廖杰研究员的支持与指导。本研究获得了国家自然科学基金、浙江省自然科学基金重大项目、中国博士后科学基金、国家资助博士后研究人员计划的资助。
参考文献:
1.Wang, Y. et al. Direct Septum-Hippocampus Cholinergic Circuit Attenuates Seizure Through Driving Somatostatin Inhibition. Biol Psychiatry87, 843–856 (2020).
2.Cheng, L. et al. Histamine H1 receptors in dentate gyrus-projecting cholinergic neurons of the medial septum suppress contextual fear retrieval in mice. Nat Commun15, 5805 (2024).
3.Xu, L. et al. An H2R-dependent medial septum histaminergic circuit mediates feeding behavior. Current Biology32, 1937-1948.e5 (2022).
4.Liao, J. et al. De novo analysis of bulk RNA-seq data at spatially resolved single-cell resolution. Nat Commun13, 1–19 (2022).
5.Nichterwitz, S. et al. Laser capture microscopy coupled with Smart-seq2 for precise spatial transcriptomic profiling. Nat Commun7, 1–11 (2016).
6.Augustine, V. et al. Hierarchical neural architecture underlying thirst regulation. Nature555, 204–209 (2018).
7.Saleem, M. et al. Sox6 as a new modulator of renin expression in the kidney. Am J Physiol Renal Physiol312, F285–F297 (2020).
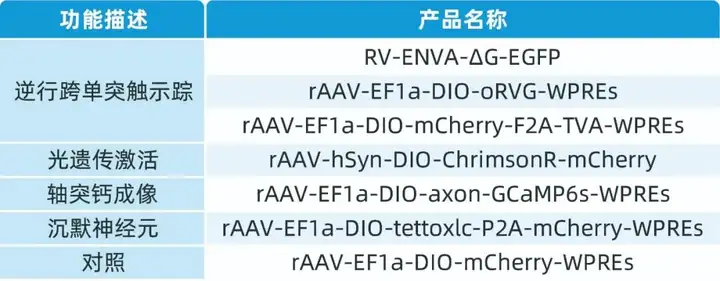
本文使用的来自枢密科技的病毒产品,列表如下:

了解产品及服务
扫码添加客服微信:BrainVTA2020

市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK