2024-05-09 阅读量:1338
众所周知,心脏具有自律功能,同时受复杂的神经网络控制,这种脑-心之间的调控,从脊髓至大脑皮层共同构成了错综复杂的心血管神经调控网络。如内侧前额叶和岛叶皮层、杏仁核和终纹床核、外侧下丘脑和下丘脑背内侧核及室旁核、中脑导水管周围灰质、臂旁区和延髓等多个脑区。大脑皮质损伤可导致心功能障碍,而心血管疾病也可引发大脑部分功能障碍,因此“脑-心轴”和“心-脑轴”研究备受关注。初级运动皮层(M1)不仅在运动执行功能中起主导作用,还参与高级认知功能和疼痛调节。M1与心脏的联系通过PRV追踪已证实,但M1调控心功能的具体机制和路径并未阐明。
2024年3月15日,陕西师范大学体育学院暨运动生物学研究所田振军教授团队联合脑与行为科学研究所贺志雄副教授等在《Advanced Science》(IF15.1)上在线发表题为“Manipulation of Glutamatergic Neuronal Activity in the Primary Motor Cortex Regulates Cardiac Function in Normal and Myocardial Infarction Mice”的文章,研究通过病毒示踪、fMOST三维成像、光遗传学、化学遗传学和钙成像等技术发现,小鼠初级运动皮层(M1)谷氨酸能神经元影响心功能,明确了下游中缝核(MnR)是M1回路中调节心功能的关键中继脑区之一,同时采用心肌梗死(MI)模型验证了病理状态下M1神经元活动通过MnR对心功能的影响。该研究为深入分析脑与心脏之间的确切调控关系提供了重要证据,为研究“脑心综合征”的发病机制和治疗提供了新思路。博士生薄文艳和青年教师蔡梦昕副教授为论文共同第一作者,田振军教授和贺志雄副教授为共同通讯作者。

研究结果
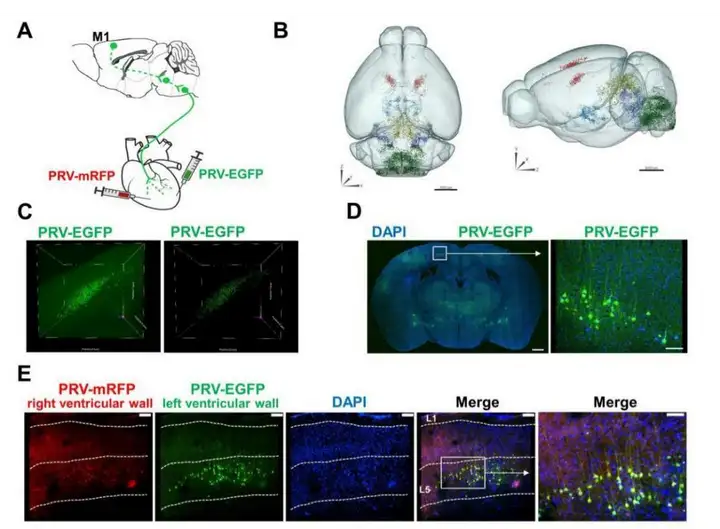
研究人员首先在左、右心室壁注射PRV-EGFP和PRV-mRFP,利用fMOST进行小鼠全脑三维重建,构建了小鼠“脑-心轴”神经全景图。发现M1脑区神经元存在EGFP和mRFP共标,且M1区被标记的神经元位于第5层(M1 L5)。表明 M1 L5神经元可能同时控制左心室和右心室的心肌活动。
图1. 利用fMOST对心源性注射伪狂犬病病毒的小鼠进行全脑成像
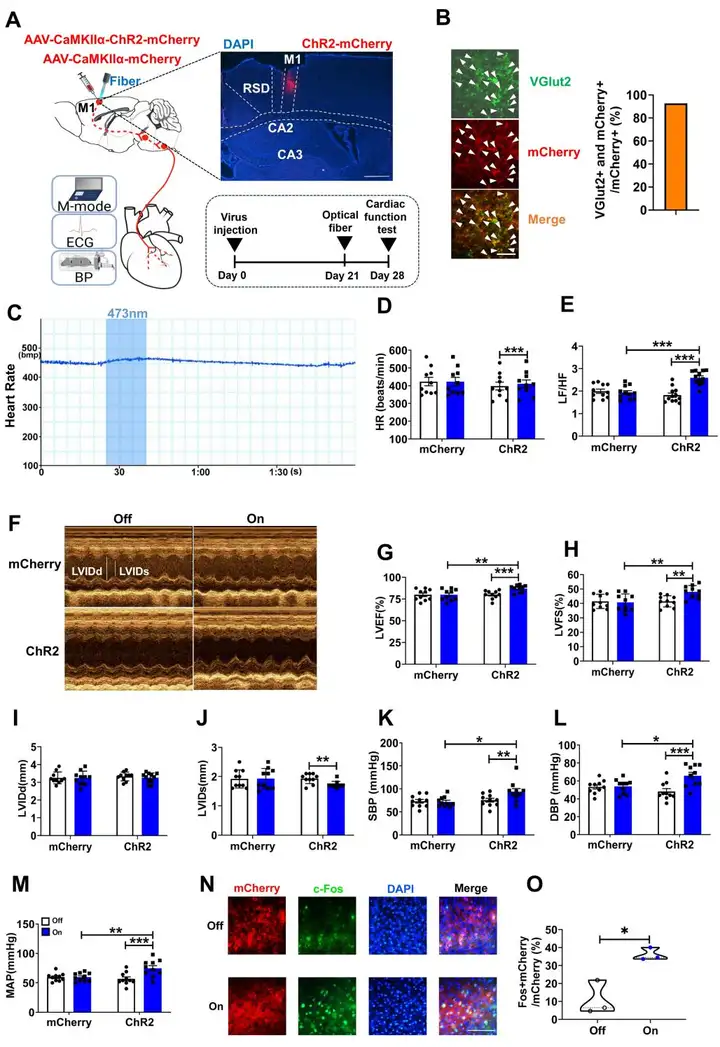
研究人员进一步通过光遗传学激活、化学遗传学失活和消融来操纵M1谷氨酸能神经元发现:光遗传激活M1谷氨酸能神经元显着增加心率(HR)、左心室射血分数(LVEF)、左心室缩短分数(LVFS)、增加收缩压(SBP)、舒张压(DBP)和平均动脉压(MAP);化学遗传抑制M1神经元可显著降低心率、心功能和血压;利用Caspase3消融谷氨酸能神经元后显著降低心功能和血压,而不改变心率。
图2. 激活M1谷氨酸能神经元影响心功能和血压
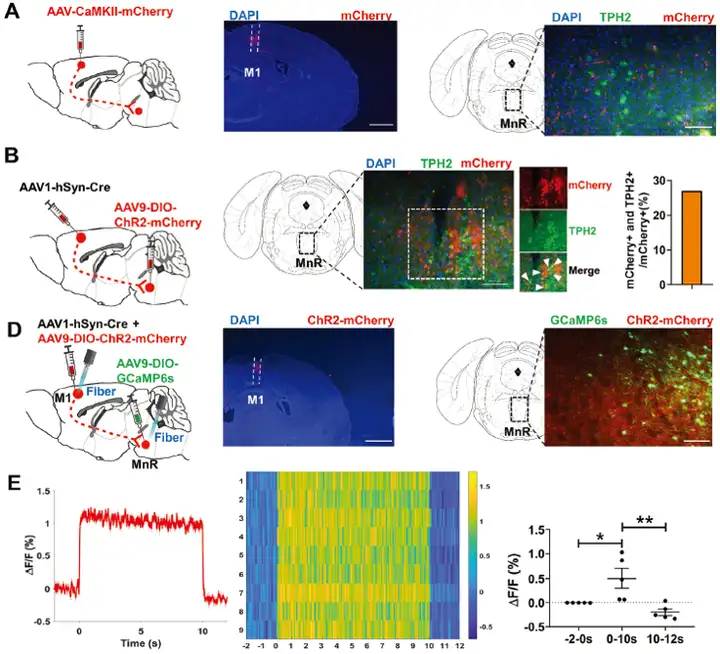
为了探讨初级运动皮层M1区谷氨酸能神经元影响正常小鼠心功能和血压的神经机制,探索M1投射的下游脑区,研究人员进一步利用神经示踪、光遗传学结合药理学和在体光纤记录等技术,发现M1谷氨酸能神经元向MnR强烈投射,且MnR中的色氨酸羟化酶2 (TPH2) 阳性神经元接近M1投射纤维,然后利用光遗传和钙成像相结合,证实了MnR神经元接收来自M1的直接输入。
图3. M1神经元直接投射到MnR区
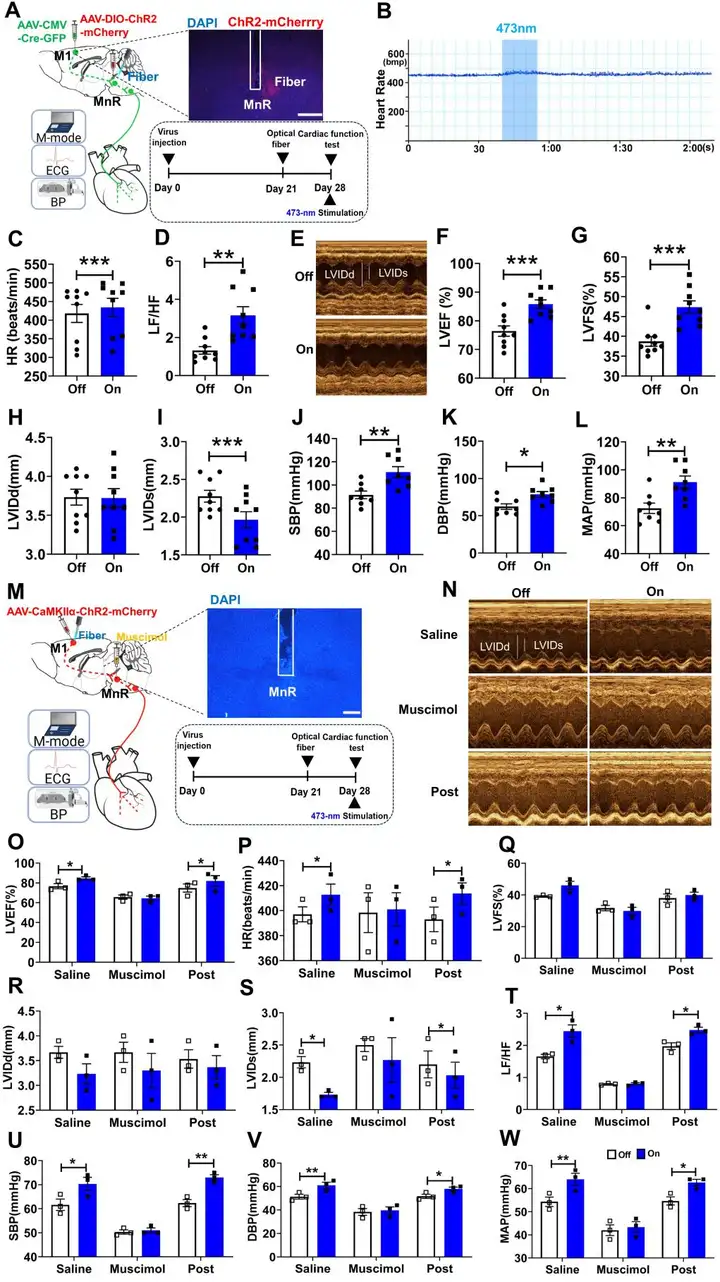
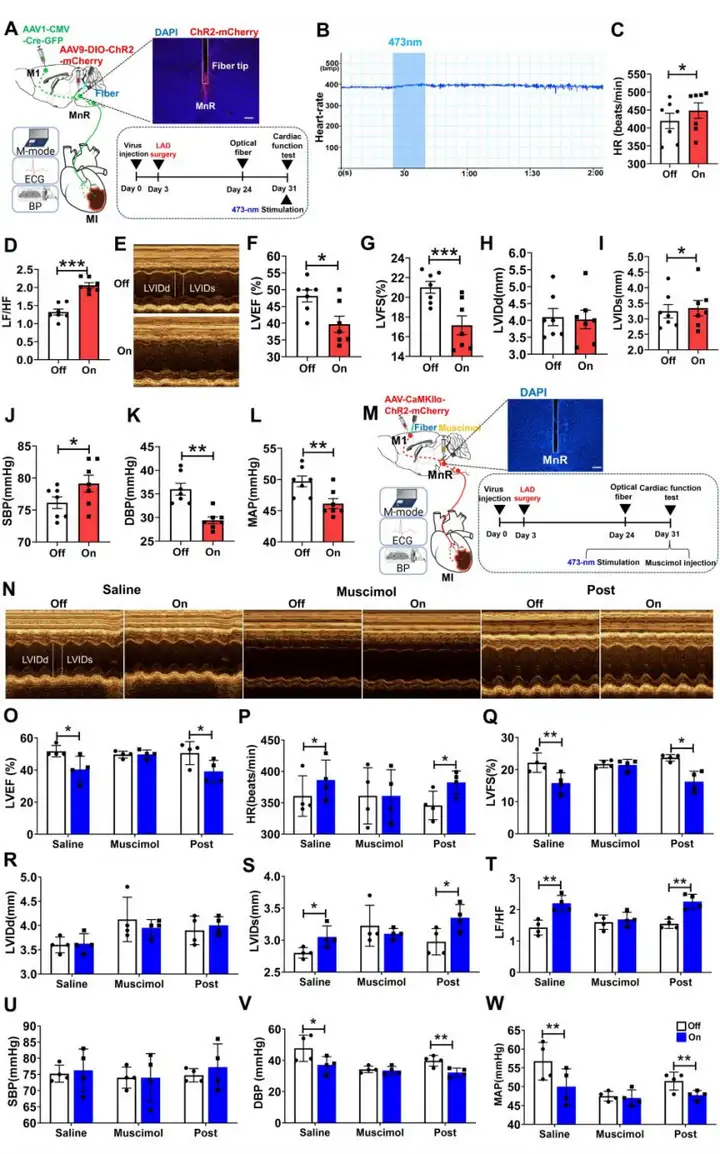
研究人员进一步通过光遗传激活M1突触后MnR神经元,发现小鼠心率显著增加、心脏功能增强、血压显著升高。同时仅光遗传激活M1谷氨酸能神经元就足以影响心脏功能、血压和自主神经活动的平衡,在MnR注射蝇蕈醇(muscimol)可抑制光遗传激活效应,表明MnR神经元对于M1引起心脏活动是必要的。
图4. 操控M1投射至MnR区神经元影响正常小鼠心功能
罹患心梗后心交感神经过度激活是诱发恶性心律失常和导致患者死亡的关键因素。因此,探索调控心梗后心功能的中枢靶区,对抑制心交感神经过度激活,改善心功能至关重要。研究人员进一步在心肌梗死(MI)状态下研究M1谷氨酸能神经元对心功能的影响,通过光遗传、化学遗传和Caspase3消融技术发现,激活心梗小鼠M1区谷氨酸能神经元进一步恶化心功能;抑制该神经元可改善心功能并影响血压,同时显著降低心脏交感神经兴奋。接着通过神经示踪,光遗传结合药理学等技术,发现M1-MnR通路在心梗小鼠心功能调控中发挥重要作用。在MnR区注射muscimol后,激活M1区谷氨酸能神经元引起的心梗小鼠心功能和血压的变化被抑制。
图5. 操控M1投射至MnR区神经元影响心肌梗死小鼠心功能
以上结果表明,操纵M1神经元活动通过MnR影响正常小鼠的心率、心功能和血压,抑制病理条件下小鼠M1神经元活动可显著改善心功能。
全文总结
在这篇研究中,研究人员利用病毒示踪、fMOST三维成像、钙成像和遗传学技术对小鼠大脑影响心脏活动的机制进行了探索,发现M1中特定兴奋性神经元群与小鼠心脏功能相关,激活这些神经元可增加心率、射血分数和血压,而抑制它们则会降低心功能和血压。发现中缝核(MnR)作为M1回路中的关键中继脑区之一,影响心功能。通过建立心肌梗死(MI)模型,发现病理状态下M1神经元通过MnR同样可调节心功能。这些结果证实了M1 L5神经元在心功能和血压调节中的重要性,为理解心血管调节的神经机制提供了新见解。
通讯作者简介
随着经济社会发展和人们生活方式的变化,心血管疾病已成为慢性非传染性疾病死因之首,并具有年轻化趋势。在心血管疾病临床研究和治疗方面已经取得长足发展,运动对心血管疾病的预防和康复作用也越来越受到关注,但其机制仍未完全阐明。田振军教授团队长期聚焦运动因子与心脏保护研究,通过对心梗后的运动干预方式、抑制氧化应激和炎症的重要运动因子筛选,以及远隔器官参与运动对心血管保护的机制研究,先后发现了卵泡抑素样蛋白1(FSTL1)[1]、心磷脂酰基转移酶(ALCAT1)、鸢尾素(Irisin)、肌肉特异性组蛋白甲基转移酶Smyd1、Apelin受体早期内源性配体(ELABELA)、成纤维细胞生长因子21(FGF21)以及miR126等运动因子在运动与缺血心脏保护中的作用,发表了系列成果,为推动运动与心血管疾病的预防和康复手段及方法筛选,提供了实验证据。联合团队先后主持国家自然科学基金9项,在SCI/CSSCI源刊发表研究论文200余篇,获陕西省科技进步奖和哲学社会科学优秀成果奖以及陕西省高等学校科技奖5项。
贺志雄,博士,副教授,硕士生导师,主要从事双亲行为的神经环路机制研究。在Advanced Science、eLife、Journal of Neuroscience、Psychoneuroendocrinology、Neurobiology of Learning and Memory、Behavioural Brain Research、Pharmacology Biochemistry and Behavior、Brain Research、Behavioural Processes共发表学术论文30余篇。现任中国动物学行为学分会青年委员,陕西省动物学会理事和陕西省生理学会青年理事。主持国家自然科学青年基金、陕西省自然科学青年基金、中国博士后面上项目,作为科研骨干参与科技部科技创新2030—“脑科学与类脑研究”重大项目(社会性行为的神经机制及其演化)等科学研究项目。
参考文献
[1]Xi Y, Hao M, Liang Q, Li Y, Gong DW, Tian Z. Dynamic resistance exercise increases skeletal muscle-derived FSTL1 inducing cardiac angiogenesis via DIP2A-Smad2/3 in rats following myocardial infarction. J Sport Health Sci. 2021 Sep;10(5):594-603.
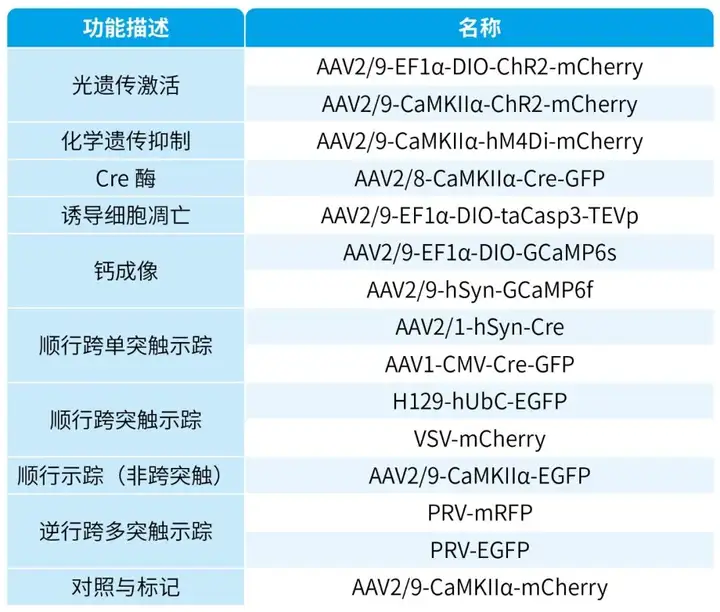
本文使用的病毒产品均来自枢密科技,列表如下:
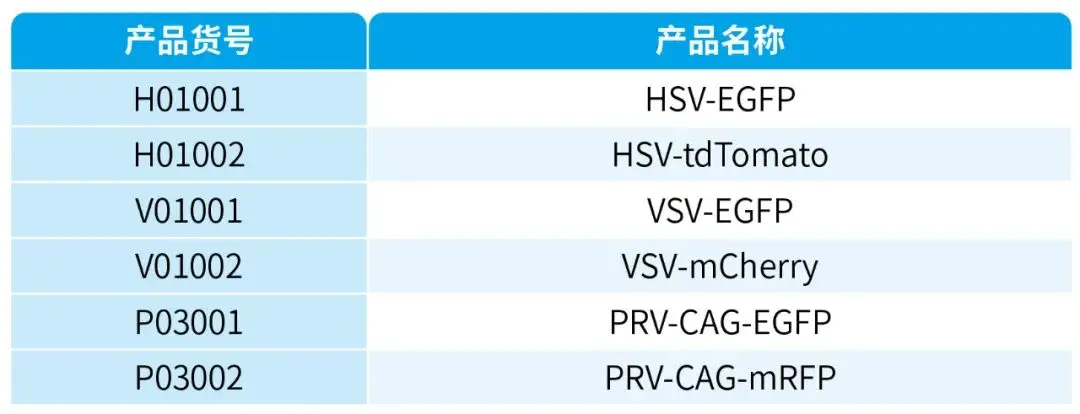
我司可提供顺行跨突触示踪单纯疱疹病毒HSV和水疱性口炎病毒VSV、13次方滴度1型-Cre/Flp的AAV病毒;逆行跨多突触示踪伪狂犬病毒PRV及病毒脑立体定位注射服务,部分相关产品列表如下:

了解产品及服务
请扫码或添加客服微信:BrainVTA2020

市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK