2026-04-23 阅读量:21
简介
大脑功能依赖神经元间精准的信息传递,解析特定神经元的输出连接、明确其信息投射靶点,是揭示神经环路机制的核心。科研界长期亟需一款工具:能从基因指定的起始神经元出发,严格沿着顺行方向(突触前→突触后)精准标记单突触连接的下游神经元。然而当前主流顺行示踪工具均存在短板:单纯疱疹病毒(HSV-1)与水疱性口炎病毒(VSV)经改造后虽能实现顺行跨单突触示踪,但存在神经毒性与逆行扩散泄漏现象;腺相关病毒1型(AAV1)、黄热病病毒(YFV)虽可顺行运输,却缺乏起始神经元的细胞类型特异性,还存在跨突触效率不稳定及潜在的逆行污染问题,难以满足现代神经环路研究的精准要求。2025年5月发表于Nature Methods(IF=36.1)的重磅研究“ATLAS: a rationally designed anterograde transsynaptic tracer”,开发出新型蛋白示踪工具ATLAS(anterograde transsynaptic label based on antibody-like sensors,基于抗体样传感器的顺行跨突触标记),实现从基因指定神经元出发的严格顺行、单突触、非毒性且活性依赖的跨神经元示踪,为神经环路解析提供了全新技术方案。

技术原理
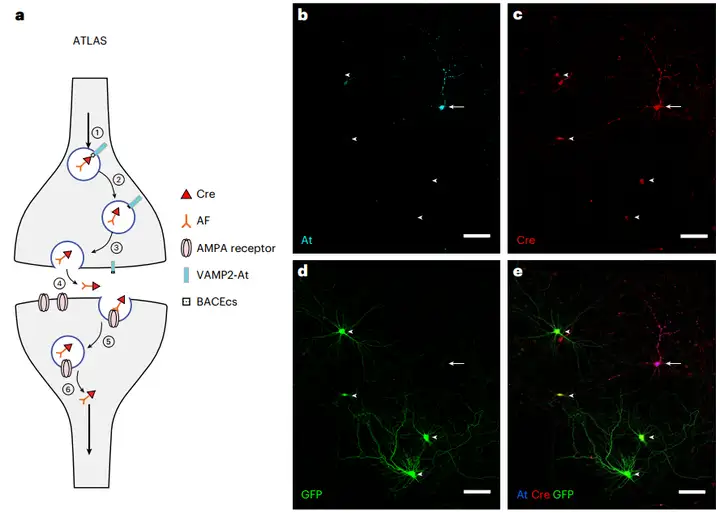
ATLAS的巧妙之处在于,它是一种理性设计的融合蛋白,由可独立替换的功能模块组成,其工作机制高度模仿了生理性的突触传递过程。
1、ATLAS核心模块化组件
VAMP2:突触前蛋白——突触小泡蛋白2,介导ATLAS靶向突触小泡。在优化版本ATLASsn中将VAMP2的胞质结构域替换为靶向突触结合蛋白1的纳米抗体(SYTnb)形成SYTnb-VAMP2Δ,从而消除全长VAMP2高表达带来的神经毒性;
At:ALFA-tag,一种高亲和力的小型合成抗体标签,用于可视化ATLAS蛋白在起始神经元的表达与分布;
BACEcs:β分泌酶(BACE1)特异性切割位点,切割后释放效应片段(AF-重组酶);
AF(AMPA.FingR):mRNA展示技术筛选的抗体样纤连蛋白,特异性结合突触后膜GluA1(AMPA型离子型谷氨酸受体关键亚基)N端胞外域;
重组酶(Cre/Flp):在核定位信号引导下入核,触发重组酶依赖的报告基因表达,实现对单突触下游细胞的荧光标记。
2、ATLAS顺行跨单突触步骤
1)突触小泡靶向:ATLAS经VAMP2(或优化版SYTnb-VAMP2Δ)定位至起始(突触前)神经元的突触小泡;
2)酶切释放:BACE1切割BACEcs,释放AF-重组酶效应片段;
3)突触间隙释放:突触小泡与突触前膜融合,效应片段释放至突触间隙;
4)突触后特异性结合:AF精准结合突触后膜GluA1 N端,将效应片段牢牢固定在突触后膜表面;
5)内吞入胞:AF-重组酶经网格蛋白介导的内吞作用进入突触后神经元;
6)核内报告激活:重组酶在核定位信号引导下入核,触发重组酶依赖(loxP/frt系统介导)的报告基因(如GFP、mCherry)表达,标记突触后细胞。
图1. ATLAS的跨突触运输及体外测试的示意图
(Rivera, Jacqueline F et al., Nature methods, 2025)
ATLAS系统应用要点
1.病毒搭配方案:AAV-ATLASsnCre-WPRE-pA与AAV-DIO-mCherry/EGFP搭配使用,具体为上游脑区注射ATLASsnCre病毒,下游靶区注射DIO-mCherry/EGFP病毒。
2.效率优化策略:实验结果表明,当上游脑区混合注射AAV-ATLASsnCre-WPRE-PA与补充外源性BACE的AAV-hSyn-HA-BACE-WPRE-PA(混合比例为BACE:ATLASsnCre=5:1),同时下游靶区注射DIO-mCherry/EGFP时,可显著提升跨单突触标记效率。
3.示踪层级限制:ATLAS系统仅能实现顺行跨单突触示踪,无法用于顺行跨多突触的研究。
4.方向特异性:ATLAS系统几乎无逆行跨突触标记,其跨单突触示踪具有严格的顺行性。
5.适用细胞类型:标记下游GluA1阳性细胞。
6.活动依赖性特征:当上游注射区域的细胞被激活时,下游靶区的DIO-mCherry/EGFP荧光强度会显著增加。
应用案例
1、精准解析mPFC-Str环路
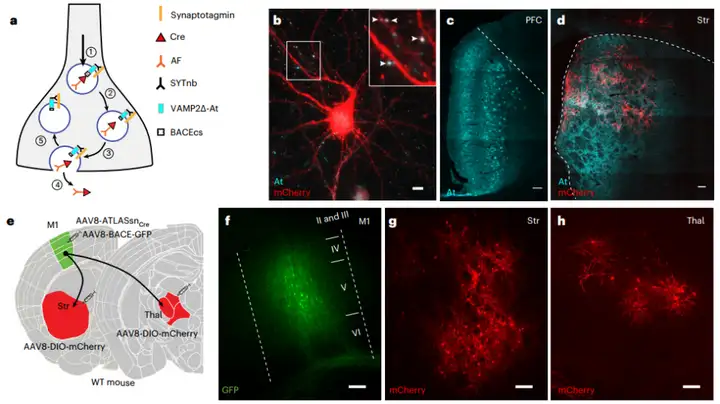
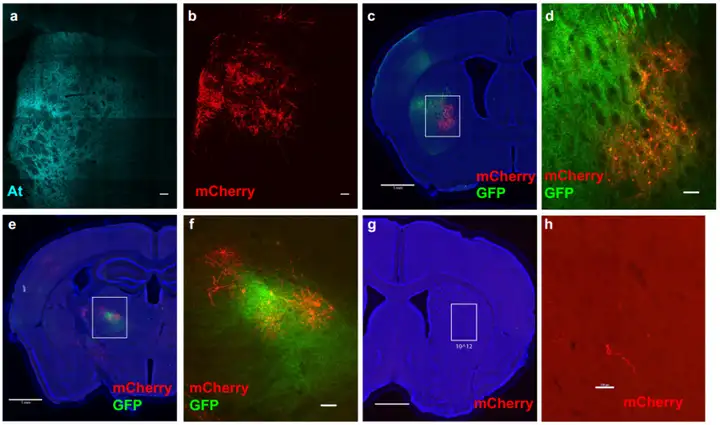
研究者将ATLASsn(AAV8-ATLASsnCre)与BACE辅助病毒AAV8-BACE-HA共注射至小鼠内侧前额叶皮层(mPFC),在纹状体(Str)注射报告病毒AAV8-DIO-mCherry。2周后观察结果显示,mPFC的起始神经元被成功标记(At免疫组化染色),且Str中出现了大量红色mCherry标记的突触后神经元;突触后mCherry标记的背侧区域与来自mPFC的突触前末梢At标记几乎完全共定位,证实了ATLASsn的高效顺行跨突触能力(图2)。
2、实现“一到多”多靶点同步示踪(M1-Str/Thal)
研究者将AAV8-ATLASsnCre与AAV8-BACE-GFP共注射至小鼠初级运动皮层(M1),同时在Str和丘脑(Thal)注射报告病毒AAV8-DIO-mCherry,2周后可同时观测到M1起始神经元标记(GFP),以及Str、Thal内特异性的下游神经元荧光信号(mCherry),两种荧光信号高度重叠,标记结果与已知解剖环路完全吻合。仅注射报告病毒的对照组无明显背景信号,证明ATLASsn可高效完成单脑区起始→多下游脑区的顺行跨突触示踪,特异性强、背景极低,适配复杂环路的多靶点解析需求(图2)。
图2. ATLASsn的跨突触示踪
(Rivera, Jacqueline F et al., Nature methods, 2025)
3、实现从基因指定神经元出发的严格顺行
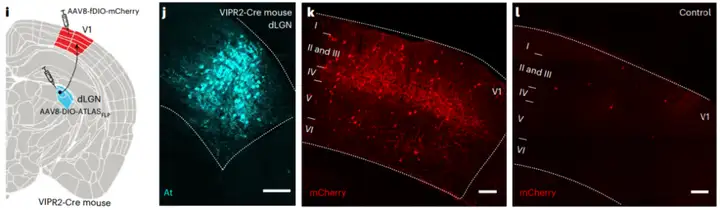
为实现基因定义示踪,研究者构建了Cre依赖性表达的AAV8-DIO-ATLASFLP(携带Flp重组酶),进一步在VIPR2-Cre转基因鼠(仅背外侧膝状核(dLGN)神经元中表达Cre)的dLGN注射AAV8-DIO-ATLASFLP,借助Cre依赖特性实现仅dLGN神经元表达ATLAS,从而实现了严格的起点特异性;在其投射脑区初级视皮层(V1)注射Flp依赖的AAV8-fDIO-mCherry。结果在dLGN中特异性检测到At染色,并成功在V1的IV层(主要投射层)及II/III和V层观察到符合解剖学特征的mCherry标记。证明ATLAS能有效介导从基因定义神经元出发的顺行跨突触示踪(图3)。
图3. 在VIPR2-Cre小鼠中实现从基因指定神经元dLGN到V1的严格顺行跨突触示踪
(Rivera, Jacqueline F et al., Nature methods, 2025)
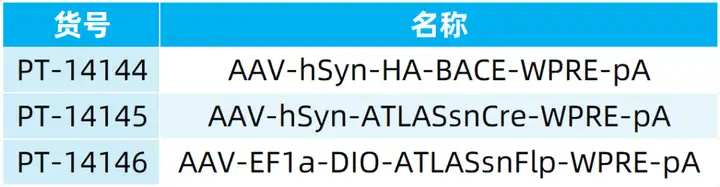
我司可提供ATLAS顺行跨单级突触病毒工具,列表如下:
扫码添加客服

更多产品及详情欢迎咨询!

市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK