2024-06-17 阅读量:2862
重组腺相关病毒(rAAV)是FDA批准的体内基因治疗载体,在心血管基础和转化研究中被广泛应用。AAV血清型9(AAV9)具有高度心脏亲和性。AAV9搭载心脏肌钙蛋白T(Tnnt2,又称cTnT,特异性启动子)是最常用的心肌特异性递送基因的载体。但是,AAV9-Tnnt2载体在心脏外的其他器官,存在基因表达泄漏。因此,对该载体进行更严格的生物分布评估,并进行针对性的优化,对于心脏研究和基因治疗具有重要意义。
2024年5月28日,北京大学基础医学院、北京大学心血管研究所、血管稳态与重构全国重点实验室郭宇轩研究员团队在Circulation杂志上发表题为“MicroRNA-122-mediated liver detargeting enhances the tissue specificity of cardiac genome editing”的论文[1]。该研究基于Cre-LoxP、CRISPR/Cas9等超敏DNA记录技术,发现AAV9-Tnnt2载体在肝脏中广泛泄漏表达。利用microRNA-122在肝脏组织中高度特异性表达的特点,该团队在AAV9-Tnnt2转基因的3’UTR引入miR122的靶序列(miR122TS),大幅度降低了AAV9-Tnnt2在肝脏组织中的表达泄漏,提高了其心脏特异性。利用这种优化的载体,该团队通过静脉注射AAV,成功实现心肌特异性的CaMKIIδ单碱基编辑失活,显著缓解心梗小鼠模型的疾病表型,并且不造成额外肝损伤。因此,本研究构建了更加严格的心脏特异性AAV体内基因递送载体,实现了AAV在心脏研究中的技术升级。
结果
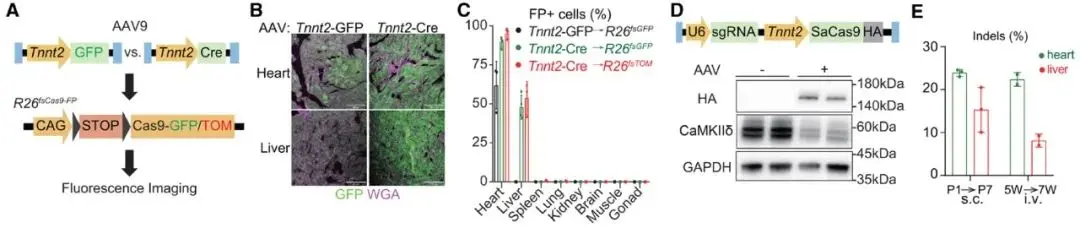
为了评估AAV9-Tnnt2组织特异性,我们首先构建AAV9-Tnnt2-GFP载体,并以5×1010 vg/g(boby weight)的剂量注射到出生后第1天(P1)小鼠体内,并在P14处用共聚焦显微镜评估GFP信号(Fig A-C)。GFP信号仅在心脏中检测到,而在肝脏、脾脏、肺、肾、脑、脾脏或性腺中检测不到(Fig B和C)。相反,当我们在R26fsCas9-GFP小鼠中注射相同剂量的AAV9-Tnnt2-Cre载体激活Cre依赖的GFP报告基因时,在约50%的肝细胞中观察到GFP信号(Fig B-C)。在tdTomato报告基因小鼠(R26fsCas9-tdTomato,Fig C)中也观察到基于AAV9-cTnT-Cre的肝脏激活。因此,AAV9-Tnnt2系统在肝脏中表现出低水平的广泛基因表达渗漏。综上所述,虽然AAV9-Tnnt2-GFP由于灵敏度的限制,在肝脏中难以检测到信号,但是在Cre-Loxp这种高灵敏度的检测手段下,AAV9-Tnnt2载体的肝脏泄露变得尤为明显。
与Cre-LoxP类似,CRISPR/Cas9基因编辑技术也是对低水平或瞬时基因表达高度灵敏的DNA记录技术。因此,我们测试了AAV9-Tnnt2载体是否会在肝脏中引起异位基因编辑。我们针对公认的心脏病治疗靶点Camk2d基因设计sgRNA,并构建同时表达Cas9和sgRNA的载体AAV9-U6-sgRNA-Tnnt2-SaCas9-HA(Fig D),在P1处皮下注射该载体,在P7处在心脏中验证CaMKIIδ蛋白(钙/钙调素依赖性蛋白激酶IIδ)缺失(Fig D)。结果表明,该载体特异性地敲除心脏组织中的CaMKIIδ蛋白。sgRNA靶向位点的二代测序显示,肝脏中有>10%的DNA插入和缺失(indels)(Fig E),达到了心脏组织中indels产生率的一半。而当将该载体静脉注射到5周龄的动物体内时,获得了类似的结果(Fig E)。因此,AAV9-Tnnt2介导的基因编辑泄漏与年龄或注射方法无关。
Fig 1:AAV9-Tnnt2介导的基因编辑泄漏与年龄或注射方法无关。
为了降低AAV9-Tnnt2在肝脏中的表达泄漏,作者选择了microRNA-122(miR122),它是肝脏中特异性表达,在microRNA中丰度最高,且介导基因沉默的microRNA。将miR122干扰靶序列(miR122TS)结合到3’UTR,可以抑制AAV在肝脏的转录[2]。作者进行动物学验证,将miR122TS掺入AAV9-Tnnt2-Cre中,观察到R26fsCas9-tdTomato小鼠tdTomato阳性肝细胞减少了90%以上,而心脏Cre-LoxP的激活不受影响(Fig F)。肝脏mRNA测序和小RNA测序各检测到仅两个miR122TS掺入的差异表达基因(Fig G)。尽管RNA测序进一步证实了miR122TS下调Cre的表达,但内源性miR122水平不受影响(图H)。小鼠和人类的miR122TS序列相同。作者用AAV9-Tnnt2-Cre处理人肝细胞系Huh7,也观察到miR122TS显著降低了Cre表达。
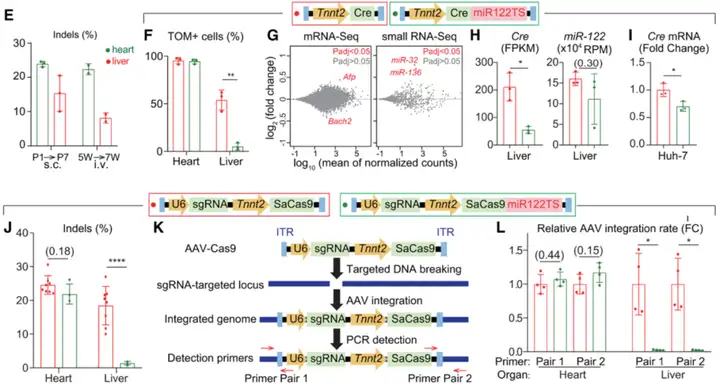
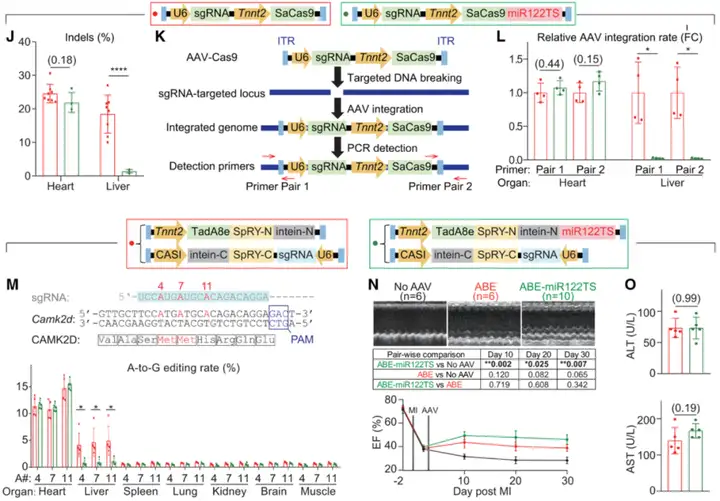
接下来,我们发现将miR122TS整合到AAV9-Tnnt2-SaCas9载体中,结果显示也大大减少了肝脏基因编辑的泄漏,而不改变心脏基因编辑(Fig J)。已知CRISPR/Cas9触发的DNA双链断裂会导致AAV整合到sgRNA靶向位点[4](Fig K)。使用靶向AAV和宿主基因组DNA边界的引物进行qPCR检测表明,miR122TS可以避免这种异位的AAV整合肝脏(Fig L)。
AAV9-Tnnt2系统最近被用于递送腺嘌呤碱基编辑器(ABEs)来消融心脏中的CaMKIIδ氧化位点,作为缺血性心脏病的潜在治疗方法[3]。我们发现AAV9-Tnnt2-ABE系统在系统给药时也出现肝脏渗漏,这可以通过加入miR122TS来解决(Fig M)。我们在小鼠中手术造成心肌梗死,并在心肌梗死后3天静脉注射ABE载体。超声心动图证实,ABE介导的Camk2d编辑是缓解心肌梗死的有效途径。miR122TS没有影响这种治疗效果(Fig N),也没有引起肝损伤生物标志物的升高,包括丙氨酸转氨酶和天冬氨酸转氨酶(Fig O),这证明了新的AAV9-Tnnt2-miR122TS载体是心脏基因治疗的有效载体。
结论
综上所述,本研究揭示了常用的AAV9-Tnnt2基因传递系统在肝脏中存在广泛的转基因泄漏的现象。这种现象通常不影响该载体在心肌细胞中特异性地过表达基因,但是在Cre-LoxP、CRISPR/Cas9和ABE等对低表达基因灵敏度极高的应用场景中会造成严重的肝脏泄漏情况。幸运的是,这个问题可以通过将miR122TS添加到重组AAV转基因的3’UTR来解决,从而实现心肌细胞特异性的体内基因编辑。由于内源性miR122的丰度和肝脏中Tnnt2驱动的miR122TS的低水平表达,miR122TS不太可能干扰内源性miR122途径。miR122的靶序列在小鼠和人类中是相同的,因此AAV9-Tnnt2-miR122TS系统可以潜在地应用于转化和临床研究。
通讯作者介绍:
郭宇轩,研究员,博士生导师。北京大学心血管研究所PI,分子心血管学教育部重点实验室PI。主要研究方向:1.心肌发育与病理生理;2.基因编辑与基因治疗;3.干细胞与类器官技术。
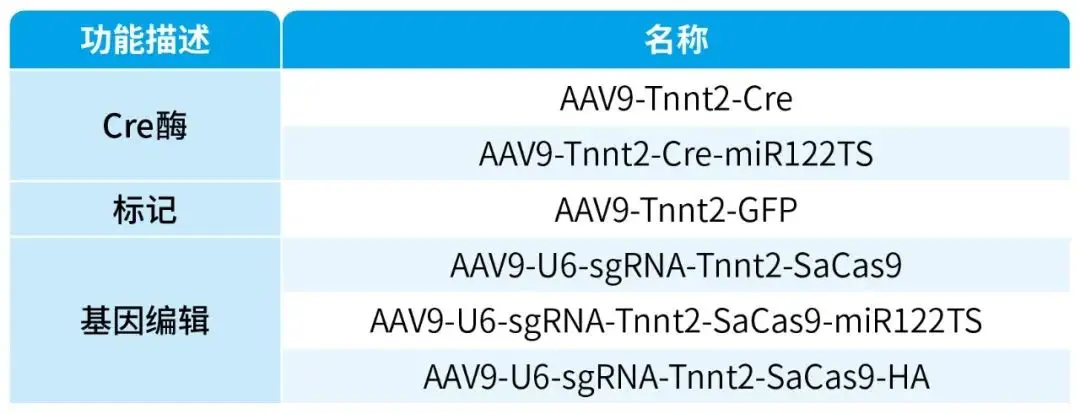
本文使用的病毒产品,列表如下:

了解产品及服务
请扫码或添加客服微信:BrainVTA2020

市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK