2024-02-04 阅读量:1124
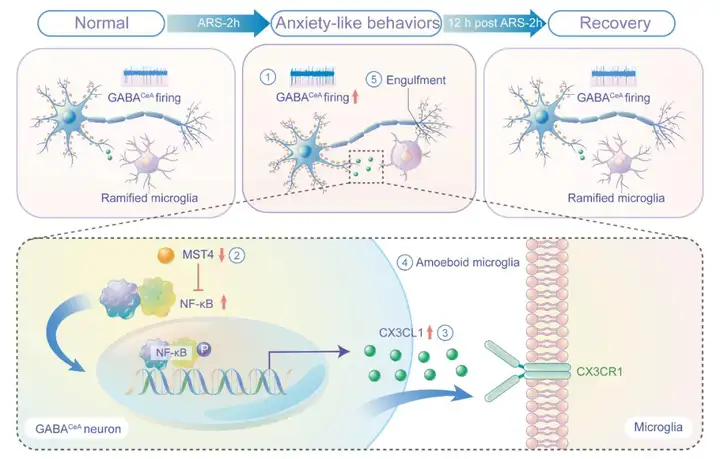
急性压力引起的焦虑可能是一种进化适应,用于对需要密切关注的刺激保持高度警惕和持续关注,或避免反复暴露在危险条件下。众所周知,急性焦虑可以随着压力刺激的消除而逐渐消失。然而,在这一动态消退过程中,个体如何应对急性压力并驱动焦虑消退的机制仍不清楚。
2024年1月10日,中国科学技术大学张智/曹鹏/晋艳教授团队在Nature Communications上发表了名为“Microglia govern the extinction of acute stress-induced anxiety-like behaviors in male mice”的研究论文。该研究综合运用了在体多通道记录、三维重构技术和化学遗传学等,发现急性束缚应激导致小鼠中央杏仁核CeA中GABACeA能神经元的活性增加,导致12 h内的焦虑样行为;同时,通过MST4-NF-κB-CX3CL1信号增加GABACeA神经元CX3CL1分泌,从而激活CeA中的小胶质细胞。活化的小胶质细胞反过来通过吞噬GABACeA神经元树突棘来抑制其活性,最终导致由束缚应激诱导的焦虑样行为的消失。中国科学技术大学生医部博士后陈丹阳、博士生娄倩倩和已毕业博士生宋相杰为本文的共同第一作者。中国科学技术大学生医部张智教授、曹鹏博士后和晋艳副教授为本文的共同通讯作者。本研究得到科技部、国家自然科学基金、省科技重大专项计划、安徽省自然科学基金、博新计划等项目的资助,以及中国科学技术大学生命科学核心设施中心的帮助。
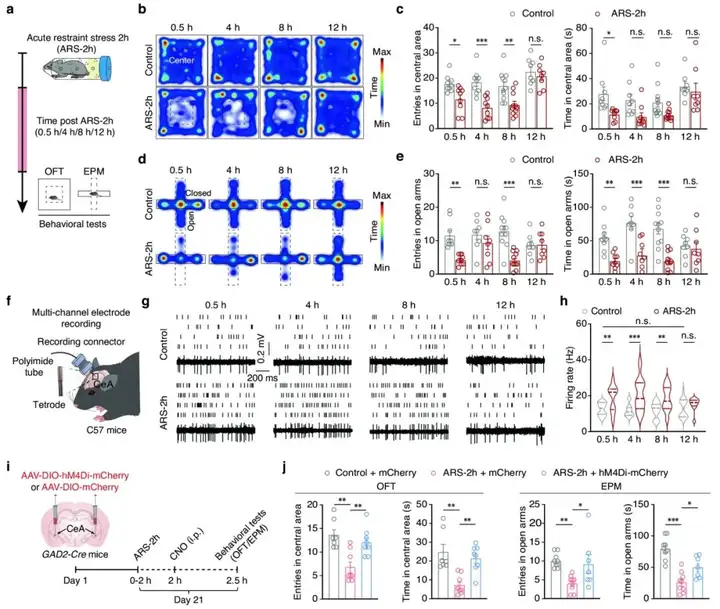
急性束缚2小时(ARS-2h)是常用的小鼠焦虑样行为的模型。ARS-2h小鼠在应激后0.5 h、4 h和8 h,小鼠表现出焦虑样行为,而在应激后12 h消失。CeA在焦虑状态的产生中起关键作用。然后,作者通过在体多通道记录发现小鼠在应激后0.5 h/4 h/8 h,GABACeA神经元活性增加,在应激后12 h恢复到与对照组相当的水平,与行为测试的结果很好的吻合。化学遗传学抑制GABACeA神经元缓解了应激后小鼠的焦虑样行为。这些结果表明,应激可增加小鼠GABACeA神经元活性,并诱导焦虑样行为,而这种神经元活性的降低伴随着焦虑样行为的消失。
图1. GABACeA神经元介导急性束缚应激诱导的焦虑样行为
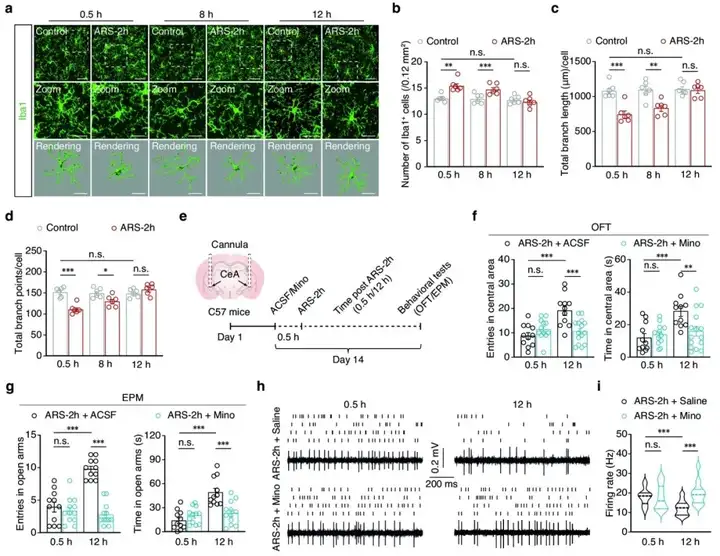
ARS-2h小鼠在应激后0.5 h和8 h,CeA中的小胶质细胞活化,在应激后12 h被逆转。通过颅内注射小胶质细胞抑制剂米诺环素(Minocycline,Mino),作者发现在应激后12 h小鼠焦虑样行为仍然存在,而且神经元活性并未恢复正常。这些结果表明,抑制小胶质细胞活化可阻断应激诱导的GABACeA神经元过度活跃的恢复和焦虑样行为的消失。
图2. 焦虑样行为的消失依赖于活化的小胶质细胞
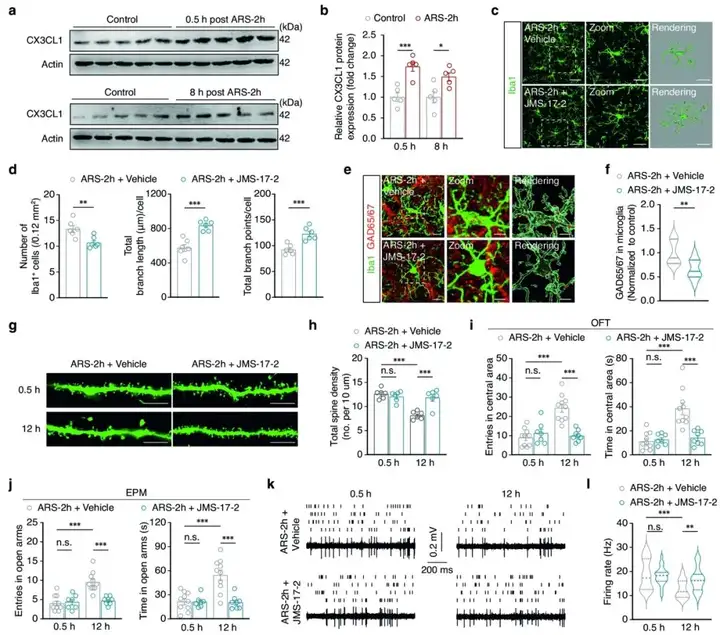
为了研究焦虑样行为消失期间小胶质细胞对应激的敏感性与GABACeA神经元活性降低之间的潜在关系,作者在ARS-2h模型小鼠中检测了GABACeA神经棘的重塑。模型小鼠中GABACeA神经元树突棘的密度在应激后0.5 h和8 h增加,而在应激后12 h恢复到对照水平。为了研究GABACeA神经元树突棘与小胶质突起之间的相互作用,作者检测了ARS-2h小鼠小胶质细胞的吞噬功能。实验证明应激后活化的小胶质细胞对GABACeA神经元的树突棘发挥了修剪作用。这些结果表明,激活的小胶质细胞可以通过明显的负反馈机制抑制GABACeA神经元的活性,促进后期焦虑样行为的恢复。
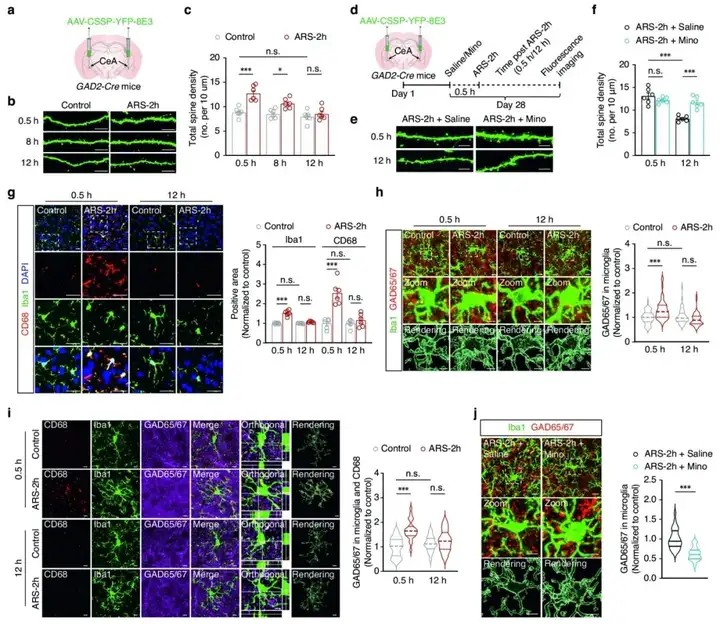
图3. 小胶质细胞通过吞噬GABACeA树突棘来消除焦虑样行为
为了进一步探索急性应激后GABACeA神经元过度活跃诱导小胶质细胞活化的潜在分子机制,作者检测发现ARS-2h小鼠中CX3CL1在0.5 h和8 h显著高于对照小鼠。此外,作者发现CX3CR1拮抗剂JMS-17-2预处理的ARS-2h小鼠CeA中,小胶质细胞的吞噬能力显著降低,而且在应激后12 h神经元的树突棘密度没有恢复正常。进一步实验发现,JMS-17-2阻碍了应激后焦虑样行为的恢复。这些结果表明,应激诱导后12 h内,趋化因子CX3CL1表达升高可活化小胶质细胞,并促进其对GABACeA神经元树突棘的吞噬,从而降低GABACeA神经元活性,促进模型小鼠焦虑样行为的消失。
图4. 阻断CeA中的CX3CL1-CX3CR1信号防止急性应激后焦虑样行为的消失
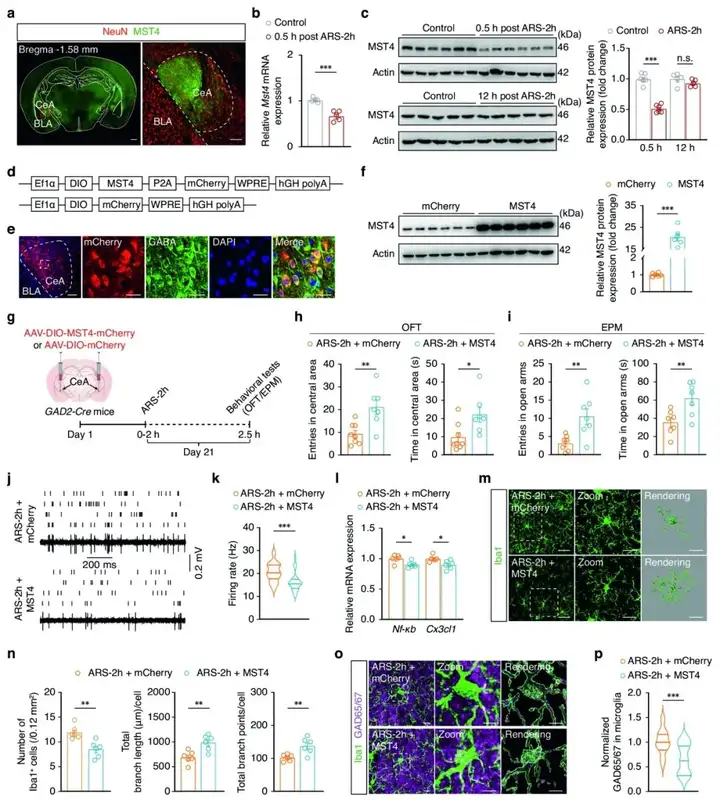
鉴于上述证据支持ARS诱导的NF-κB-CX3CL1信号上调在CeA中的作用,作者接下来研究了ARS中启动这一过程的潜在机制。作者发现在应激后0.5 h,CeA中抑炎因子MST4的mRNA和蛋白质水平均显著降低,并在ARS-2h后12 h恢复到对照组的水平。作者发现在CeA中过表达MST4可逆转小鼠焦虑样行为,并且过表达MST4的应激小鼠,小胶质细胞的吞噬能力显著降低。这些结果说明过表达MST4逆转应激后小胶质细胞对神经元树突棘的吞噬。
图5. GABACeA神经元中MST4的过度表达缓解了急性应激诱导的焦虑样行为
因此,本项研究表明,小胶质细胞驱动的负反馈机制对于保护大脑免受健康或疾病状态下神经元的过度激活很重要。急性应激早期的小胶质细胞激活可以在调节神经元活动中发挥保护作用,这与以往研究中的慢性应激的促伤害作用不同。
通讯作者介绍:
张智,教授,博士生导师,国家高层次海外引进人才(2012年),国家杰出青年基金获得者(2020年),国家重点基础研究发展计划(973计划)首席科学家(2014年),科技创新2030(中国脑计划)首席科学家(2021年)。2012年11月起任中国科学技术大学生命科学学院教授,主要从事疼痛与情绪以及不同感觉系统相互作用的分子和神经环路研究,致力于临床的转化和应用。原创性研究成果以最后通讯作者发表于Science、Nature Neuroscience(3 篇)、Nature Metabolism(2 篇)和Neuron等,入选中国神经科学重大进展(2 次)和Cell 出版社中国年度最佳论文。
曹鹏,中国科学技术大学生命科学与医学部博士后,合作导师为张智教授,主要研究方向为疼痛与情绪的神经机制。以第一作者在Neuron、Cell Reports等期刊发表文章,成果入选Cell出版社年度中国最佳论文,中国神经科学重大进展,ESI高被引论文。
晋艳,中国科学技术大学生命科学与医学部,副教授,中国科学院青促会会员,安徽省杰出青年基金获得者,入选仲英青年学者奖励计划,安徽省神经科学学会秘书长。长期从事疼痛与情绪相互作用的神经机制研究,发表SCI研究论文26篇,其中,以第一/通讯作者(含共同)发表 Nature Neuroscience、Neuron、The Journal of Clinical Investigation、National Science Review和Cell Reports等研究论文 10 余篇,多篇论文分别入选中国神经科学重大进展、Cell出版社中国最佳论文、iNature中国生命科学20大进展和Faculty1000推荐阅读。
本文使用的病毒产品均来自枢密科技,列表如下:


了解产品及服务
请扫码或添加客服微信:BrainVTA2020

市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK