2021-11-18 阅读量:2195
编者按
光遗传学技术是一种具有精确靶向性,高时空分辨率,毫秒级快速响应等优点的新兴神经调控手段,非常适合运用到神经系统中进行闭环控制。闭环光遗传学可以对神经适应性、可塑性和神经活性变化等生理问题进行深入研究,闭环控制可以通过检测神经元和神经环路的波动,以自发的实现对神经活性和动物行为的实时控制。然而迄今为止,大多数已发表的动物行为学相关的光遗传学文章仍是以开环控制系统为主,通过直接输入相关的参数,直接观察结果的响应。例如,以一定频率的光脉冲刺激腹侧背盖区(VTA)的多巴胺神经元,激活多巴胺神经元的活性,引起社会接触行为的变化。这种开环模式并不需要对结果进行量化和反馈。小编在这里给大家推荐Grosenick L等发表在《Neuron》的综述,作者在闭环光遗传学中利用神经活动或者行为的同步性,在闭环反馈环路中通过检测指标引导刺激,实时决定如何以及何时进行光遗传学刺激。例如,使用动态电压钳检测到锥体神经元锋放电增加,随后通过光遗传学刺激激活抑制性PV阳性的中间神经元,从而抑制锥体神经元的放电,完成一个反馈抑制的环路。光遗传学闭环调控(同时观察神经元活性的变化并实时进行光遗传学干预)是研究神经环路与相关表型因果关系的有利武器,特别是研究环路干预在单位时间尺度对生理功能和行为学效应的影响。本综述重点介绍了光遗传学闭环控制系统的技术和理论基础以及最新进展。

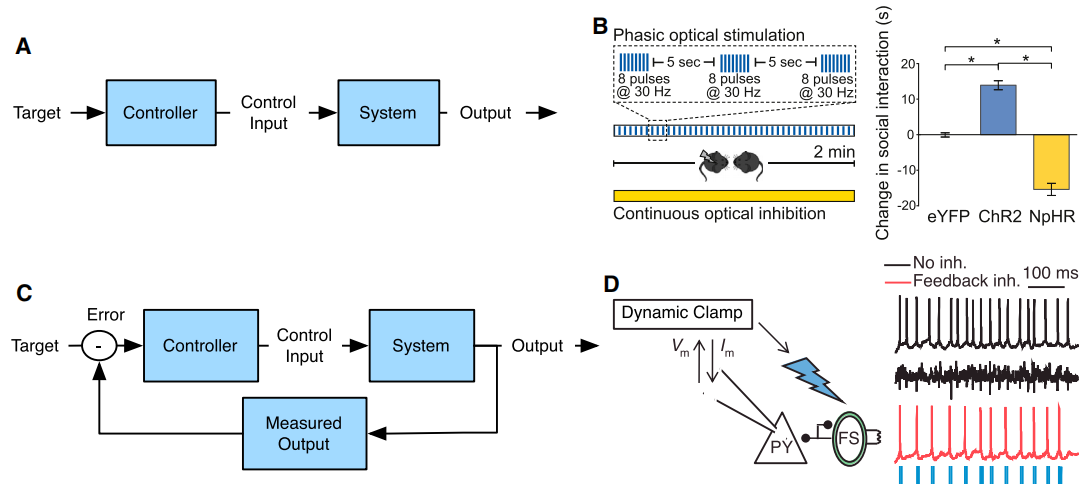
图1.开环控制系统和闭环控制系统
一、闭合光遗传学的电学与光学元件
数字化电生理测量为闭环光遗传学检测提供了量化标准,而光刺激作为闭环系统的调节手段,可精确的干预检测目标的动态变化。在活体水平方面,光学电极是用于集成电记录和光反馈的最简单和使用最广泛的元件,并且已经经历了好几次设计改进,研发出集成μLED的光学电极。在系统工程中,这些设备被分类为单输入单输出(single-input single-output,SISO)系统,即允许对系统进行单一的电测量和单一的光学控制来调控系统。此外,一些技术将电测量和光反馈电极整合到了一起,在记录的同时保持光的输入,称为光电极,光电极、16通道记录的光电极和微阵列的锥形光电极共同被称为单输入多输出(single-input multiple-output,SIMO)系统。类似的,通过电记录和光遗传学调控,在多个脑区进行记录和刺激的系统,被称为多输入多输出(multiple-input multiple-output,MIMO)系统,包括集成光纤和二极管的多通道硅电极,结合多个电极的光纤束和玻璃光阵列电极等。
除了光输入和电输出的元件外,闭环光遗传学还有一些其他的元件,比如高度灵活的、仿生的全聚合物光纤,该光纤可避免使用过程中出现光纤的损耗;超薄的、机械兼容的、深脑兼容的电极,该电极可在行为过程中同时进行光刺激和电记录;柔性聚合物技术开发可以同时进行光刺激、神经记录和药物输送的光纤探针等。
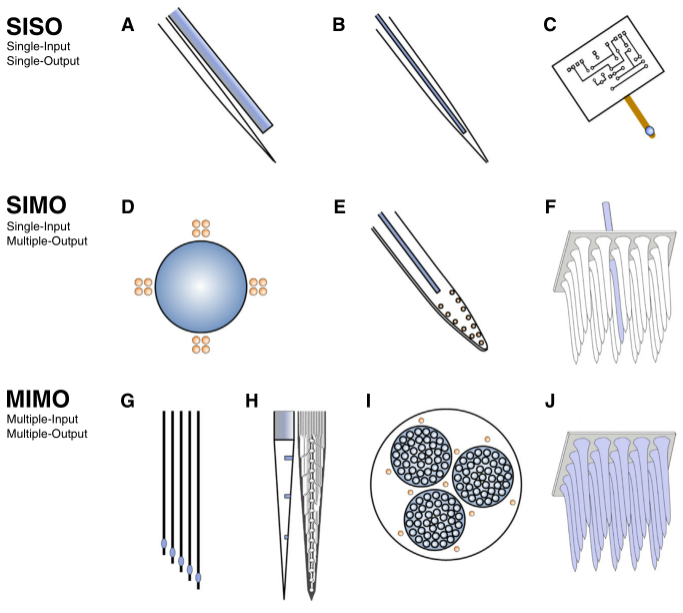
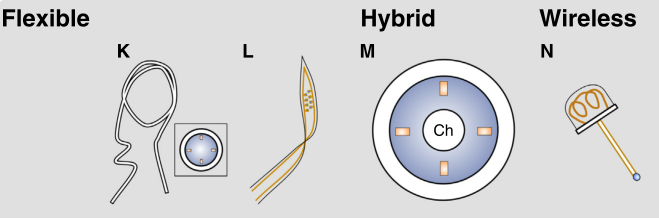
图2.闭合光遗传学系统相关元件
二、闭环光遗传学的光刺激器和光传感器
可兼容神经元活性光学传感器的光遗传学工具,对于闭环光遗传学的使用至关重要。所谓兼容,指的是神经元活性光学传感器和启动光遗传学刺激器所需的激发波长之间基本没有光谱重叠。但由于大多数光遗传学的视蛋白具有广泛的激发光谱,因此应用时需要对光激发强度进行限制,或者选择激发波长距离较远的视蛋白和传感器进行组合。
在单光子情况下,红移的新的遗传可编码Ca2+指示剂(GECI)与蓝光激活的控制工具如ChR2及其变体可兼容使用在闭环光遗传学系统中。类似的,红光激发的C1V1T/T、光抑制性蛋白eNpHR3.0与蓝光激活的传感器GECI结合也有广阔的前景。在双光子情况下,GCaMP变体可用于短波长驱动进行双光子成像,而C1V1视蛋白变体可用于长波长驱动的光刺激器。
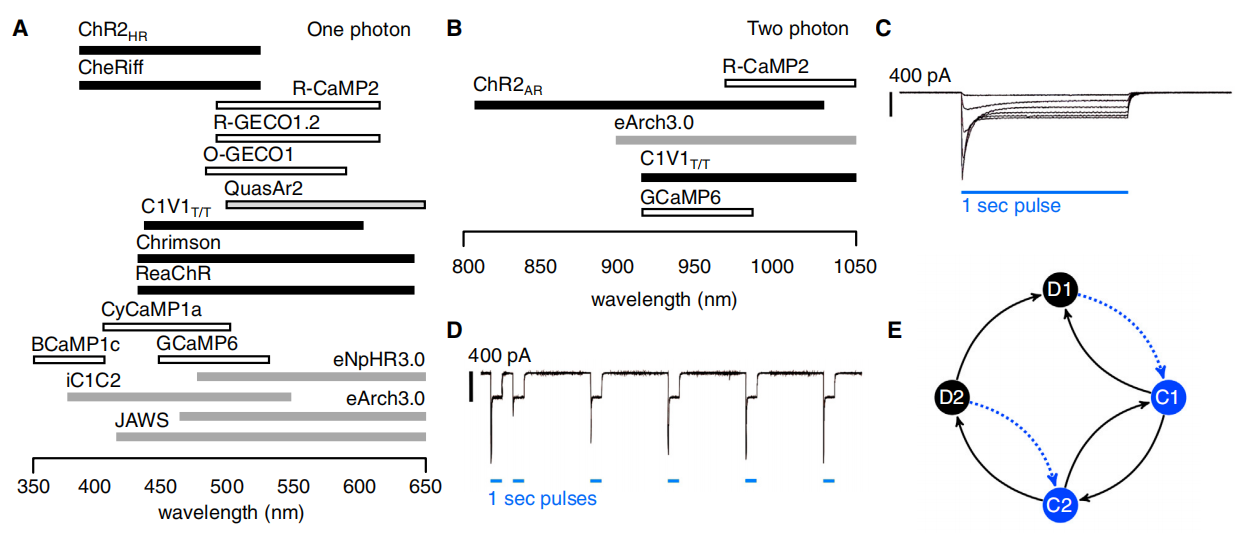
图3.闭环光遗传学的光刺激器和光传感器
三、闭环光遗传学的神经元靶向策略
特定类型的神经元编码特定的功能,但在实验上分离不同的神经元群并不容易,因为不同的神经群,特别是兴奋性神经元,通常属于相似的遗传类别。鉴于这些神经群在时间上是动态活跃的,并随着动物状态的变化而变化,因此实时动态监测特定的神经元群,并在时间尺度上精准的特异性干预对于神经元功能研究至关重要。
通过使用基于活性调节的c-fos启动子元件的诱导系统,可对活性神经元进行特异性标记,并使用光遗传学研究特异功能集合的活性神经元群体。通过这种方法,可在恐惧记忆编码过程中,通过多西环素来选择性地驱动活性神经元表达光遗传学蛋白,然后用光遗传学激活或抑制活性神经元,进而诱导出不同的恐惧行为反应。
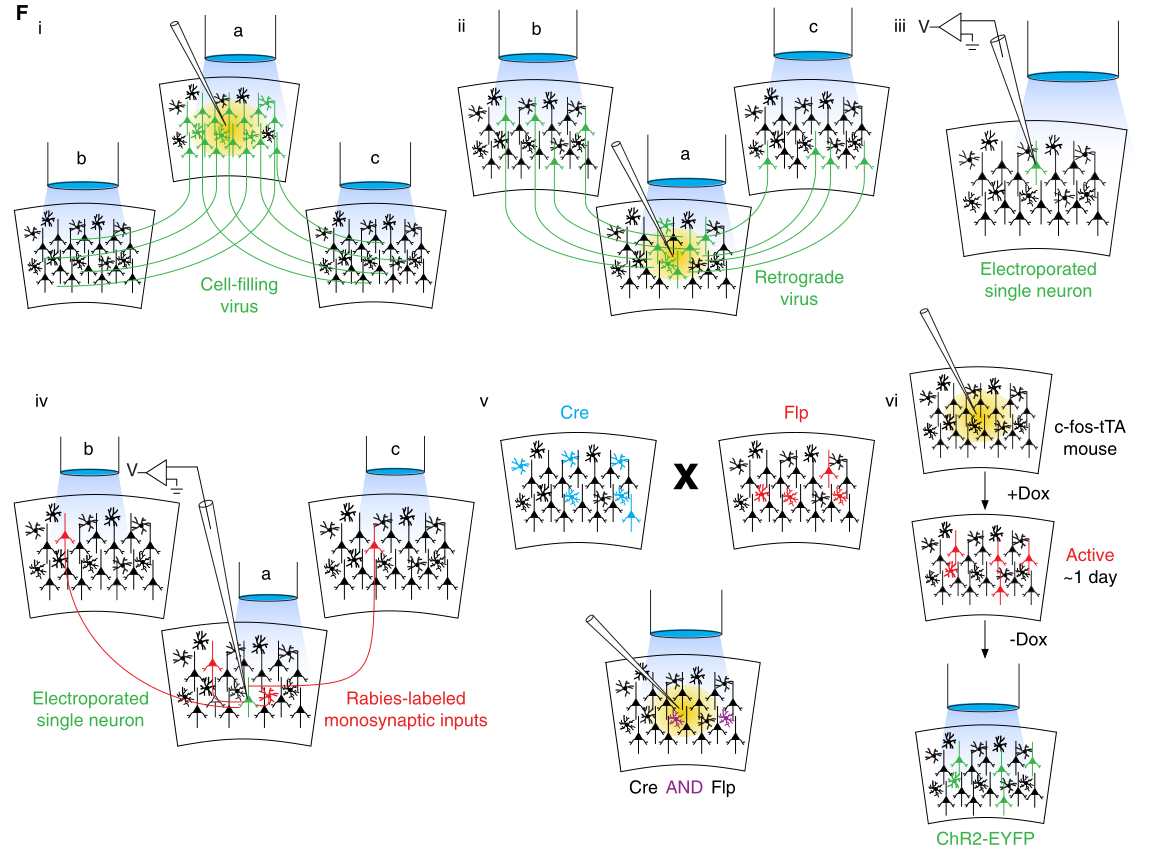
图4.闭环光遗传学的神经元靶向策略
四、闭环光遗传学在自由活动动物中的运用
通过特异性的标记特定的细胞群体,结合闭环光遗传学,通过光纤记录将神经元活性反馈,并通过光刺激器将神经元活性保持在特定的生理范围,以达到重复诱导的生理行为的发生。例如,在自由行为的动物中对表达酪氨酸羟化酶的VTA神经元进行特异性标记,标记之初便通过光纤钙成像记录神经元的初始活性,随后表达红光激发的视蛋白C1V1和蓝光激发的钙指示剂GCaMP3,在动物活动期间对VTA脑区表达酪氨酸羟化酶的神经元光纤钙成像记录和光遗传学刺激,当神经元钙活性异常时,能通过光遗传学刺激恢复到正常的神经元活性,形成活体动物的闭环光遗传学系统。
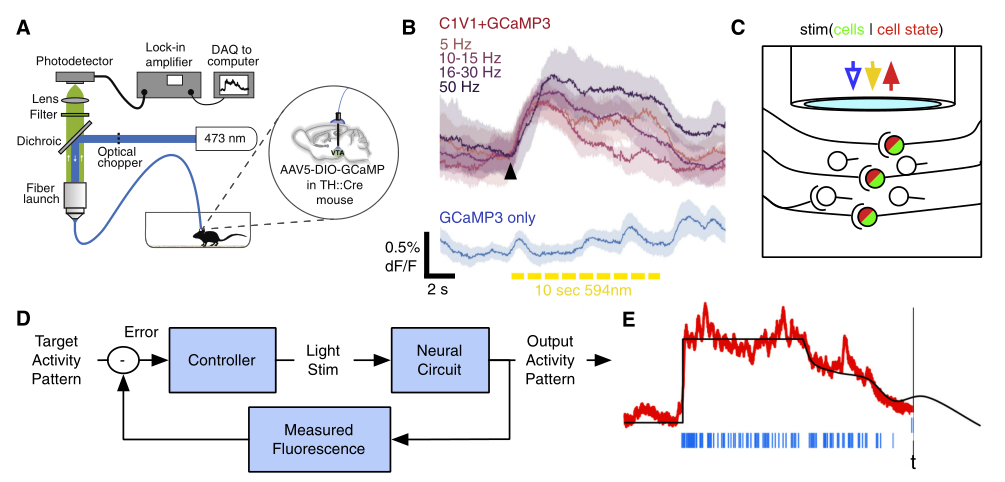
图5.闭环光遗传的在自由活动动物中的运用
五、闭环光遗传学对神经元群体的精细化调控
近年来已经有许多工具可与光遗传学兼容,在细胞分辨率尺度上实现光遗传学刺激和神经活动的光学成像。这些工具可具体分类为单光子配对视蛋白和双光子配对视蛋白。单光子荧光成像模式用于活动观察的可以细分为宽场成像、光片成像和光场成像。双光子成像方法在用于活动观察时主要有双光子激光扫描显微镜、双光子景深扩展和双光子3D随机扫描,这些方法都可构建二维和三维的功能成像。基于光子成像的激光扫描,可通过时间序列和全息影像的组合配合光遗传学刺激,通过在三维空间中同时聚焦多个衍射的双光子点,实时监测至少十个神经元细胞的动态变化,并能以单细胞分辨率模式在体外和体内进行特定区域的光刺激。
闭关光遗传学的一个重要问题是对于何种类型的神经元进行光刺激才能有比较好的实验效果。研究人员通过电生理记录海马脑区和神经元成像的方式来筛选神经网络中高度连接的神经元,发现这些高度连接的神经元似乎对更大范围的神经元网络振荡非常重要。随后根据神经元在驱动网络震荡的同步性构建算法模型,评估每一个神经元最佳震荡阶段的最佳光刺激条件,并通过网络进行进一步测试,形成一个良好的闭环光遗传学模式。一旦形成稳定的闭关光遗传学的输入输出模式,便可以选择适当的输入,尝试在复杂的神经元网络中实现特定神经元的活性干预。
然而目前闭环光遗传学在神经元群体中的精细化调控的应用还比较困难,因为同时对多个神经元进行在线预测和操纵,是一个非常复杂的神经工程学问题。但是,鉴于上述在神经元成像、光学传感器和光刺激器优化方面的显著技术进步,作者相信实现闭环光遗传学在神经元群体中的精细化调控只是一个时间问题。
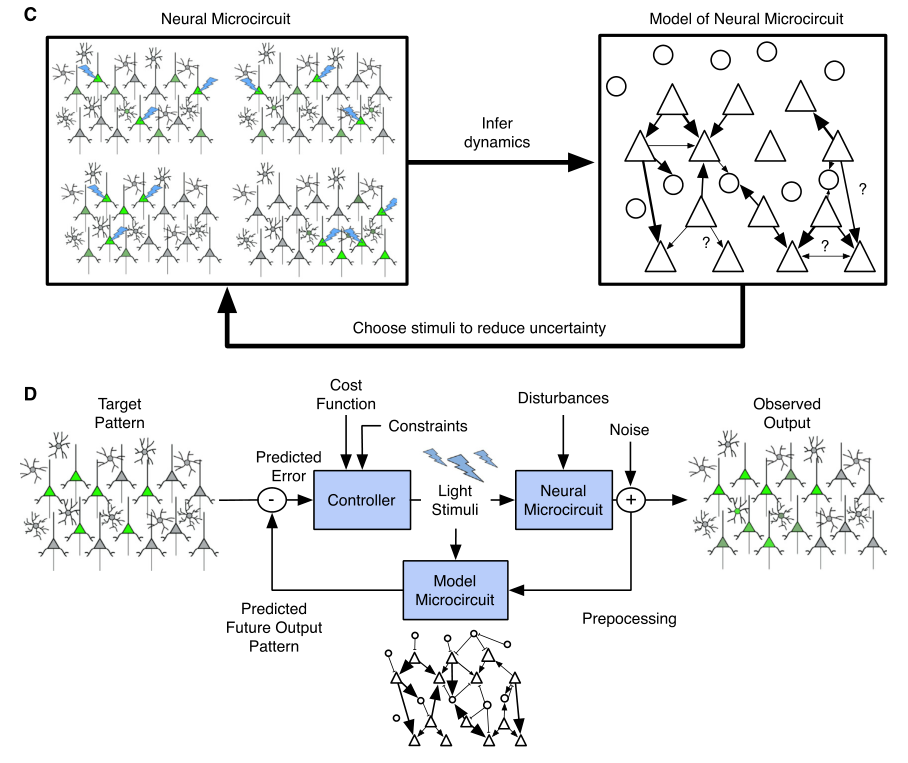
图6.闭环光遗传学在神经元群体中的精细化调控
展望
基于长期的电生理学、药理学、影像学和临床研究,传统(开环)的光遗传学已经确定了许多特定的神经细胞群体的活动模式和对特定行为结果的影响。然而,即使取得了如此巨大的进步,仍然很难从如此复杂的神经网络中进行检测和调节特定的神经元类型,并取得良好的行为效应。随着闭环光遗传学技术的不断成熟,相信在不久的将来,通过闭环光遗传学技术将获得神经元活动模式的最基本但却最有效的特征,从而提高对正常大脑功能和神经精神疾病症状的理解,并开发相应的治疗策略。
图片来源:Neuron
原文链接:http://dx.doi.org/10.1016/j.neuron.2015.03.034

扫码查看原文

市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK