2026-03-26 阅读量:146
临床药物研发常面临药物系统毒性高、稳定性不足、靶向性有限以及生物利用度低等多重药理学挑战。递送载体通过实现药物的高效封装、稳定保护与靶向递送,有效破解上述难题,已成为当今生物医药领域的核心工具。近年来,高分子递送材料[尤其是具备出色生物互作特性的材料,如聚乙二醇(PEG)、聚乳酸-羟基乙酸共聚物(PLGA)、聚乙烯亚胺(PEI)]已在临床普及应用,显著推动了肿瘤靶向化疗、mRNA疫苗、小干扰RNA(siRNA)疗法及基因递送等多种前沿治疗策略的转化。然而,药物载体经静脉注射后普遍面临严重的非选择性系统清除问题,导致实际到达靶组织的有效剂量极低,严重限制了治疗效果。尽管已知肝脏单核吞噬系统是介导该过程的主要细胞群体,但当前领域既缺乏安全且具有普适性的干预策略,也尚未建立能够系统解释其高效清除行为的机制框架。相关研究长期停留在现象描述但机制缺失的状态,难以进一步实现实质性突破。
2026年3月19日,中国科学技术大学王育才教授团队在Science发表题为“Commensal-driven serotonin production modulates in vivo delivery of synthetic and viral vectors”的研究论文。汪沁、陈子琦和张国荣博士为文章共同第一作者,王育才、朱书和蒋为教授为本研究的通讯作者。研究团队通过系统的多器官偶联活体显微成像和多平台递送体系验证:药物递送过程本质上是材料与机体生理系统相互作用的结果,限制其递送效率的关键环节来源于多器官之间的动态调控,而非仅仅单一材料参数的优化;通过干预新发现的递送调控机制,可以广谱性提升各类高分子及病毒类递送载体的终端递送效率与疗效。这一认识将递送问题从传统“材料优化”范式提升至“系统调控”层面,为后续递送载体材料的理性设计提供了新的理论指导框架。
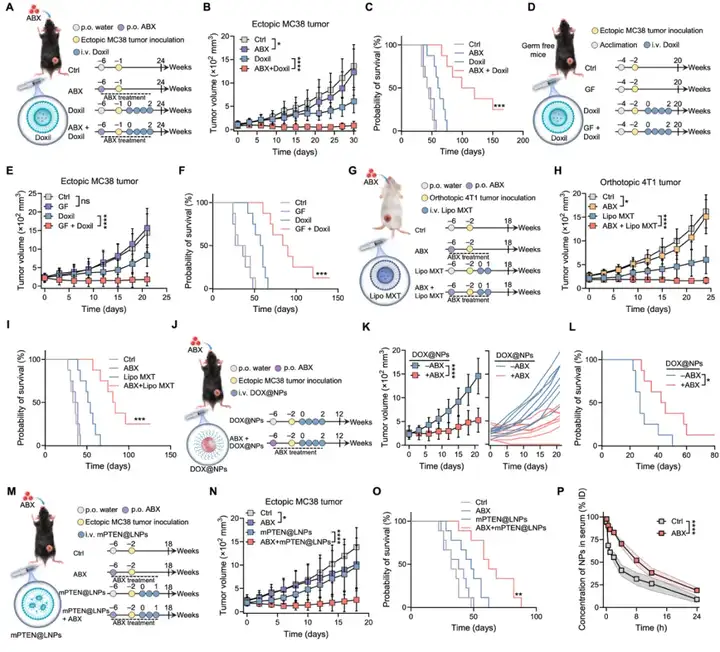
团队发现,清除小鼠肠道共生菌可显著提升多类载体向肿瘤组织的递送效率,包括聚合物纳米颗粒、脂质纳米颗粒(LNP)、脂质体、白蛋白纳米颗粒等合成载体,以及腺病毒(AdV)和溶瘤腺病毒(OA)等病毒载体(图1),并且这种递送效率的提升可直接转化为多种抗肿瘤治疗策略的疗效增强。例如,联合肠道菌清除与纳米化疗药物处理,可显著提高结肠癌、乳腺癌、黑色素瘤小鼠对化疗的响应性,将各类化疗药物的抗肿瘤疗效提升5倍以上。除肿瘤治疗外,肠道菌清除可显著增强高分子载体与病毒载体介导的多器官体细胞基因编辑效率,并提高基于mRNA的蛋白替代疗法的治疗效果。这些结果表明,肠道共生菌在生理稳态下对载体的体内递送具有普遍性的抑制作用。
图1、肠道共生菌缺失可广谱性提高各类载体的血液循环能力,从而显著增强载体的系统性递送效率与相关疗法的疗效
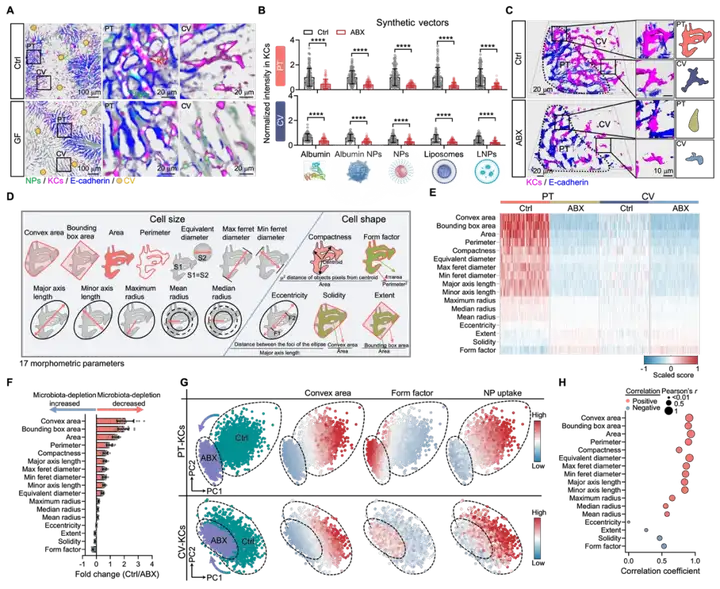
为解析肠道共生菌调控载体体内循环的机制,团队开发了一套基于活体成像的单细胞形态及载体定量分析系统,实现了在活体水平对载体与细胞之间动态互作过程的实时追踪(图2)。基于该分析平台,团队构建了肝脏吞噬细胞(Kupffer cells,KCs)在不同生理状态下的行为与形态学全景图谱,定量揭示了肠道共生菌对肝脏KCs功能状态的调控作用,发现肠道菌清除可显著抑制肝脏KCs对各类载体的摄取能力(下降幅度最高可达70%),并诱导其发生显著的形态学重塑和表型转变。以上结果表明,肝脏KCs的稳态吞噬功能依赖于肠道菌的持续调节。
图2、使用活体成像研究高分子载体的体内转运与生物互作过程
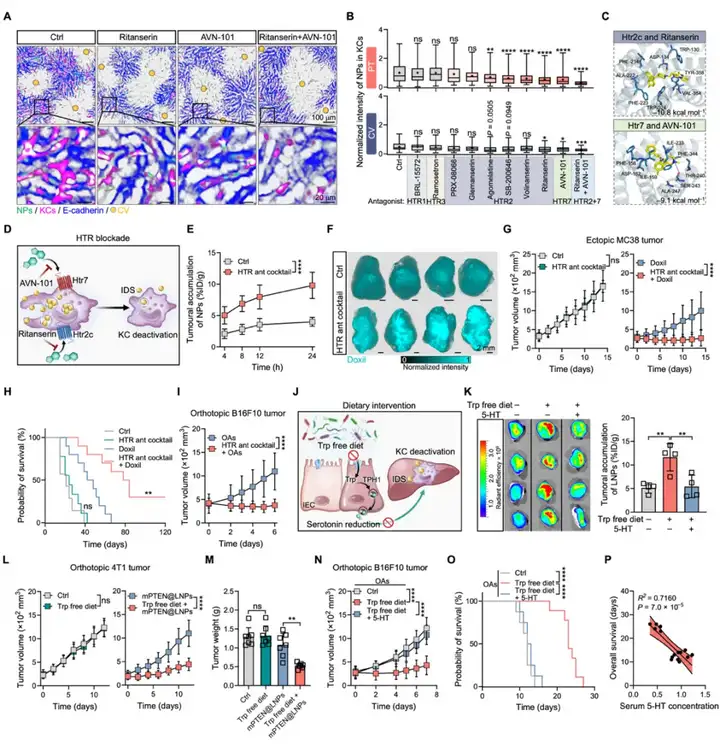
在应用层面,针对血清素(5-羟色胺,5-HT)信号轴的干预为提升体内递送效率提供了一种无需改造材料本身的普适性策略。无论是通过药理学手段阻断5-HT刺激信号,还是通过饮食限制其前体色氨酸的摄入,均可有效抑制肝脏KCs介导的非特异性清除,从而系统性延长载体循环时间并增强其靶向递送能力,在多种治疗模型中实现显著的疗效提升(图3)。
图3、靶向干预5-HT信号轴可显著增强各类载体的系统性递送效率与相关疗法的疗效
结论
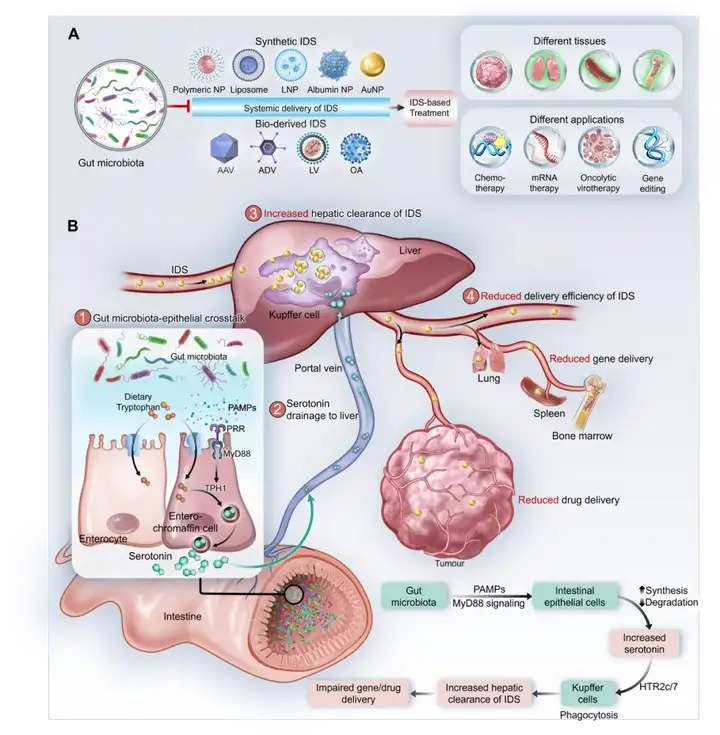
总体而言,团队证实了该清除调控机制作为跨器官网络的关键节点,对高分子载体递送效率具有决定性的核心作用。该研究不仅揭示了影响递送效率的关键系统性机制,也重塑了材料领域对体内递送问题的基本认知边界,为精准肿瘤治疗与基因治疗等依赖高效体内递送的前沿技术提供了新的解决路径。
图4、机体清除药物递送载体的底层机制与调控策略
中国科学技术大学王育才教授、朱书教授、蒋为教授为本论文的共同通讯作者,汪沁博士、博士生陈子琦、张国荣特任副研究员为该论文共同第一作者。中国科学技术大学附属第一医院张树庚主任为本研究提供了重要支持。本研究获国家自然科学基金、国家重点研发计划、中国科协青年人才托举工程、中国科学院战略性先导科技专项、安徽省自然科学基金等科技项目资助。
团队主要成员合影
王育才教授团队介绍
王育才教授团队在高分子药物递送载体材料的理性设计、体内转运及临床转化研究领域深耕多年并积累了丰富经验,通过提出“机制指导的系统性递送载体优化”策略,团队发现并设计突破了多种递送屏障,为各类载体体系的高效递送提供了可行的思路。团队从突破基底膜屏障提升肿瘤递送效率(Nat. Nanotechnol. 2024, 19 (1): 95-105)、到利用一氧化氮精准调控肿瘤血管双层屏障增强纳米颗粒穿透(Nat. Biomed. Eng. 2025, 9 (9): 1486-1501),再到构建口服抗生素递送平台实现肠道上皮靶向性递送(Nat. Biomed. Eng. 2022, 6 (7): 867-881),同时在器官选择性mRNA递送方向上,先后实现了咪唑类离子化脂质介导的脾脏特异性递送(J. Am. Chem. Soc. 2024, 146 (22): 15085-15095)、自体抗原呈递细胞原位递送编辑(Nat. Biomed. Eng. 2025, 9 (8): 1320-1334)与聚合物—脂质整合纳米颗粒的器官选择性定量设计(J. Am. Chem. Soc. 2026, http://doi.org/10.1021/jacs.5c22504)等一系列成果为本次突破奠定了坚实基础。总体而言,该研究从机体系统调控层面深化了对载体清除机制的认识,在一定程度上突破了长期以来限制递送效率的非特异性清除瓶颈,并推动该领域由“材料优化”向“系统调控”范式转变,为构建可预测、可调控的体内递送体系提供了新的理论基础与实现路径。
本文使用的来自枢密科技的病毒产品,列表如下:

扫码添加客服
更多产品及详情欢迎咨询!


市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK