2023-09-14 阅读量:398
腺病毒(Adenovirus,AdV)是直径约为70-100 nm、空间结构为立体对称的20面体、衣壳由252个壳粒组成的无包膜线性双链DNA病毒。目前已知的人腺病毒血清型有51种,根据组织嗜性不同被分成ABCDEF六个不同亚群,其中C亚群的第2和第5血清型为最常见的腺病毒载体。基于人腺病毒5型(Ad5)改造的载体使用较为广泛,其特点是人为地删除了E1和E3基因,导致腺病毒失去复制能力和一定程度上降低免疫原性,使得Ad5成为一种广泛、安全、有效的基因运输载体。腺病毒除了用作基因治疗药物载体和疫苗载体以外,在基础生物医学研究上也受到科研工作者的青睐,可以搭载最高达8kb大小的目的基因。
1.腺病毒基因组不会整合到宿主细胞中,可以直接进行翻译和转录,相比RNA病毒起效更快。
2.腺病毒感染能力强,转导效率高,是体外难感染细胞最佳选择;对于细胞实验在感染后36-48小时会出现表达高峰;对于动物实验则在5天左右即达到表达高峰,表达效果可维持1-3周左右。
3.腺病毒具有嗜肝性,尾静脉注射主要感染肝脏。
那么腺病毒作为基因递送载体在疾病治疗及发病机制研究中有哪些应用呢?
一、利用AdV过表达KLK8诱导海马神经元凋亡(Xu DH, et al. Cell Death Dis. 2023.)
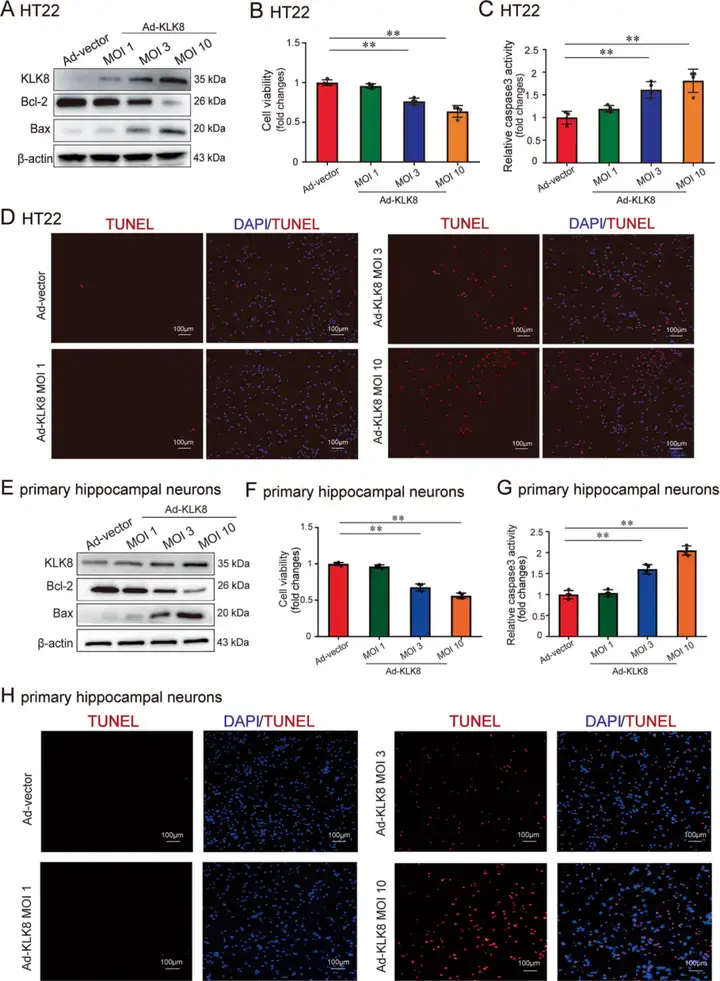
既往研究显示神经元凋亡已被公认为抑郁症发病机制中的关键一环。组织激肽释放酶相关肽酶8(KLK8)是一种胰蛋白酶样丝氨酸蛋白酶,与包括抑郁症在内的多种精神疾病的发病机制有关。于是,Xu Dan-Hong等人探究KLK8在慢性不可预知轻度应激(CUMS)诱导的抑郁症啮齿动物模型中对海马神经元细胞凋亡的潜在影响。研究人员首先证明CUMS成功诱导小鼠抑郁表型,而前人研究表明海马、内侧前额叶皮层(mPFC)和杏仁核均参与CUMS诱导的抑郁样行为,于是,进一步检测发现海马中KLK8表达显著上调,且是三个脑区中表达水平最高的。接下来,作者发现海马KLK8上调与抑郁表型相关,并证明KLK8转基因大鼠中CUMS诱导的抑郁样行为和海马神经元凋亡增加,而KLK8敲除小鼠中CUMS诱导的抑郁样行为及海马神经元凋亡减少。因此,作者继续研究KLK8对神经元凋亡的直接影响。利用表达KLK8的腺病毒载体(Ad-KLK8)以递增的MOI分别感染HT22小鼠海马神经元细胞和原代海马神经元。结果表明Ad-KLK8以剂量依赖方式分别在HT22和原代海马神经元中诱导细胞损伤(细胞活力降低);增加caspase-3(蛋白酶,凋亡效应因子)活性、促凋亡蛋白Bax表达和TUNEL阳性细胞比例,并使抗凋亡蛋白Bcl-2表达降低。即KLK8过表达在体外诱导海马神经元凋亡。
图1. KLK8过表达在体外诱导神经元凋亡(A-D:HT22小鼠海马神经元细胞,E-H:原代海马神经元)
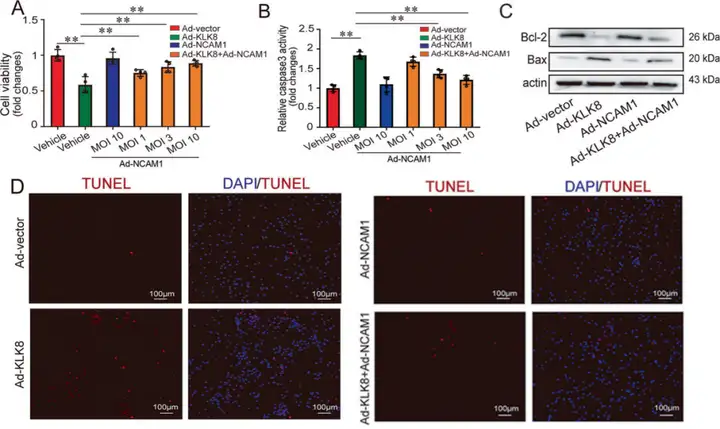
进一步研究发现,NCAM1(神经细胞粘附分子1)是海马神经元中KLK8的潜在底物。为确认NCAM1是否参与KLK8过表达诱导的神经元凋亡,研究人员在感染Ad-KLK8的HT22细胞中继续感染Ad-NCAM1,结果表明Ad-NCAM1以剂量依赖方式阻碍HT22细胞中Ad-KLK8诱导细胞损伤的增加;caspase-3蛋白活性、Bax表达和TUNEL阳性细胞比例的增加,及Bcl-2表达的降低。
图2. NCAM1过表达拯救KLK8过表达诱导的HT22细胞凋亡
二、利用AdV过表达CSF2RB促进缺血性心力衰竭中静脉递送MSCs的疗效(Qi T, et al. Theranostics. 2023.)
对于缺血性心力衰竭而言,间充质基质细胞(MSCs)的侵入性心肌内注射只允许有限的重复注射,且疗效较差。静脉注射是一种替代方法,因为这种途径能重复、无创且易于递送。然而,静脉注射后由于MSCs缺乏靶向性使这些细胞无法在心肌缺血区域累积。
多项研究表明,CSF2(集落刺激因子2)在梗死区的表达显著增加,并损害心肌缺血(MI)后的康复。也有研究表明CSF2还作为内源性损伤信号,通过增强MSCs的多谱系分化和迁移能力,促进行子宫内膜切除术动物模型中MSCs的疗效。此外,西京医院心血管内科陶凌主任医师课题组前期研究表明鸢尾素通过上调集落刺激因子2受体β亚基(CSF2RB,CSF2受体之一)显著增加心肌缺血/再灌注(MI/R)模型小鼠静脉注射MSCs的心脏归位。于是,该课题组成员Qi Tingting等人探究CSF2RB的过表达是否以及如何调控MSCs的心脏归位及它们对缺血性心力衰竭的心脏保护作用。研究人员对成年C57BL/6J小鼠进行MI/R或假手术。观察到MI/R后缺血心脏CSF2蛋白表达和分泌显著增加。随后在分离自小鼠附睾脂肪的脂肪组织来源间充质基质细胞(ADSCs)中感染携带CSF2RB基因的腺病毒(MOI=50时显著增加CSF2RB蛋白表达且不影响细胞活力),MI/R后3天开始小鼠每三天静脉注射ADSCs(ADSC-NC和ADSC-CSF2RB),共7次。MI/R后第22天利用2种方法分析ADSCs在小鼠体内器官中的分布。第一种方法小动物活体成像技术中ADSCs被亲脂性近红外荧光染料DiR标记,检测DiR荧光信号。结果显示MI/R+ADSC-CSF2RB小鼠心脏组织中DiR信号明显更高(而MI/R+ADSC-CSF2RB与MI/R+ADSC-NC两组肺、肝和脾组织中DiR信号相同)。第二种方法是利用从绿色荧光蛋白EGFP转基因小鼠附睾脂肪分离的ADSCs(被EGFP标记),并通过EGFP免疫染色以量化心脏、肺、肝和脾脏切片中EGFP阳性细胞的数量。结果显示CSF2RB过表达显著增加静脉注射ADSC-GFP的心脏归位。值得一提的是,几乎所有的ADSC-GFP都是在肌钙蛋白T阴性的心脏组织梗死区。总的来说,这些结果表明CSF2RB过表达特异性增加静脉递送ADSCs在心脏的植入。
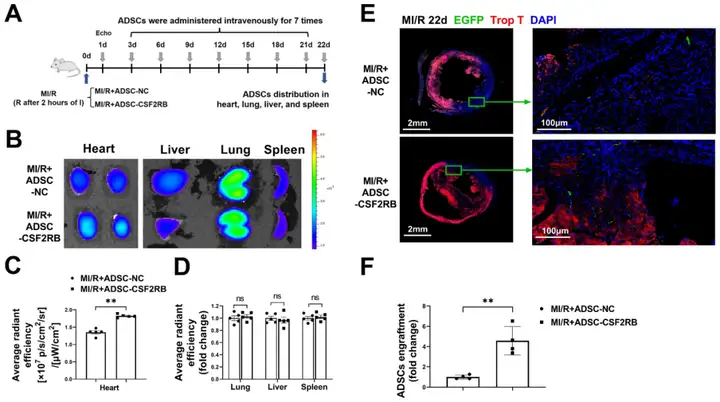
图3. CSF2RB过表达增加静脉递送ADSCs的心脏归位
下一步,研究人员评估静脉递送ADSCs对MI/R小鼠的心脏保护作用。与MI/R + Vehicle相比,MI/R后三周ADSC-NC的静脉递送并没有显著增加左心室射血分数LVEF,但轻微降低左心室舒张末期内径LVEDD和左心室收缩末期内径LVESD;而ADSC-CSF2RB组显著增加了LVEF,降低了LVEDD和LVESD。MI/R后6周发现ADSC-NC和ADSC-CSF2RB都显著增加LVEF,降低LVEDD和LVESD。更为重要的是,相比于ADSC-NC组,ADSC-CSF2RB组小鼠LVEF、LVEDD和LVESD得到进一步改善。此外,与Sham组比较,MI/R后6周MI/R+Vehicle组左心室收缩末期压LVESP、左心室收缩时室内压最大上升速率dP/dtmax显著降低,左心室舒张末期压LVEDP、左心室舒张时室内压最大下降速率-dP/dtmax明显增加。相比于MI/R+Vehicle,ADSC-NC治疗显著降低LVEDP和-dP/dtmax,但没显著增加LVESP或dP/dtmax;而ADSC-CSF2RB治疗则几乎完全恢复LVESP、LVEDP和±dP/dtmax。表明ADSC-CSF2RB对MI/R小鼠心功能的改善更强。综合来看,这些结果清楚地表明静脉注射过表达CSF2RB的ADSCs增强ADSC介导的长期MI/R小鼠模型中心功能的提高。
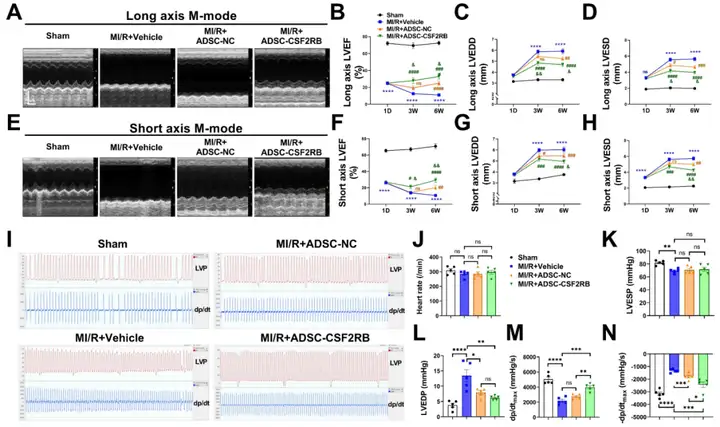
图4. CSF2RB过表达增强静脉递送ADSCs改善MI/R后心功能的效果
三、利用AdV过表达LAPTM5减轻非酒精性脂肪性肝炎(NASH)(Jiang L, et al. Nat Commun. 2023.)
非酒精性脂肪肝炎(NASH)是发展为肝硬化和肝癌的主要原因,其病理特征是肝脂肪性病变、肝细胞气球样变、肝小叶和肝脏炎症以及间质纤维化。目前,预防和治疗NASH的有效措施仍然有限,还没有相应的治疗药物,因此寻找NASH的分子靶点也越来越受到重视。近年来,许多研究证明溶酶体调节许多疾病的发生发展。其中溶酶体相关跨膜蛋白5(LAPTM5)是LAPTM家族成员之一,可作为一些疾病的干预靶点。研究表明,LAPTM5作为炎症信号通路的调节因子,通过调节MAPK信号通路活性来改善心肌肥大;MAPK信号通路的激活与NASH的发展和进展密切相关。因此,研究人员提出假设LAPTM5参与调控NASH的发生发展。作者首先发现LAPTM5在脂肪肝中表达下调并与NASH进展相关,LAPTM5蛋白水平与NAS评分呈负相关。因此,研究人员继续探讨LAPTM5对肝细胞脂质代谢和炎症的影响,从C57BL/6小鼠中分离出原代肝细胞,并感染过表达Laptm5的腺病毒载体(AdLaptm5-Flag),尼罗红染色显示,与AdGFP组相比,AdLaptm5组棕榈酸/油酸(PAOA)诱导的肝细胞脂质积累明显改善并伴有甘油三酯(TG)和总胆固醇(TC)浓度的降低,而两组牛血清白蛋白(BSA)处理后肝细胞脂质沉积无显著差异。此外,qPCR和Western blotting结果(脂肪酸代谢相关、炎症相关标志物的表达水平)进一步证实了LAPTM5对脂质代谢和炎症的抑制作用。总的来说,体外实验结果表明,LAPTM5对代谢应激诱导的肝细胞脂质沉积和炎症发挥保护作用。
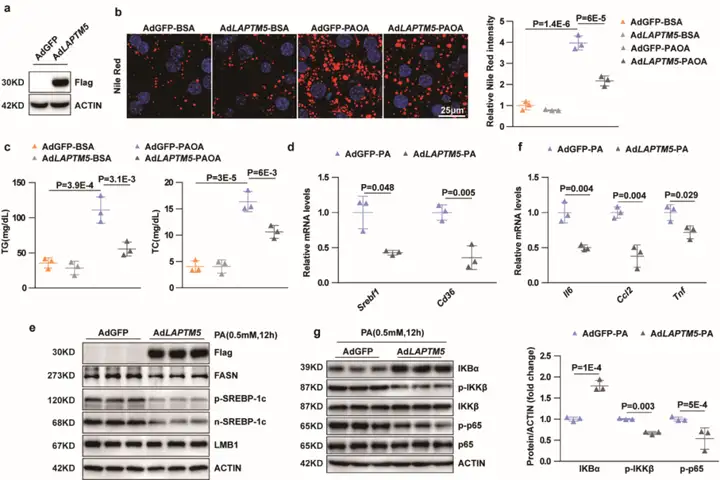
图5. LAPTM5抑制肝细胞脂质积累和炎症
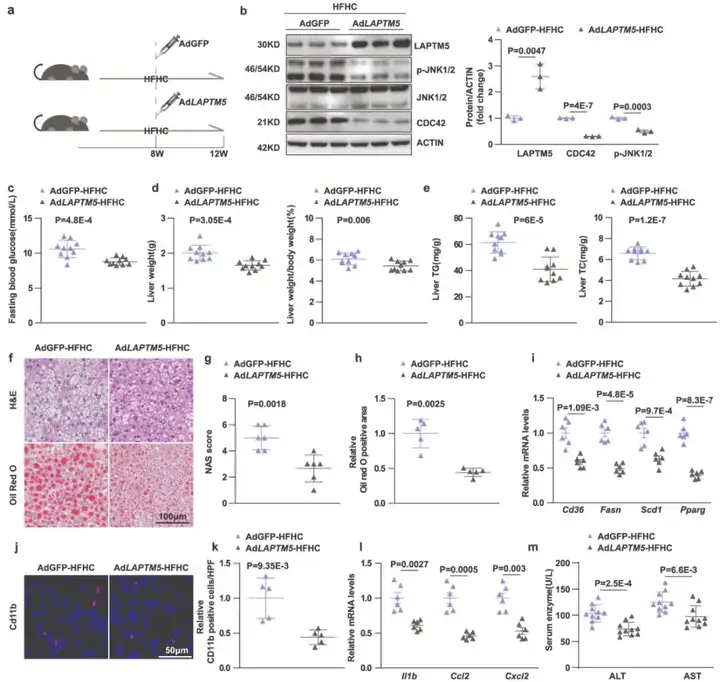
此外,作者探讨LAPTM5对NASH的治疗效果。将过表达Laptm5的腺病毒(AdLAPTM5)注射到已接受8周高脂高胆固醇(HFHC)饮食(诱导NASH模型)的小鼠体内,再进行HFHC喂养4周,以AdGFP为对照。结果发现,与AdGFP组相比,AdLaptm5组空腹血糖、肝重量和肝重量与体重的比值显著降低,明显改善HFHC喂养小鼠肝脏中的脂质积累、炎症和肝损伤。综上所述,上述结果表明腺病毒介导的肝脏Laptm5过表达可改善NASH,证明LAPTM5作为NASH和代谢紊乱的治疗靶点前景巨大。
图6. 腺病毒介导的肝脏Laptm5过表达减轻NASH
参考文献
[1]Xu DH, Du JK, Liu SY, et al. Upregulation of KLK8 contributes to CUMS-induced hippocampal neuronal apoptosis by cleaving NCAM1. Cell Death Dis. 2023 Apr 19;14(4):278.
[2]Qi T, Xu X, Guo Y, et al. CSF2RB overexpression promotes the protective effects of mesenchymal stromal cells against ischemic heart injury. Theranostics. 2023 Mar 13;13(6):1759-1773.
[3]Jiang L, Zhao J, Yang Q, et al. Lysosomal-associated protein transmembrane 5 ameliorates non-alcoholic steatohepatitis by promoting the degradation of CDC42 in mice. Nat Commun. 2023 May 8;14(1):2654.

市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK